理想气体示例问题:分压
在任何气体混合物中,每种组分气体都会产生一个构成总压的分压。在正常温度和压力下,可以应用理想气体定律来计算每种气体的分压。


什么是分压(partial pressure)?
让我们先回顾一下分压的概念。在气体混合物中,每种气体的分压是气体在占据该体积空间时所施加的压力。如果你把混合物中每种气体的分压加起来,这个值就是气体的总压。用于确定分压的定律假设系统温度恒定,气体表现为理想气体,遵循理想气体定律:
PV=nRT
其中P是压力,V是体积,n是摩尔数,R是气体常数,T是温度。
然后,总压力是组成气体的所有分压之和。对于气体的n组分:
Ptotal=P1+P2+P3+。。。Pn
当用这种方式写时,理想气体定律的这种变化称为道尔顿分压定律。围绕这些术语,该定律可以改写为气体摩尔数和总压与分压之间的关系:
Px=Ptotal(n/ntotal)
分压问题
气球含有0.1摩尔的氧和0.4摩尔的氮。如果气球处于标准温度和压力下,氮气的分压是多少?
解决方案
分压由道尔顿定律确定:
Px=PTotal(nx/nTotal)
式中px=气体分压xPTotal=所有气体的总压nx=气体的摩尔数xnTotal=所有气体的摩尔数
第一步
找到托托
虽然问题没有明确说明压力,但它确实告诉您气球处于标准温度和压力。标准压力为1大气压。
步骤2
把组分气体的摩尔数加起来,算出总摩尔数
nTotal=noxygen+nnitrogennTotal=0.1 mol+0.4 mol=0.5 mol
步骤3
现在你有了所有需要的信息,可以把这些值插入方程中,求解Pnitrogen
Pnitrogen=PTotal(nnitrogen/nTotal)Pnitrogen=1 atm(0.4 mol/0.5 mol)Pnitrogen=0.8 atm
答复
氮气的分压为0.8 atm。
执行分压计算的有用提示
- 请务必正确报告您的单位!通常,当使用任何形式的理想气体定律时,你们要处理的是摩尔质量,开尔文温度,升体积,大气压力。如果温度以摄氏度或华氏度为单位,请在继续之前将其转换为开尔文。
- 请记住,真实气体不是理想气体,因此,尽管在一般情况下,计算误差很小,但它不会精确到真实值。在大多数情况下,误差可以忽略不计。误差随着气体压力和温度的增加而增加,因为粒子之间的相互作用更加频繁。
- 发表于 2021-10-14 15:45
- 阅读 ( 222 )
- 分类:化学
你可能感兴趣的文章
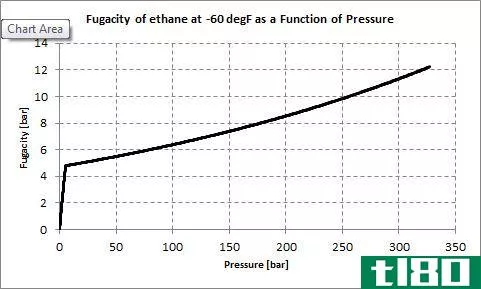
活动(activity)和逸度(fugacity)的区别
... 活度和逸度的关键区别在于活度是指一种化学物质在非理想条件下的有效浓度,而逸度是指一种化学物质在非理想条件下的有效分压。 活度和逸度是热力学中重要的化学概念。这些术语是为真实气体的非理想行为而定义的。 ...
- 发布于 2020-10-11 20:15
- 阅读 ( 948 )
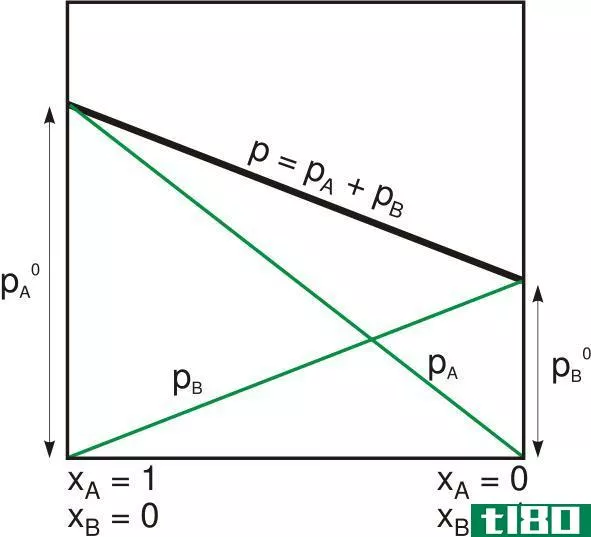
拉乌尔定律(raoult law)和道尔顿定律(dalton law)的区别
...是拉乌尔定律背后的基本理论。然而,拉乌尔定律适用于理想解。但它也能很好地与溶剂在非常稀的状态。对于真实物质(非理想物质),蒸气压的下降实际上大于我们根据拉乌尔定律计算的值。 什么是道尔顿定律(dalton law)? ...
- 发布于 2020-10-16 16:00
- 阅读 ( 973 )
kc公司(kc)和kp公司(kp)的区别
...数,以产物和反应物的压力之比表示。该平衡常数适用于气体反应混合物。Kp取决于反应混合物中气体成分的分压。 图1:混合物中气体成分的分压。 pP+qQ↔ rR+sS 上述反应的平衡常数可以写成: Kp=pRr.pSs/ 购买力平价 “p”表示分...
- 发布于 2020-10-19 00:35
- 阅读 ( 274 )
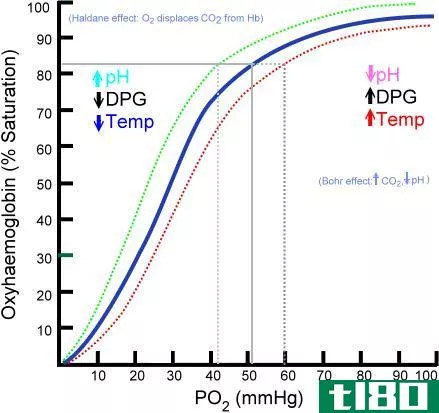
pao2(pao2)和二氧化硫(sao2)的区别
...关键的过程,受许多因素的影响,如血液的pH值、血液中气体的分压、O2的饱和水平、有效血红蛋白的浓度和心脏效率。这些因素的平衡将确保根据特定组织的需要将氧气有效地输送到外周组织。氧分压和氧饱和度是决定氧在血...
- 发布于 2020-10-20 16:31
- 阅读 ( 410 )
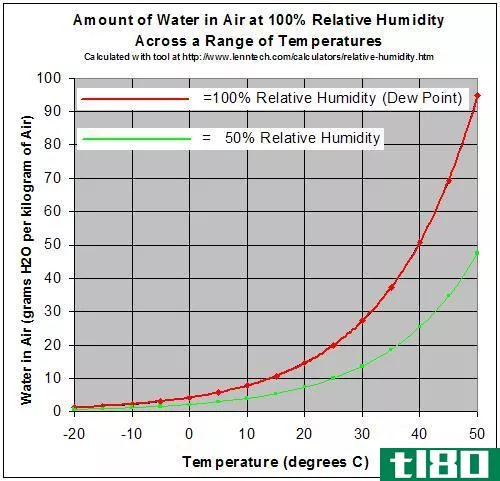
绝对的(absolute)和相对湿度(relative humidity)的区别
...气体G2产生压力P2。混合物中G1的分压为P1/(P1+P2)。对于理想气体,这也等于A1/(A1+A2)。第二个必须理解的概念是饱和蒸汽压。蒸汽压力是蒸汽在系统中平衡时产生的压力。 现在让我们假设在一个封闭的系统中仍然存在液态水...
- 发布于 2020-11-02 16:44
- 阅读 ( 398 )
分压(partial pressure)和蒸汽压(vapor pressure)的区别
...用力较强的溶液中,蒸气压较小。 蒸汽压也可以发生在理想的混合物中,这可以用拉乌尔定律来解释。它指出,液体或固体混合物**定组分的部分蒸汽压等于该组分的蒸汽压乘以给定温度下该混合物中该组分的摩尔分数。下面的...
- 发布于 2021-06-25 01:21
- 阅读 ( 559 )
分压(partial pressure)和蒸汽压(vapor pressure)的区别
...的两种压力。分压和蒸气压之间的主要区别在于,分压是气体混合物中单个气体施加的压力,而蒸气压是与冷凝形式平衡的蒸汽施加的压力。 覆盖的关键领域 1.什么是分压–定义、特征、计算2.什么是蒸气压–定义、特征、影响...
- 发布于 2021-06-28 18:52
- 阅读 ( 531 )
亨利定律(henry’s law)和拉乌尔定律(raoult’s law)的区别
...}p等于该体系的总蒸气压=PA+PB 然而,拉乌尔定律只适用于理想解。理想溶液是由溶质分子间相互作用等于溶剂分子间相互作用的溶质组成的。由于不存在可被视为理想气体的实际溶液,我们可以将此定律应用于溶质分子量较少的...
- 发布于 2021-06-29 11:05
- 阅读 ( 947 )
通风(ventilation)和呼吸(respiration)的区别
...气是向肺部提供新鲜空气,呼吸是身体与外部环境之间的气体交换。肺是大多数脊椎动物呼吸和通气的**。吸入动物时会呼吸。肺提供血液和大气之间的密切接触,促进呼吸。 覆盖的关键领域 1.什么是通气——定义、过程、作用...
- 发布于 2021-06-29 18:02
- 阅读 ( 322 )
充氧(oxygenation)和通风(ventilation)的区别
...脉,而通气发生在吸气和呼气。 充氧和通气是动物负责气体交换的两个生理过程。 覆盖的关键领域 1.什么是氧化-定义、过程、重要性2。什么是通风-定义、过程、重要性3。氧合和通气之间有什么相似之处——共同特征概述4。...
- 发布于 2021-07-02 02:05
- 阅读 ( 396 )