亲水性vs疏水性
“Hydro”是指水。从地球演化的最初阶段起,水一直是地球的主要组成部分。今天,水覆盖了地球表面70%以上的面积。从这一点来看,大部分的水在海洋中,约占97%。河流、湖泊和池塘有0.6%的水,约2%存在于极地冰盖和冰川中。地下有一定量的水,还有一小部分以蒸汽和云层的形式存在于气体中。水是我们生活中离不开的东西。由于水是一种通用溶剂,它参与了大多数反应。它是生物中含量最丰富的无机化合物。我们身体75%以上是由水组成的。它是细胞的组成部分,起溶剂和反应物的作用。水是几乎所有生物反应的介质。因此,化合物与水相互作用的能力至关重要。这种能力的程度可以用亲水和疏水两个术语来解释。
亲水的
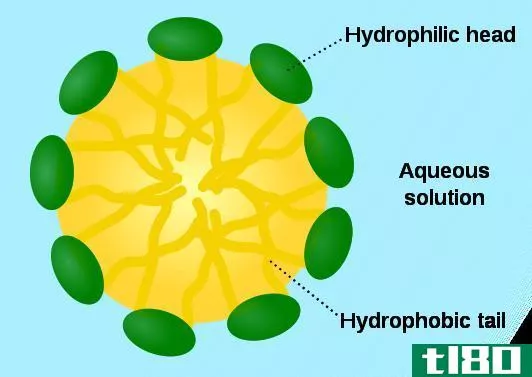
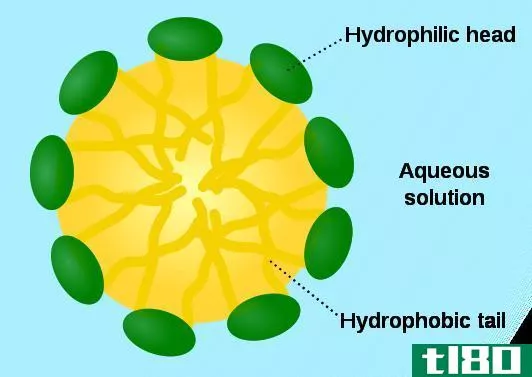
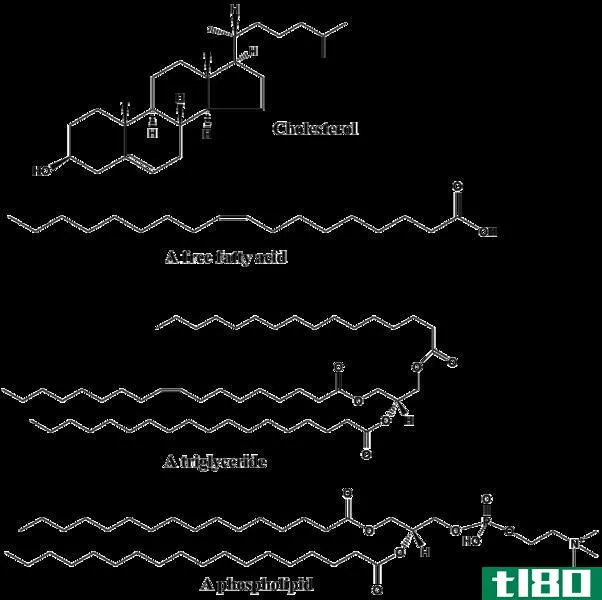
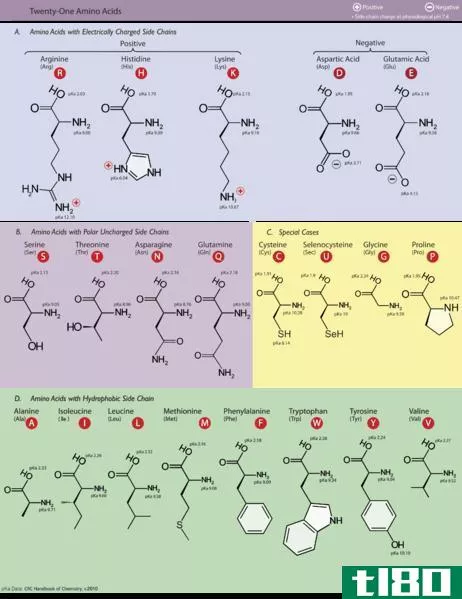
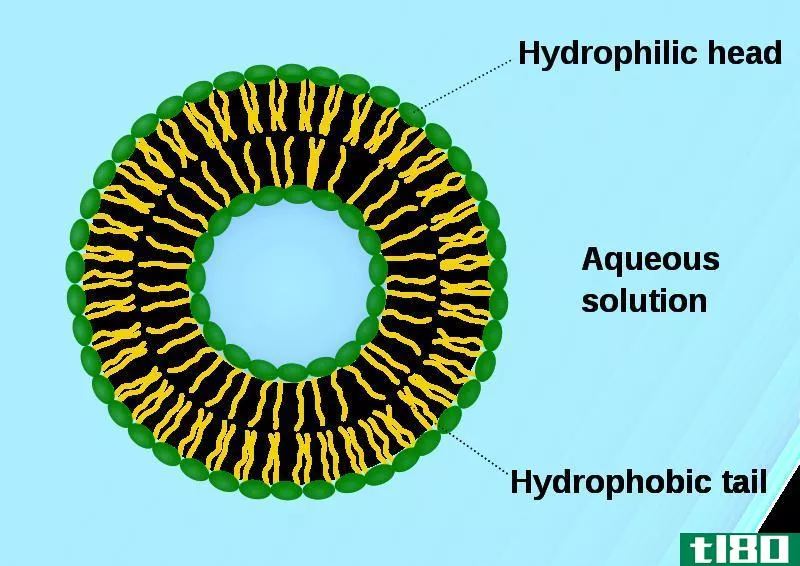
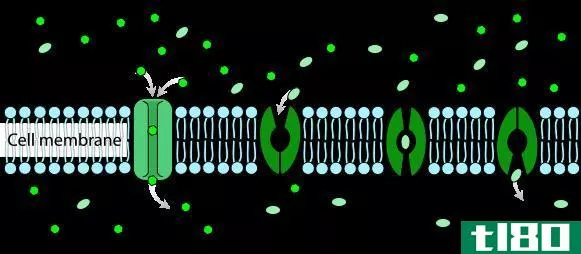
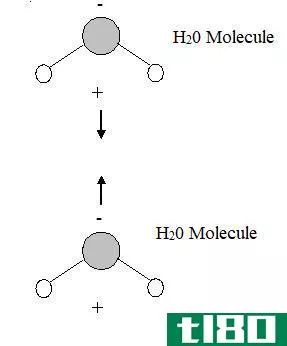
亲水意味着爱水。水是极性分子。亲水性物质是亲水性物质,因此,它们喜欢与水相互作用或溶于水。正如“类溶如水”所说,要与极性分子如水相互作用或溶解,亲水性物质也应该是极性的。所以,如果大分子中有一部分是极性的,那一端就能吸引水。例如,形成细胞膜的磷脂分子有一个亲水性的磷酸基团。虽然整个分子不是亲水的(大分子的脂质部分是疏水的),磷酸头是亲水的,因此与水相互作用。与这种分子相反,有些物质是非常亲水的。例如,盐和糖很容易吸水。它们甚至有能力从空气中吸收水分,因此当它们暴露在空气中时,它们会随着时间的推移而溶解。这是自发的,因为它是热力学上有利的。这些物质在水里会溶解,因为它们会与水形成键。通常,亲水性物质具有电荷分离,使其极性,并能与水氢键。亲水性物质用于吸水和保持材料干燥。
疏水的
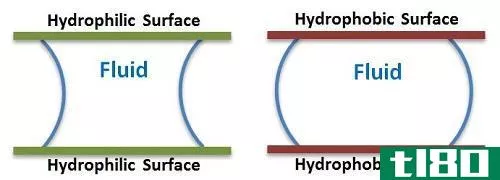
疏水性是亲水性的对立面。顾名思义,“hydro”意味着水,“恐怖”意味着恐惧。所以这些不喜欢水的物质被称为疏水性物质。因此,它们排斥水分子。非极性物质表现出这种行为。换言之,疏水性物质喜欢与油、己烷等非极性溶剂相互作用或溶解,因此,疏水性物质也被称为亲脂性(嗜脂性)。当疏水性物质在水中时,它们结合在一起并排斥水分子。疏水性溶剂对于从水中分离不溶于水的物质很重要。
| 亲水性和疏水性的区别是什么?•亲水性意味着爱水,疏水性意味着害怕水。•因此,亲水性物质与水相互作用并溶解在水中,而疏水性物质不会表现出这种行为。•亲水性物质是极性的,疏水性物质是非极性的。 |