主要区别
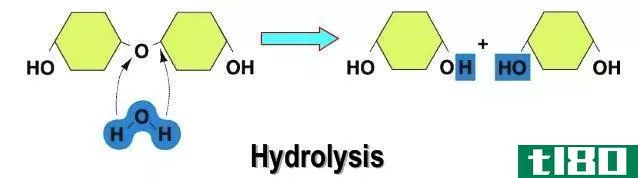
水解和水化的主要区别在于水解涉及水分子的分裂,而水合作用通常并不总是涉及水分子的分裂。
水解(hydrolysis) vs. 水合作用(hydration)
水解通常被认为是以水为反应物之一的双重分解反应过程,而水化则被认为是水分子与物质结合的化学方法。水解通常发生在水分子中的键断裂,而在有机分子中,水化通常伴随着键的断裂而发生,但在无机化合物中,有时键不会断裂。
水解通常从不饱和化合物中生成饱和化合物;另一方面,水合化合物通过脱水化合物的水合作用生成。在水解过程中,阴离子、阳离子或有时两者都与水发生反应,以改变水的pH值;相反,在水合作用中,溶质分子被溶剂分子包围。水解被认为是化学过程,因为它涉及到键和分子的破裂;另一方面,水合作用被认为是物理过程,因为它不涉及任何分子或键的化学分解。
在化学反应过程中,水解的pH值或增加或减少,其中阴离子或阳离子相对改变水的pH值;另一方面,水化的pH值在反应过程中保持恒定。水解示例为Na2CO3+2H2O→2NaOH+H2CO3;水合示例为K+Cl–+H2O→K+(aq)+Cl–(aq)。
比较图
什么是水解(hydrolysis)?
水解是一个术语,通常涉及到以水为反应物的双重分解反应过程。水解反应是经常可逆的过程。
根据Br***ted-Lowry酸碱理论,水可以作为碱或酸。这个理论是这样表述的:“酸通常产生共轭碱,当酸和碱发生反应时,碱通常通过质子交换产生共轭酸。”
如果一个水分子表现为Br***ted-Lowry酸,那么意味着水分子提供了一个质子。如果一个水分子表现为Br***ted-Lowry碱,那么通常意味着水分子通过正常生成氢离子(H3O+)接受质子。H2O、H+离子和OH-离子分别与阴离子和阳离子反应生成盐的碱和酸,生成原始碱,而原始酸一般称为水解。
水解考虑化学过程,因为它涉及到键和分子的破裂。在阴离子或阳离子相对地改变水的pH值的化学反应过程中,水解的pH值要么升高要么降低。水解类型主要有酸水解、碱水解和饱和水解。
以Na2CO3+2H2O→2NaOH+H2CO3为例,说明碳酸钠与水分子发生反应时,通常会与水分子分解生成氢氧化钠(碱)和碳酸。
水解类型
- 酸水解:与酸分解反应的相似之处通常称为酸水解。
- 碱水解:与碱解离反应的相似之处通常称为碱水解。在这种水解过程中,水通常通过形成氢氧化物离子(OH-)来提供质子。因此,这意味着水通常表现为Br***ted-Lowry酸。
- 盐水解:盐在水中混合时通常会分解成离子。当弱酸或弱碱的盐通常在水中混合时,水会使盐的混合物离子化,然后产生氢离子阳离子和氢氧化物阴离子。溶解的盐也可以分离成阴离子或阳离子,这通常称为盐水解。
什么是水合作用(hydration)?
水合作用一词定义为化学方法,它涉及水分子与物质结合或连接。此外,向离子或物质中添加H2O分子以生成水合盐或水合离子称为水合。水合作用被认为是物理过程,因为它不涉及任何分子或键的化学分解,通常由干燥剂(一种容易吸收水的化合物)形成。
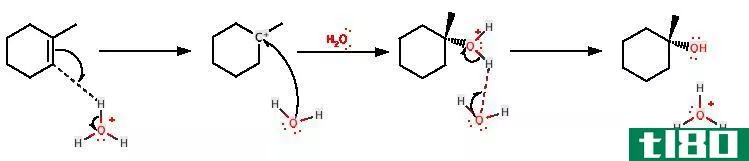
在反应过程中,水化的pH值保持不变。有机分子的水合作用通常伴随着键的断裂而发生,但在无机化合物中,有时键不会断裂,因为这是水分子与化合物的内涵。在有机化学中,水分子进入不饱和状态。在这一点上,水分子分解成一个氢氧化离子和一个质子。
氢氧化离子通常与碳原子产生键,碳原子具有更多的取代基。质子通常与碳结合,而碳的取代基数目较少,这通常能监测到马尔科夫规则。
无机化学中的水合作用通常表示水分子与无机化合物的连接。例如,在硫酸法生产过程中,通常从钛铁矿砂(FeTiO3)中生成TiO2颜料,生成的副产品是FeSO4。
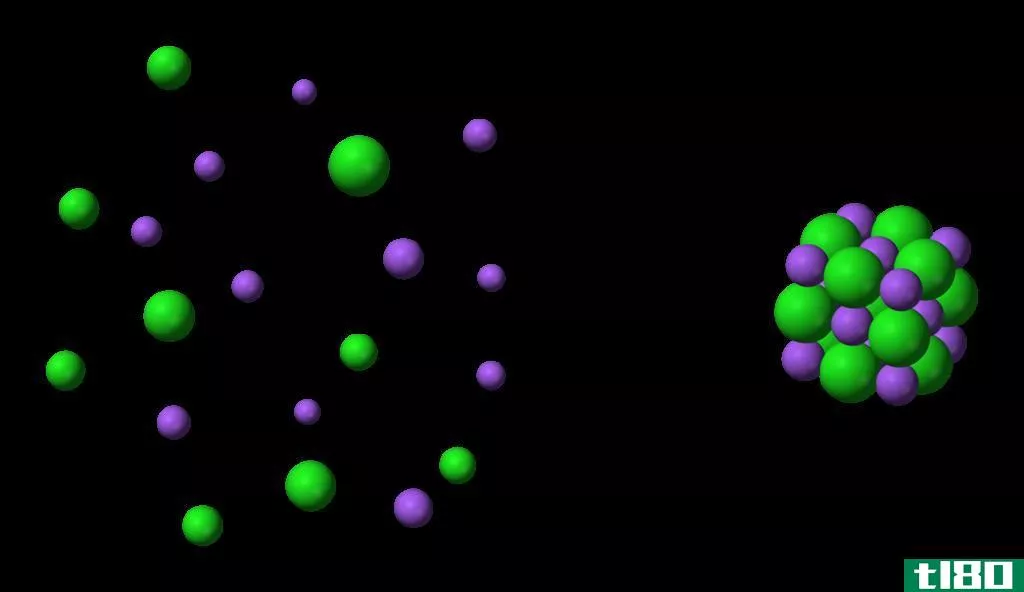
当一种盐混入水中时,通常会形成阴离子和阳离子,然后通过水分子中的离子水合作用使它们彼此分离。在这个过程中,水分子通常包围着盐离子,这就是所谓的水合作用。水化示例为K+Cl–+H2O→K+(aq)+Cl–(aq)。
主要区别
- H2O、H+离子和OH-离子的离子与阴离子和阳离子反应形成碱,酸称为水解;另一方面,向离子或物质中添加H2O分子以生成水合盐或水合离子称为水合。
- 水解考虑的是反应方法的两次分解,水通常作为反应物之一,而水合则考虑化学方法,其中包括与物质结合的水分子。
- 当水分子中的键断裂时,通常会发生水解,而水化通常发生在键中断的有机分子中,但在无机化合物中,键不发生分解。
- 从不饱和化合物,水解通常形成饱和化合物;另一方面,从脱水化合物,水合化合物形成水合。
- 阴离子、阳离子或有时两者都发生在水解过程中,以改变水的pH值;相反,在水合作用中,溶质分子与溶剂分子发生邻接。
- 因为水解涉及到键和分子的分解,所以水解考虑的是化学过程;另一方面,由于水合作用不涉及任何分子或键的化学分解,所以水合作用考虑的是物理方法。
- 在整个化学反应过程中,水解的pH值要么增加要么降低;另一方面,水合的pH值始终停留在反应过程中。
- 水解的例子被认为是Na2CO3+2H2O→2NaOH+H2CO3,而水合的例子被认为是K+Cl–+H2O→K+(aq)+Cl-(aq)。
结论
以上讨论得出结论:水解涉及水分子的分裂,在阴离子或阳离子相对改变水的pH值的化学反应过程中,水解的pH值要么增加要么降低。而水化一般并不总是涉及水分子的分裂,水化的pH值在反应过程中保持恒定。