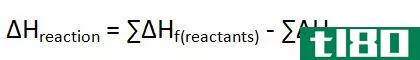潜热与比热
潜热
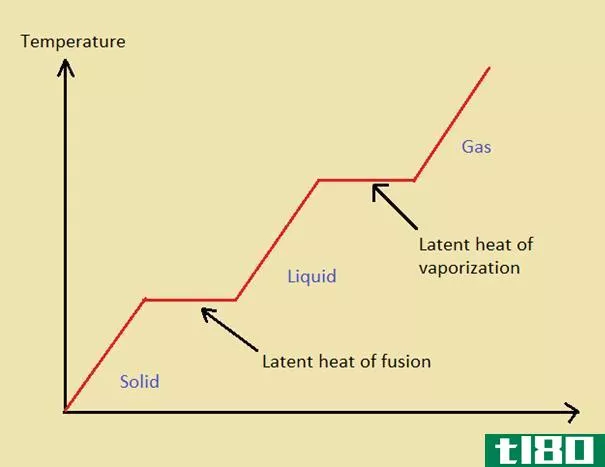
当物质发生相变时,能量以热的形式被吸收或释放。潜热是物质在相变过程中吸收或释放的热量。这种热变化在吸收或释放时不会引起温度变化。潜热的两种形式是熔化潜热和汽化潜热。熔化潜热发生在熔化或冻结过程中,汽化潜热发生在沸腾或冷凝过程中。在将气体转化为液体或液体转化为固体时,相变会释放热量(放热)。当从固体变为液体或液体变为气体时,相变吸收能量/热量(吸热)。例如,在蒸汽状态下,水分子的能量很高,并且没有分子间的引力。它们以单个水分子的形式运动。与此相比,液态水分子的能量较低。然而,如果一些水分子具有较高的动能,它们能够逃逸到蒸气状态。在常温下,水分子的汽态和液态之间会有平衡。加热时,在沸点时,大多数水分子会释放到蒸汽状态。所以,当水分子蒸发时,水分子之间的氢键必须被打破。为此,需要能量,这种能量被称为汽化潜热。对于水,这种相变发生在100摄氏度(水的沸点)。然而,当这种相变在这个温度下发生时,水分子吸收热能来破坏键合,但不会使温度升高更多。
比潜热是指将一种物质的一种相完全转变为另一种相所需的热能。
比热
热容取决于物质的量。比热或比热容是与物质量无关的热容。它可以定义为“在恒压下使一克物质的温度升高一摄氏度(或一开尔文)所需的热量。”比热的单位是Jg-1oC-1。水的比热很高,为4.186jg-1oC-1。这意味着,要使1g水的温度升高1℃,需要4.186j的热能。这个高值遇到了水在热调节中的作用。为了找到将一定质量物质的温度从t1升高到t2所需的热量,可以使用以下方程式。
q=m x s x∆t
q=所需热量
m=物质质量
∆t=t1-t2
但是,如果反应涉及相变,则上述方程不适用。例如,当水进入气相(沸点)或水结冰形成冰(在熔点)时,它不适用。这是因为,相变过程中添加或去除的热量不会改变温度。
| 潜热和比热有什么区别?•潜热是物质发生相变时吸收或释放的能量。比热是指在恒定压力下使一克物质的温度升高一摄氏度(或一开尔文)所需的热量。•当物质发生相变时,比热不适用。•比热引起温度变化,而潜热中不涉及温度变化。 |