主要区别
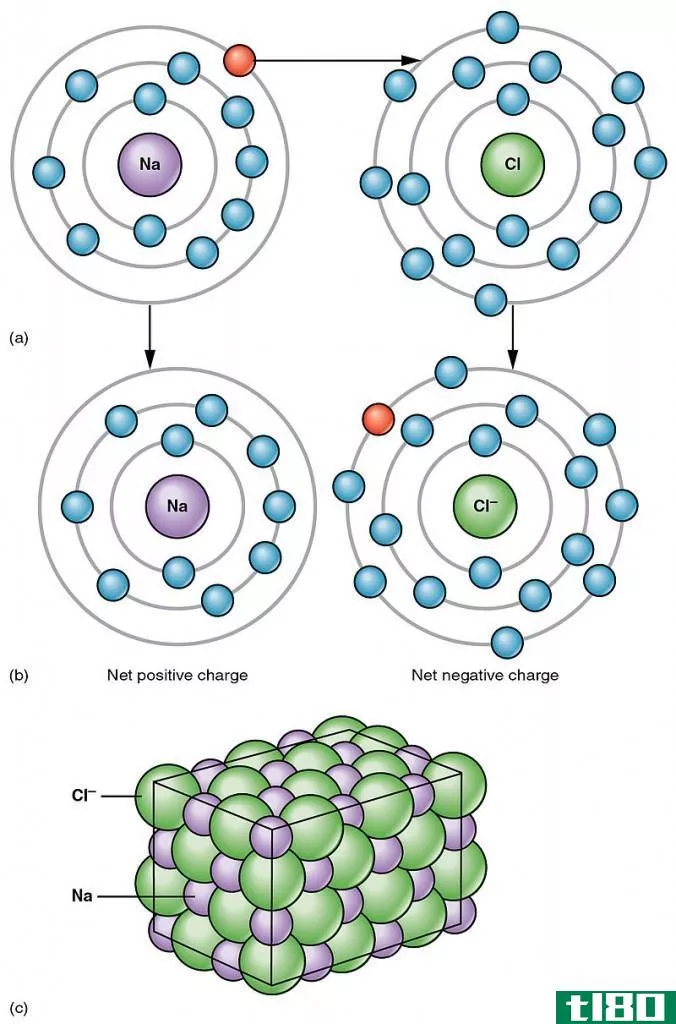
在化学领域,阳离子和阴离子是截然相反的两个术语,在区分它们之间,它们的概念与质子和电子或阴极和阳极的概念非常相似。在化学中,元素相互作用形成新的化合物,为了获得稳定性,它们失去或获得电子。原始形式的元素被称为原子,当它们失去或获得电子而变得稳定时,它们被称为原子。当失去或获得电子时,它永远不会保持中性,它有正电荷或负电荷,这取决于它是失去了一个电子,还是获得了一个电子。带正电荷的离子称为阳离子,而带负电的离子称为阴离子。当一个原子为了获得更大的稳定性而失去一个或多个电子时,它就变成了带正电的离子(阳离子),并在其上有一个正符号,表示它的施舍能力。另一方面,当一个原子获得一个或多个电子以获得更大的稳定性时,它就变成带负电的离子(负离子),并带有负号,表示它接受电子以获得稳定的能力。
比较图
什么是阳离子(cation)?
有些原子在其原始状态下是稳定的,就像惰性气体一样,但是有些为了变得更稳定而获得或失去电子,这种共享后的原子被称为离子。阳离子是一种离子,它是带正电荷的离子,它释放或释放一个或多个电子以获得稳定性。通常阳离子是由金属原子形成的,金属原子具有很高的电子迁移率,为了获得稳定性,它们从价壳层中损失一个或多个电子。原子核由电子(带负电)、质子(带正电)和中子(中性)等物质组成。在原子的初始状态下,电子和质子的数量是相等的,尽管当失去一个或多个电子而变成阳离子时,电子的数量会自动减少。所以它有更多的质子,它带正电荷,所以用正电荷来表示。在电解过程中,阴极吸引带正电荷的阳离子,而带负电荷的阴离子则远离它。
什么是负离子(anion)?
有些原子在其原始状态下是稳定的,就像惰性气体一样,但是有些为了变得更稳定而获得或失去电子,这种共享后的原子被称为离子。阴离子是一种离子,它是带负电的离子,它接受或带走一个或多个电子以获得稳定性。一般来说,阴离子是由非金属形成的,因为它们具有低电子迁移率,它们获得电子或电子以变得更稳定。当原子接受电子时,原子核中的电子数或负电荷离子数自动增加,因此由于电子数过多,这种离子具有负电荷的表示。在电解过程中,阳极吸引带负电荷的阴离子,而带正电荷的阳离子则远离它。
阳离子(cation) vs. 负离子(anion)
- 带正电荷的离子称为阳离子,而带负电的离子称为阴离子。
- 当一个原子为了获得更大的稳定性而失去一个或多个电子时,它就变成了带正电的离子(阳离子),并在其上有一个正符号,表示它的施舍能力。另一方面,当一个原子获得一个或多个电子以获得更大的稳定性时,它就变成带负电的离子(负离子),并带有负号,表示它接受电子以获得稳定的能力。
- 在电解过程中,阳极吸引带负电荷的阴离子,而阴极吸引带正电荷的阳离子。