配位共价键vs共价键
正如美国化学家G.N.Lewis所提出的,当原子在价壳中包含八个电子时,它们是稳定的。大多数原子的价壳层中的电子少于8个(周期表第18组中的惰性气体除外),因此它们不稳定。这些原子往往相互反应,变得稳定。因此,每个原子都能实现一个高贵的气体电子构型。共价键是连接化学化合物中原子的主要化学键。
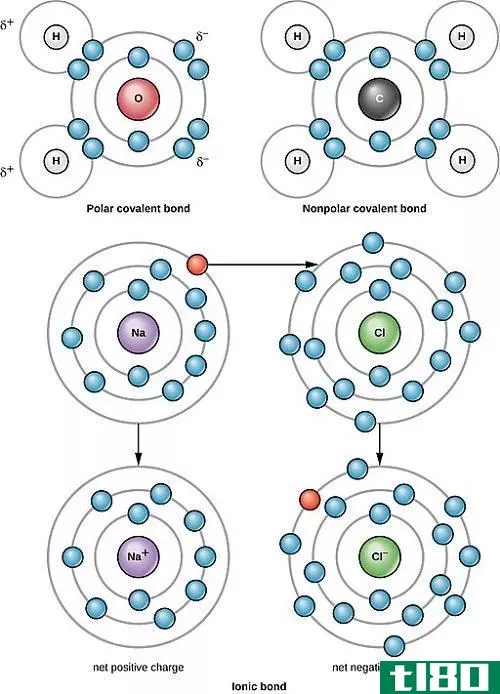
极性是由于电负性的不同而产生的。电负性是衡量原子在键中吸引电子的程度。通常用波林标度来表示电负性值。在周期表中,电负性值的变化是有规律的。从左到右经过一段时间,电负性值增加。因此,卤素在一个周期内具有较大的电负性值,而第1族元素的电负性值相对较低。在小组中,电负性值降低。当两个或两个具有相同电负性的原子在它们之间形成键时,这些原子以相似的方式拉动电子对。因此,它们倾向于共享电子,这种键被称为非极性共价键。
共价键
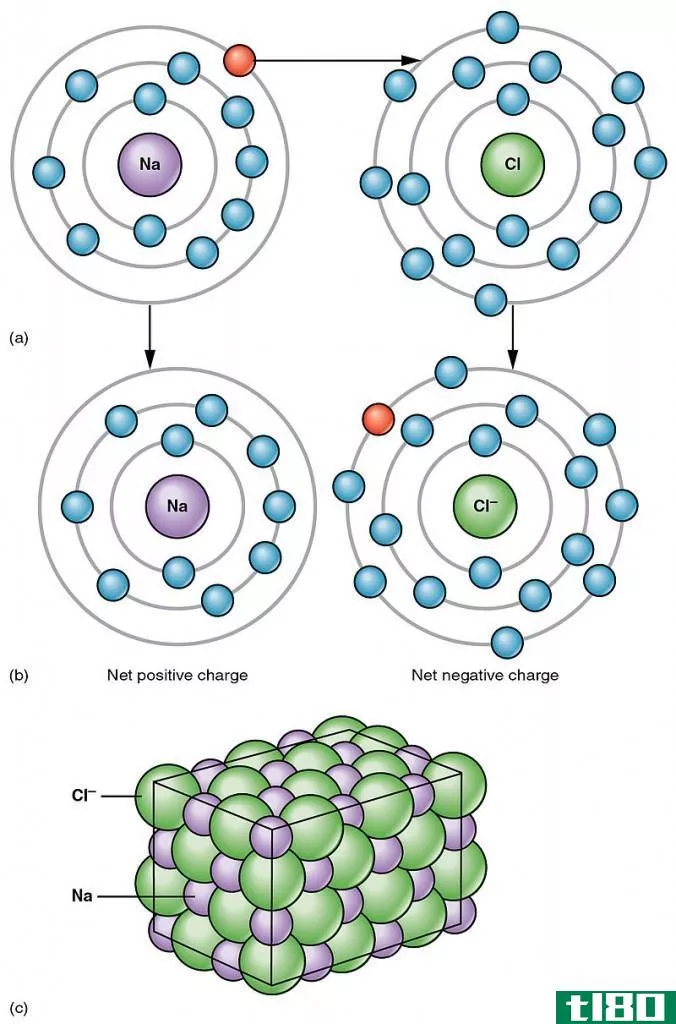
当两个具有相似或极低电负性差的原子发生反应时,它们通过共享电子形成共价键。通过这种方式,两个原子可以共享电子组态。分子是原子间共价键形成的产物。例如,当同一个原子结合形成Cl2、H2或P4等分子时,每个原子通过共价键与另一个原子结合。
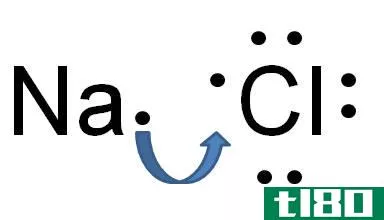
配位共价键
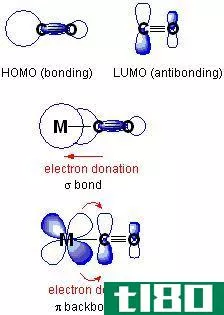
这也是一种共价键,键中的两个电子只由一个原子提供。这也被称为与格键。这种共价键是当路易斯碱向路易斯酸捐赠一对电子时形成的。因此,这也可以解释为路易斯酸和路易斯碱之间的键。从理论上讲,为了显示出施予原子和非供体原子,我们给施主原子加上正电荷,给另一个原子加上负电荷。例如,当氨将氮的孤电子对捐赠给BF3的钡时,就会产生一个配位共价键。形成后,这种键类似于极性共价键,虽然有单独的名称,但不能区分为单独的键。
| 共价键和配位共价键的区别是什么?•在共价键中,两个原子为键提供相同数量的电子,但在坐标共价键中,两个电子由一个原子提供。•在共价键中,两个原子之间的电负性差可以为零或很低,但在坐标共价键中,一种极性共价键正在形成。•为了形成配位共价键,分子中的一个原子应该有一对孤对。 |