同位素与离子
原子是所有现存物质的组成部分。不同的原子之间有变化。同样,在相同的元素中也有变化。同位素是单个元素内部差异的例子。此外,原子在自然条件下很难稳定。它们在它们之间或与其他元素形成各种组合以存在。当形成这些组合时,它们可能产生离子。
同位素
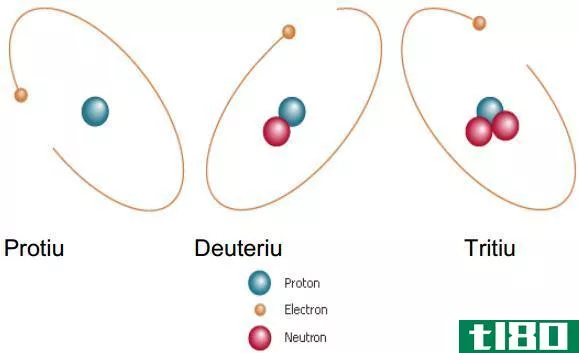
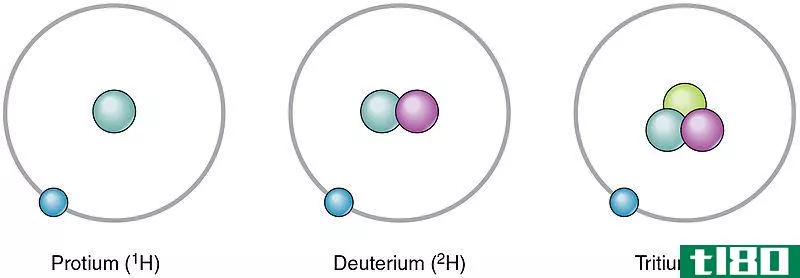
同一元素的原子可以不同。同一元素的这些不同原子称为同位素。它们因拥有不同数量的中子而彼此不同。由于中子数不同,它们的质量数也不同。然而,同一元素的同位素具有相同数量的质子和中子。不同的同位素以不同的数量存在,这是一个称为相对丰度的百分比值。例如,氢有三种同位素,如钚、氘和氚。它们的中子数和相对丰度如下。
1H–无中子,相对丰度为99.985%
相对丰度为0.015%
3H-两个中子,相对丰度为0%
一个原子核所能容纳的中子数因元素而异。在这些同位素中,只有一些是稳定的。例如,氧有三种稳定同位素,锡有十种稳定同位素。大多数情况下,简单元素的中子数和质子数相同。但是在重元素中,中子比质子多。中子数对平衡原子核的稳定性很重要。当原子核太重时,它们就会变得不稳定,因此,这些同位素就会具有放射性。例如原子核会衰变得更小。同位素由于质量不同,可能有不同的性质。例如,它们可能有不同的自旋,因此它们的核磁共振谱也不同。然而,它们的电子数是相似的,从而产生了类似的化学行为。
质谱仪可以用来获得有关同位素的信息。它给出了元素的同位素数量、相对丰度和质量。
离子
大多数原子(除了诺贝尔气体)在性质上是不稳定的,因为它们没有完全充满价壳层。因此,大多数原子试图通过获得诺贝尔气体构型来完成价壳层。原子通过三种方式实现这一点。
- 通过获得电子
- 通过提供电子
- 通过共享电子
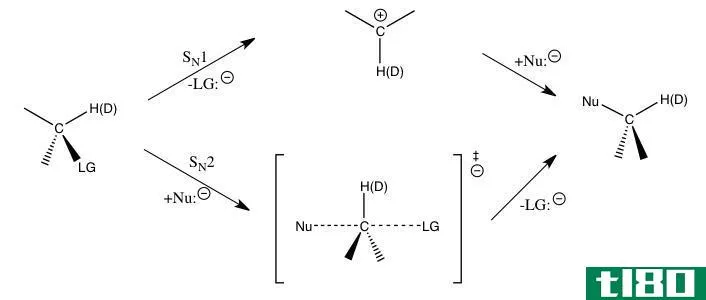
离子的产生是因为前两种方法(获得和给予电子)。通常,处于s区和d区的正电荷原子倾向于通过提供电子形成离子。通过这种方式,它们产生阳离子。大多数位于p区的负电子原子喜欢获得电子并形成负离子。通常负离子比原子大,正离子比原子小。一个或多个离子可以带电荷。例如,I族元素生成+1阳离子,II族元素生成+2阳离子。但是在d块中有一些元素可以生成+3、+4、+5等离子。由于形成离子时电子数发生变化,质子数不等于离子中的电子数。除上述多原子离子外,还可以有多原子离子和分子离子。当元素离子从分子中流失时,就会形成多原子离子(例如:ClO3-,NH4+)。
| 同位素和离子有什么区别?•同位素是同一元素的不同原子。它们的区别在于有不同数量的中子。由于电子的数量,离子与原子不同。离子可以比相应的原子拥有更多或更少的电子。•离子是带电物种,但同位素是中性的。•元素的同位素可以参与形成离子。 |