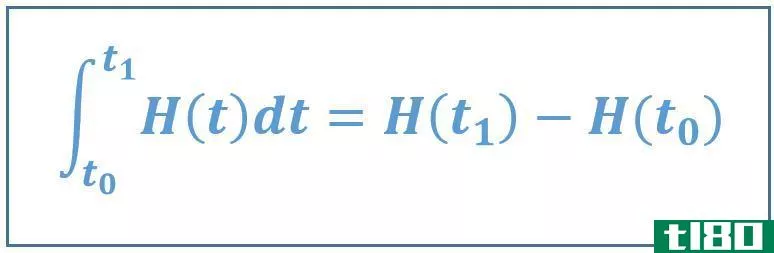内能与焓
为了化学研究的目的,我们把宇宙分成两个系统和一个环境。在任何时候,我们感兴趣的部分是系统,其余的都是围绕着系统。焓和内能是与热力学第一定律有关的两个概念,它们描述了在一个系统和周围环境中发生的反应。
什么是焓?
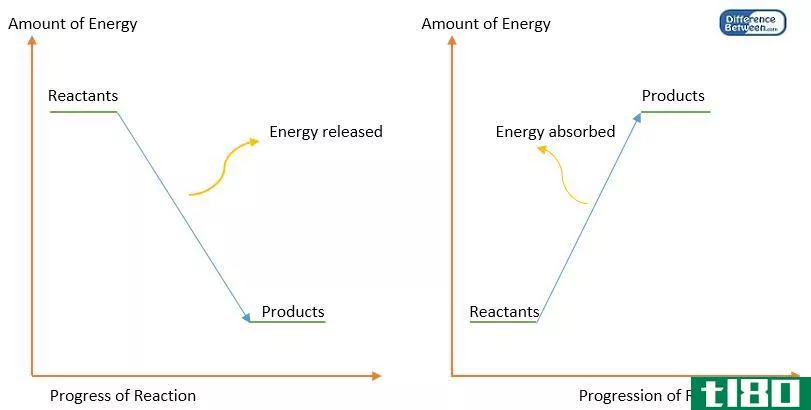
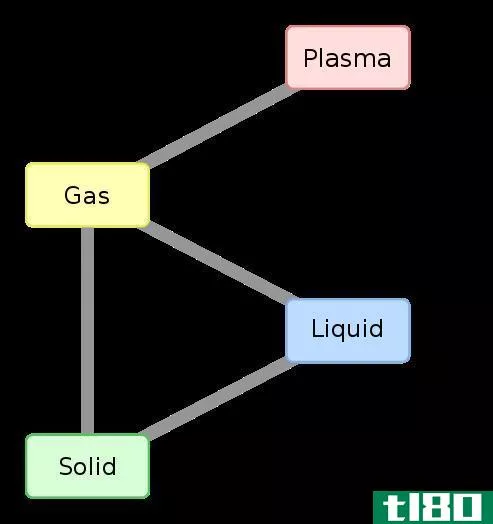
当一个反应发生时,它可能会吸收或放出热量,如果反应是在恒压下进行的,这个热量被称为反应的焓。分子的焓是无法测量的。因此,反应过程中焓的变化是测量的。在给定的温度和压力下,反应的焓变(∆H)是通过从产物的焓中减去反应物的焓得到的。如果该值为负值,则反应是放热的。如果吸热值为正值,则为吸热值。任何一对反应物和产物之间的焓变化与它们之间的路径无关。此外,焓的变化取决于反应物的相。例如,当氧气和氢气反应生成水蒸气时,焓变为-483.7kj。当相同反应物反应生成液态水时,焓变为-571.5kj。
2H2(g)+O2(g)→2H2O(g);∆H=-483.7千焦
2H2(g)+O2(g)→2H2O(l);∆H=-571.7 kJ
什么是内能?
热和功是能量传递的两种方式。在机械过程中,能量可以从一个地方转移到另一个地方,但总的能量是守恒的。在化学转化中,类似的原理也适用。考虑一个反应,比如甲烷的燃烧。
CH4+2 O2→CO2+2 H2O
如果反应发生在密封容器中,那么所发生的一切就是释放热量。我们可以用这种释放的酶来做机械工作,比如运行涡轮或蒸汽机等。有无数的方法,可以将反应产生的能量分为热和功。然而,发现热演化和机械功的总和总是一个常数。这就导致了这样一个想法:从反应物到产物,有一种叫做内能(U)的性质。内部能量的变化表示为△U。
∆U=q+w;其中q是热量,w是完成的功
内能被称为状态函数,因为它的值取决于系统的状态,而不是系统是如何进入这个状态的。也就是说,U从初始状态“i”变为“f”时,只取决于U在初始状态和最终状态下的值。
∆U=Uf–Ui
根据热力学第一定律,孤立系统的内能变化为零。宇宙是一个孤立的系统,因此,宇宙的∆U为零。
| 焓和内能的区别是什么?•焓可在以下方程式中表示,其中U是内能,p是压力,V是系统的体积。H=U+pV•因此,内能在焓项内。焓为∆U=q+w |