绝热与等温
为了化学的目的,宇宙被分为两部分。我们感兴趣的部分称为系统,其余部分称为“周围”。一个系统可以是一个有机体、一个反应容器,甚至一个细胞。系统的区别在于它们所具有的交互类型或发生的交换类型。系统可分为开放系统和封闭系统两类。有时,物质和能量可以通过系统边界交换。交换能量可以有光能、热能、声能量等多种形式,如果系统的能量因温差而改变,我们说已经有了热流。绝热和多向是两个与系统内传热有关的热力学过程。
绝热的
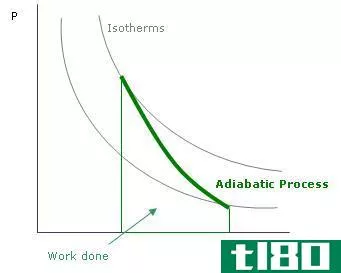
绝热变化是指没有热量进出系统的变化。停止传热主要有两种方法。一种方法是使用隔热边界,这样就不会有热量进入或存在。例如,在杜瓦瓶中进行的反应是绝热的。另一种绝热过程发生在一个过程变化很快的时候,因此,没有时间来传递热量。在热力学中,绝热变化用dQ=0表示。在这些情况下,压力和温度之间存在一种关系。因此,在绝热条件下,系统由于压力而发生变化。这就是在云形成和大尺度对流中发生的情况。在高海拔地区,大气压力较低。当空气被加热时,它会上升。因为外界空气压力低,上升的空气包会试图膨胀。当膨胀时,空气分子会工作,这会影响它们的温度。这就是温度上升时温度降低的原因。根据热力学原理,包裹体中的能量保持不变,但它可以被转换来做膨胀功,或者维持它的温度。与外界没有热交换。同样的现象也适用于空气压缩(例如活塞)。在这种情况下,当空气包被压缩时,温度升高。这些过程被称为绝热加热和冷却。
等温
等温变化是指系统保持恒定温度的变化。因此,dT=0。一个过程可以是等温的,如果它发生得很慢并且过程是可逆的。所以,变化非常缓慢,有足够的时间来调整温度变化。此外,如果一个系统可以像热沉一样,在吸收热量后保持恒定的温度,那么它就是一个等温系统。对于理想的has,在等温条件下,压力可以从下面的方程中给出。
P=nRT/V
由于功,W=PdV可导出以下方程。
W=nRT ln(Vf/Vi)
因此,在恒定温度下,膨胀或压缩功发生在改变系统体积的同时。由于在等温过程中没有内能变化(dU=0),所以所有提供的热量都用于做功。这就是在热机中发生的事情。
| 绝热和等温有什么区别?•绝热意味着系统和周围环境之间没有热交换,因此,如果是压缩,温度会升高,或者膨胀时温度会降低。•等温意味着,没有温度变化;因此,系统中的温度是恒定的。这是通过改变热量得到的。在绝热条件下,dQ=0,但dT≠0。然而,在等温变化中,dT=0且dQ≠0。•绝热变化迅速,而等温变化非常缓慢。 |