碳和石墨的主要区别在于碳是一种化学元素,而石墨是碳的同素异形体。
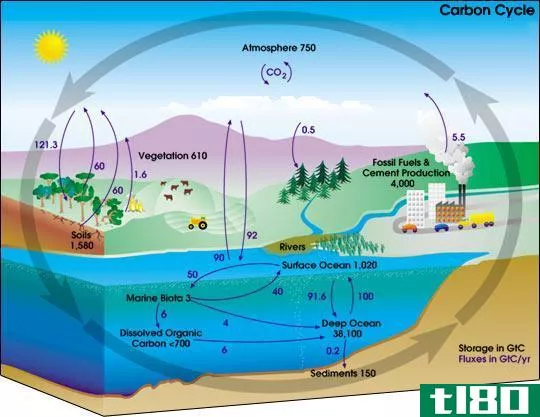
碳和石墨都是碳的形式,其中石墨是碳的同素异形体,也是碳的最稳定形式。碳是一种自古以来人们就知道的非金属。人类使用不同形式的碳,我们称之为碳同素异形体,如木炭、石墨烟尘和钻石。早些时候,人们并没有意识到这些化合物只是碳的不同形式,后来科学家才发现了碳的同素异形体。carbon一词来源于拉丁语carbo,意思是炭。碳是一种天然存在的元素,是自然界中第四种最丰富的元素。它通过碳循环在人类和植物生命中起着至关重要的作用。
目录
1. 概述和主要区别
2. 什么是碳
3. 什么是石墨
4. 并列比较-碳与石墨表格形式
5. 摘要
什么是碳(carbon)?
碳是一种原子序数为6,化学符号为C的化学元素,我们可以把它归类为非金属元素,也可以在元素周期表中是p块元素。这个元素是四价的,这意味着它有四个价电子,因此,它可以形成四个共价化学键。这种元素有三种主要的同位素,C-12和C-13是稳定的,而C-14是放射性的。

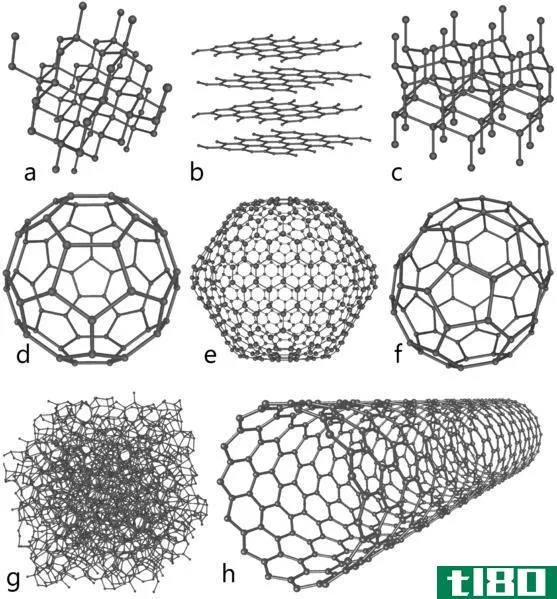
图01:石墨和金刚石是已知的最稳定的碳同素异形体
关于碳的一些化学事实如下:
- 原子序数是6。
- 标准原子量是12。
- 电子组态为[He]2s2 2p2
- 在标准温度和压力下的状态是固态。
- 在3642°C下升华
- 最稳定的同素异形体是石墨和金刚石。
- 氧化状态-最稳定的氧化状态是+4,并且+2也存在。
此外,这种物质可以在非常高的温度下升华(高于最高熔点的金属,如钨)。最重要的是,这种物质比铁和铜更耐氧化。碳是构成有机化合物结构的主要化学元素,也存在于无机化合物中。
什么是石墨(graphite)?
石墨是碳的稳定同素异形体。同素异形体是两种或两种以上不同的物理形态中的每一种可以存在的物质。这种同素异形体是自然形成的,它是一种结晶体。我们可以在变质岩和火成岩中找到这种化合物。这是一种矿物,具有某些极端的特性,对工业需要很有用。例如,它是非常柔软的,因此,它可以劈裂,只要施加一点压力。而且,它的比重很低。相反,这种物质非常耐热。它对任何其他物质的接触几乎是惰性的。

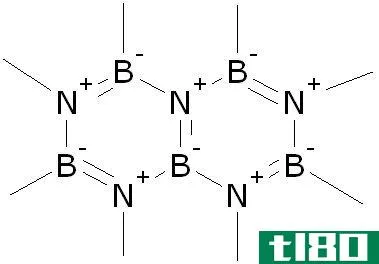
图02:石墨的化学结构
当考虑石墨的结构时,有一层碳原子层,其中一层有一个碳原子网络。在那里,一个碳原子通过共价键与另外三个碳原子相连。因此,碳层是平面的。每个碳原子的剩余电子趋向于一起形成一个电子云。这个电子云对导电性很重要。
碳(carbon)和石墨(graphite)的区别
碳是一种原子序数为6,化学符号为C的化学元素,而石墨是碳的稳定同素异形体。碳是石墨和石墨的区别。此外,碳是一种非金属,可以以不同的结构出现,我们称之为同素异形体,如石墨、金刚石、木炭等。因此,石墨的化学结构不同于其他同素异形体,这些同素异形体中每个碳原子周围有三个共价键(与其他碳原子)和能导电的电子云。其他碳的同素异形体不能导电。因此,这是碳和石墨的主要区别。
下面的信息图提供了有关碳和石墨之间区别的更多详细信息。

总结 - 碳(carbon) vs. 石墨(graphite)
碳是构成生物的主要化学元素。石墨是碳的一种天然矿物形式。然而,碳和石墨的关键区别在于碳是一种化学元素,而石墨是碳的同素异形体。
引用
1“碳”,维基百科,维基媒体基金会,2018年10月1日。这里有2个。“石墨”,地质学。此处提供
2“石墨”,地质学。