主要区别
混合物和溶液的主要区别在于混合物是两种未经化学溶解的物质的混合物,而溶液是两种溶解物质的混合物。
混合物(mixture) vs. 解决方案(solution)
在混合物中添加物质的量并没有固定的比例。在溶液中加入相同比例的物质。混合物可以是均质的,也可以是非均质的。然而,溶液总是均匀的混合物。将混合物中的物质混合后,它们的化学性质仍然相同。混合后溶液中物质的化学性质发生变化。
混合物可以以三种状态存在。溶液只有一种液态存在。成分混合在混合物中,没有化学键。成分通过化学键混合。借助于任何类型的热和机械方法,混合物很容易分离。解决方案很难用不同的方法分离。
混合物之间没有适当的分子相互作用。然而,在溶液中,一种物质的分子之间存在着适当的相互作用。在混合物中,物质的混合不受任何规范的规定。溶液的混合由特定的化学极性和浓度调节。注意到混合物中物质的熔点等物理性质受到很大影响。溶液中物质的物理性质没有剧烈变化。
混合物中的物质没有完全混合。物质在溶液中混合均匀。混合物只是混合的一种行为。溶液也是溶解的状态。这种混合物没有固定的熔点。该溶液具有特定和固定的熔点。
比较图
什么是混合物(a mixture)?
在化学的定义中,混合物是由两种或两种以上不同物质组成的物质。这些混合物质是物理结合的原因。这两种或多种元素以溶液、胶体和悬浮液的形式混合在一起。在混合物中,化合物是机械混合而不是形成化学键或任何化学变化。这意味着混合物中的所有成分都有其不变的化学性质。
混合物成分的物理性质,例如熔点,与原始成分相比会有轻微的变化。混合成分也可以通过热处理和机械加工相互分离。有些混合物像共沸混合物一样很难分离。组分不会混合在混合物中;既不会将其结合在一起,也不会产生新的物质。例如,水和沙子的混合物,这两种成分都不会被化学物质吸收,很容易通过过滤过程分离出来。
还有一些分离组分的其他方法,如蒸发、离心、蒸馏、萃取、色谱等。要进行这种分离,必须充分考虑物质的某些物理性质,如尺寸、密度和溶解度。混合物不具备它们的特性。然而,
类别
- 均质混合物:均质混合物在整个混合物中有固定的成分。例如,水中的盐。
- 非均匀混合物:混合物中不同点的非均匀混合物的组成不同。例如,我们呼吸的蓝色海洋和空气也是一种异质的混合物。
什么是解决方案(a solution)?
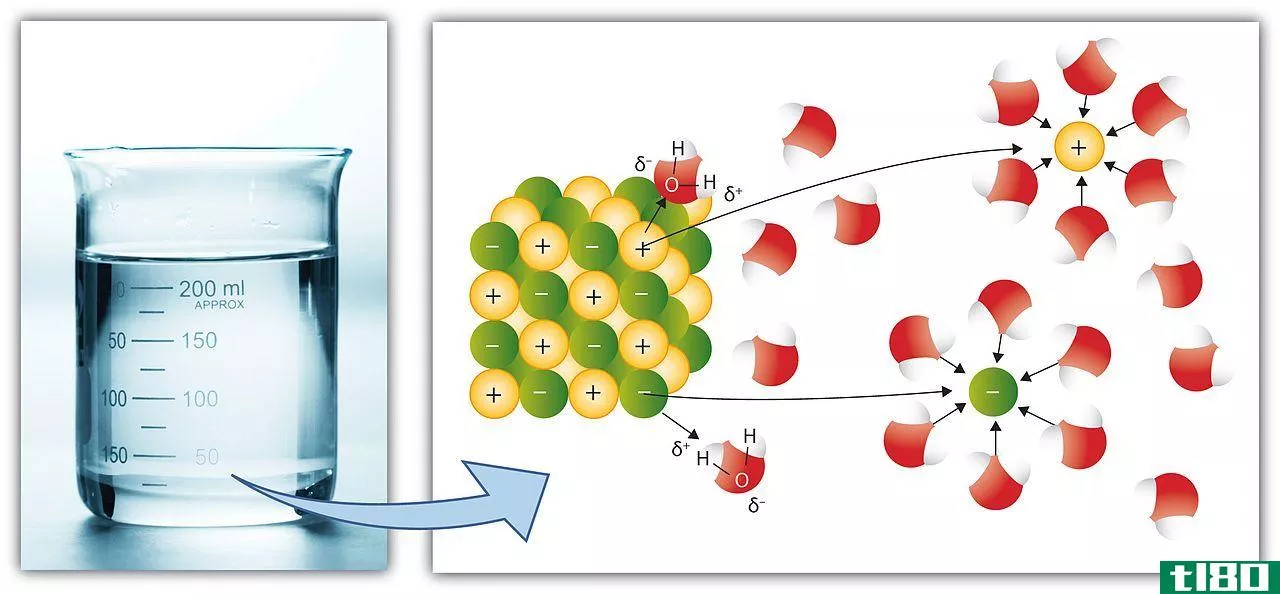
溶液是两种或两种以上同类物质的均质混合物。当一种物质是溶剂或水时,这种溶液被称为“水溶液”。在水溶液中,一种物质是溶质,另一种是溶剂,溶质溶解在溶剂中。物质在溶液中混合,由于化学极性的影响,分子间产生相互作用。如果混合物中的溶剂在很大一部分,那么在这种情况下,溶液本身就是溶剂。任何溶液中溶质的浓度总是可以用整个质量溶液的百分比来表示。
在溶液中,最重要的部分总是溶剂,它在溶液中大量存在。然而,溶质只是一种可以溶解在任何溶液中的物质。通常,溶质颗粒的大小约小于1纳米(nm)。这些溶质粒子要么在分子水平,要么在原子水平。溶质和溶剂颗粒混合在一起,形成键和其他相互作用,所以即使在显微镜下也很难区分。当溶质和溶剂轻轻均匀地分布在一起时,它们就形成了一种特殊的均匀性。
这就是为什么很难分离溶液的成分。例如,氯化钠溶解在水中是固体,它变得透明。通常情况下,溶液是透明的,因为溶质颗粒的尺寸非常小,并且它抵抗光的反射。
主要区别
- 混合物是一种或多种物质的混合物,而溶液只是一种物质的混合物。
- 混合物不是在均匀混合物中;另一方面,溶液是在均匀混合物中。
- 物质在混合物中混合;相反,在溶液中,物质完全溶解。
- 混合物的物质是固体或液体;另一方面,溶液中含有溶质和溶剂。
- 混合物可以是固体、气体或液体,而溶液总是液体。
- 混合物的成分可以分离,但溶液的成分不能分离。
- 与溶解溶液相比,混合物是物质的统一。
- 与溶液中的物质颗粒相比,物质颗粒在混合物中松散结合。
- 混合物不会影响物质的化学性质。然而,溶液改变了混合物质的化学性质。
- 在混合物中,物质粒子只是物理结合;在另一方面,在溶液中,物质粒子是化学结合的。
结论
结果表明,混合物是关于不同物质的,而溶液是关于类似物质的。