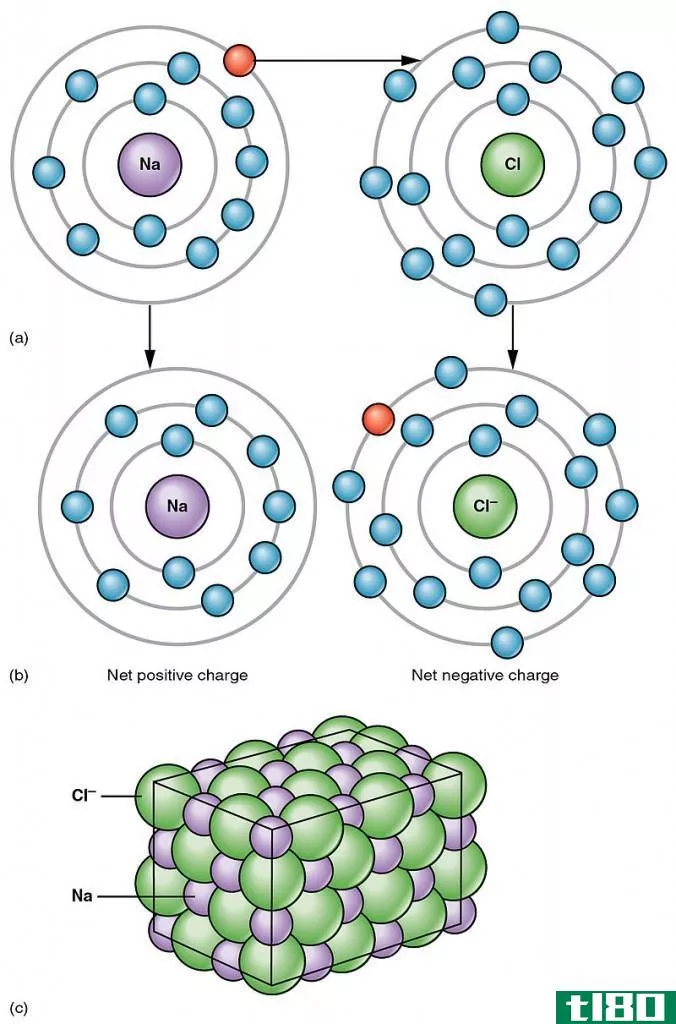
原子化焓和键离解焓之间的关键区别在于,原子化焓描述了将分子分离成原子所需的能量,而键离解焓描述了分子中化学键的离解。
有时,如果存在简单键,一些简单化合物的原子化焓和键解离焓是相同的。这是因为,在简单的化合物中,键的离解形成了构成分子的原子。
目录
1. 概述和主要区别
2. 原子化焓是多少
3. 键的解离焓是多少
4. 并列比较-原子化焓与键解离的表格形式
5. 摘要
什么是原子化焓(enthalpy of atomisation)?
原子化焓是将化学物质完全分离成原子时发生的焓变。这种化学物质可以是化学元素,也可以是化合物。我们可以用ΔHat来表示焓的变化。在原子化过程中,所有类型的化学键都被分解,而没有形成任何化学键。因此,原子化焓总是一个正值。这种焓变化的标准焓值是“标准原子化焓”。本文中考虑的标准条件为268.15 K温度和1 bar压力。
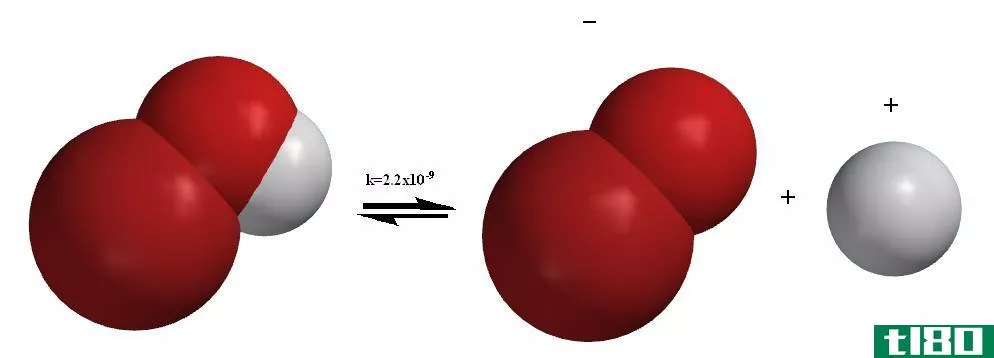
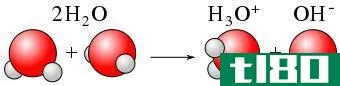
例如,水分子的原子化焓是指分离水分子中两个氢原子和氧原子所需的能量。换句话说,水的原子化焓是两个O-H键的键离解能之和。类似地,元素固体的原子化焓就是该物质的升华焓,因为升华涉及固体在蒸发时转化为单原子气体。
什么是键解离焓(enthalpy of bond dissociation)?
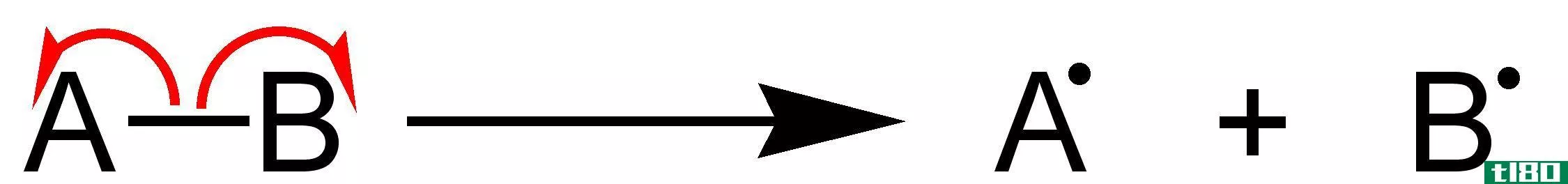
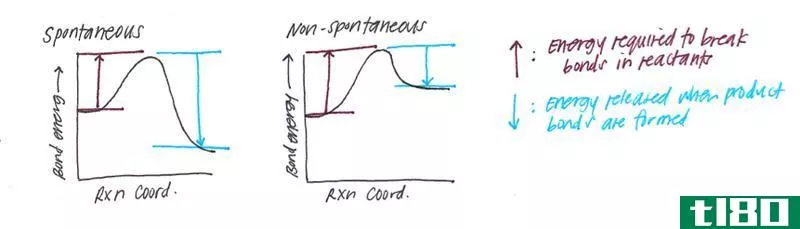
键解离焓描述化学键解离过程中发生的焓变化。换句话说,它是化学键强度的量度。因此,我们可以说,当化学键A-B被溶血分解,碎片A和B发生的标准焓变化就是键的解离焓。如果我们考虑的分子是双原子分子,那么键离解焓等于原子化焓。通常,这种键解离产生的A和B片段是自由基。我们可以用DH0来表示键的解离焓。
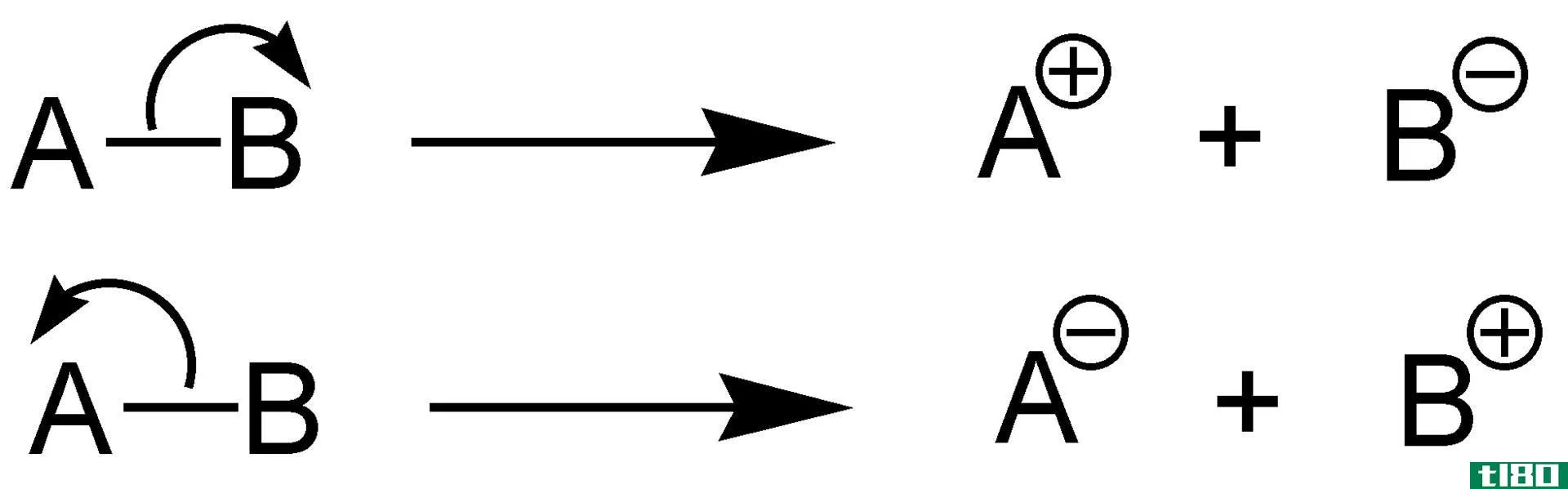
我们可以使用不同的方法来测量键的离解,如光谱法测定能级、热解或光解产生自由基、测量化学动力学和平衡、各种量热法和电化学方法等。
原子化焓(enthalpy of atomisation)和键裂解(bond dissociation)的区别
原子化焓和键离解焓之间的关键区别在于,原子化焓描述了将分子分离成原子所需的能量,而键离解焓描述了分子中化学键的离解。键解离焓和原子化焓总是正值。有时,如果存在简单键,一些简单化合物的原子化焓和键解离焓是相同的。然而,这些术语在大多数情况下是不同的。
下面的信息图表显示了原子化焓和键解离焓之间的更多差异。

总结 - 原子化焓(enthalpy of atomisation) vs. 键裂解(bond dissociation)
对于一些简单的化合物,原子化焓和键解离焓可以互换使用,但并不总是等价的。原子化焓和键离解焓之间的关键区别在于,原子化焓描述了将分子分离成原子所需的能量,而键离解焓描述了分子中化学键的离解。
引用
1“原子化焓”,维基百科,这里有。