N2O4和NO2的主要区别在于N2O4是抗磁的,而NO2是顺磁的。
N2O4是四氧化二氮,而NO2是二氧化氮。虽然化学式N2O4可通过将化学式NO2的化学计量值加倍而获得,但这两种化合物具有不同的化学和物理性质。
目录
1. 概述和主要区别
2. 什么是N2O4
3. 什么是NO2
4. 并列比较——N2O4与NO2的表格形式
5. 摘要
什么是氧化亚氮(n2o4)?
N2O4是四氧化二氮。我们通常称之为四氧化二氮。这种化合物是无色液体,是化学合成过程中非常有用的试剂。这种化合物能与二氧化氮形成平衡混合物。此外,四氧化二氮是一种强氧化剂,也是自燃的。它与各种形式的联氨接触时是自燃的(这使得联氨和四氧化二氮的混合物成为火箭常用的二元推进剂)。

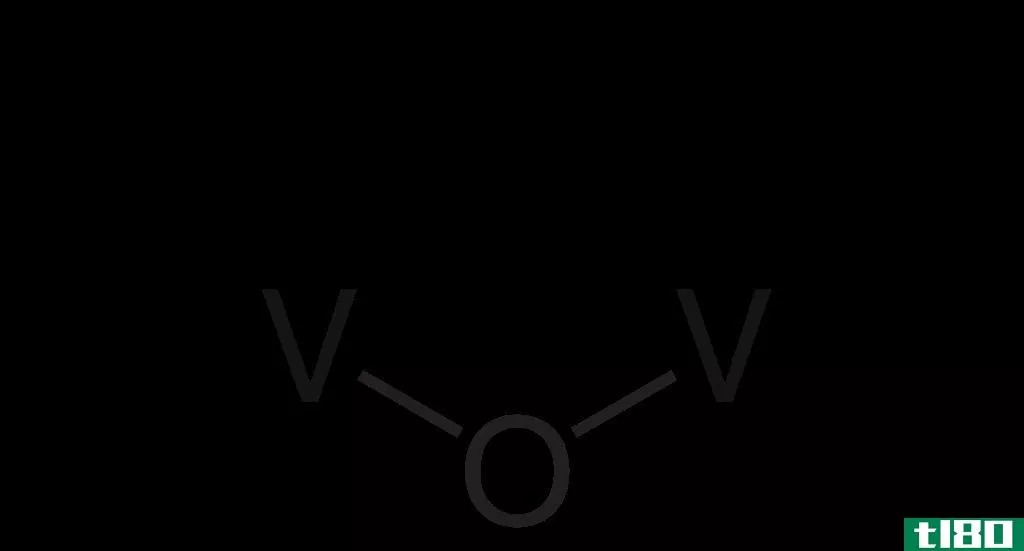
图01:四氧化二氮分子的分子堆积
我们可以把四氧化二氮分子看作是两个结合在一起的硝基。这个特殊的反应形成了四氧化二氮和二氧化氮的平衡混合物。同时,我们可以观察到四氧化二氮分子是一个平面分子,在两个氮原子之间有一个弱键。这是因为这种化学键比通常的N-N化学键长得多。
当考虑这个分子的磁性时,它是抗磁的,因为这个分子的任何原子上都没有未配对的电子。此外,这种液体物质通常是无色的,但也可能出现黄色,这是由于NO2的存在取决于上述平衡。更重要的是,在高温下,平衡向NO2而不是N2O4推进。
四氧化二氮可以通过氨的催化氧化产生,其中蒸汽用作稀释剂以降低燃烧温度。在这个反应过程中,第一步是氨氧化成一氧化氮,第二步是一氧化氮氧化成二氧化氮,然后二聚成四氧化二氮。
什么是二氧化氮(no2)?
NO2是二氧化氮。它是几种氮氧化物之一。我们可以观察到它是工业合成硝酸的中间体,硝酸在肥料生产中很重要。此外,NO2是一种棕色气体,具有类似氯的气味。当加入水中时,这种化合物会发生水解。然而,这种气态物质在低温下会转化为黄棕色液体。而且,这种颜色变化是由于NO2转化为N2O4引起的。

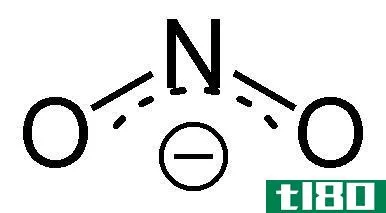
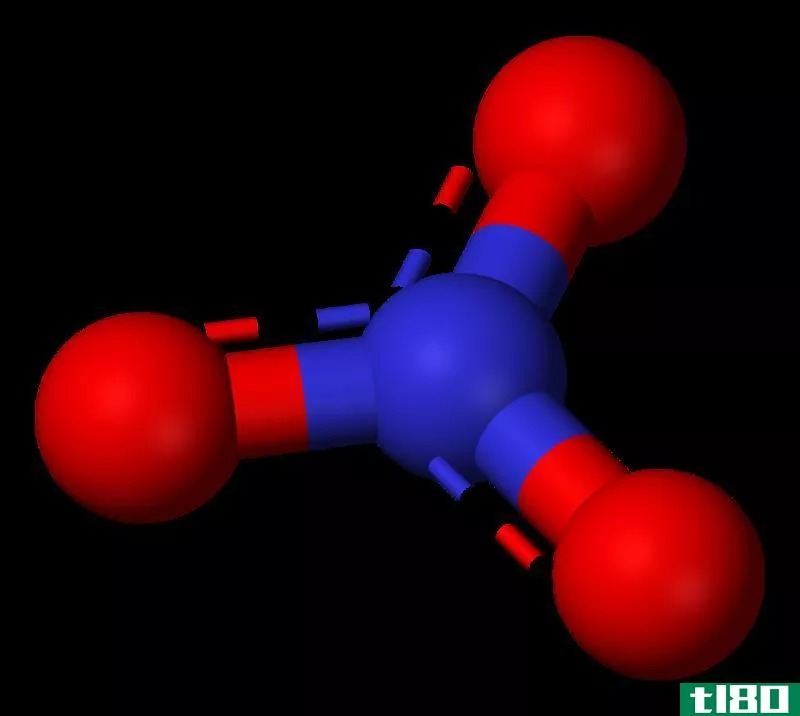
图02:NO2的化学结构
NO2分子的氮原子有一个未配对的电子,而分子中有两个N=O键。因此,这种化合物是顺磁性的,也就是说,它能被外部磁场吸引。此外,这个单一的未配对电子也意味着它是一个自由基化合物。
当考虑制备NO2物质时,它通常是通过空气中的氧气氧化一氧化氮形成的。而且,这种物质在大多数使用空气作为氧化剂的燃烧过程中形成。
二氧化氮几乎没有不同的用途,包括用作**硝酸的中间体、**化学**的硝化剂、丙烯酸酯的阻聚剂、面粉漂白剂等。
氧化亚氮(n2o4)和二氧化氮(no2)的区别
N2O4是四氧化二氮,而NO2是二氧化氮。N2O4和NO2的主要区别在于N2O4是抗磁的,而NO2是顺磁的。此外,N2O4以液体形式出现,而NO2是气态物质。此外,N2O4是无色液体,而NO2是棕色气体。
以下信息图表列出了N2O4和NO2之间的更多差异,以便进行并列比较。
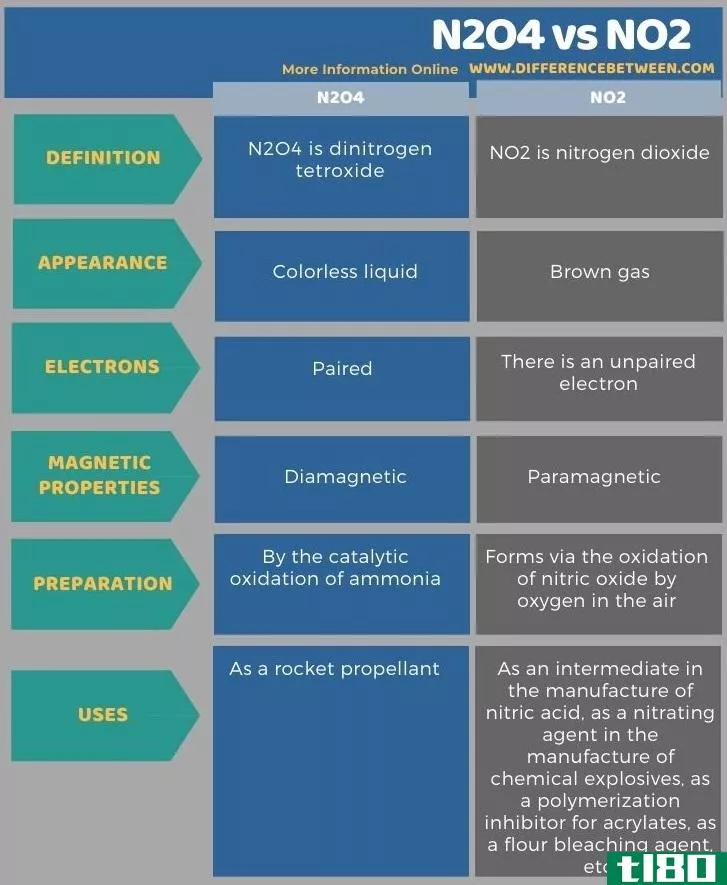
总结 - 氧化亚氮(n2o4) vs. 二氧化氮(no2)
N2O4是四氧化二氮。NO2是二氧化氮。当考虑这两种化合物的化学性质时,磁性是非常重要的。N2O4和NO2的主要区别在于N2O4是抗磁的,而NO2是顺磁的。抗磁性意味着N2O4分子不会被外部磁场吸引,因为这个分子中没有未配对的电子。顺磁性意味着分子被外部磁场吸引,因为在NO2分子中有一个未配对的电子。
引用
1“四氧化二氮”,Pubchem,可在这里买到。