电化学电池(electrochemical cell)和电解槽(electrolytic cell)的区别
电化学电池的主要区别(main difference electrochemical cell) vs. 电解槽(electrolytic cell)
电化学包括对发生化学过程的系统中电子运动的研究。这里,化学反应可以用来产生电流,或者电流可以用来促进非自发的化学反应发生。在这两种情况下,电能转化为化学能或相反的情况都会发生。发生这些转化的系统被称为电池,或者更准确地说,是电化学电池。有两种类型的电化学电池称为伏打电池和电解电池。电化学电池和电解电池的主要区别在于,电化学电池不需要外加电流,而电解电池需要外加电流。
覆盖的关键领域
1.什么是电化学电池-定义、特性、工作原理2.什么是电解电池-定义、特性、工作原理3.电化学电池和电解电池的区别是什么-主要区别的比较
Key Terms: Anode, Cathode, Electrochemical Cell, Electrolysis, Electrolytic Cell, Galvanic Cell, Oxidation, Reduction, Voltaic Cell
什么是电化学电池(an electrochemical cell)?
电化学电池是通过自发的化学反应产生电能的系统。参与这个过程的化学反应称为氧化还原反应。氧化还原反应是通过电子在化学物质之间的转移而发生的。氧化还原反应包括两个半反应:氧化反应和还原反应。氧化反应总是向系统释放电子,而还原反应则从系统中获取电子。因此,两个半反应同时发生。
电化学电池有两种类型,即电压电池和电解电池。电化学电池由两个半电池组成。半反应发生在两个半细胞中。在那个细胞中发生的化学反应引起两个半细胞之间的电位差的增加。
半电池应由电极和电解液组成。因此,一个完整的电化学电池由两个电极和两种电解质组成;有时,两个半电池可能使用相同的电解液。如果使用两种不同的电解液,则应使用盐桥以保持电解液之间的接触。这是通过使离子通过盐桥的通道来实现的。电子通过外部电路从一个半电池流到另一个半电池。这两个电极被称为阳极和阴极。
氧化和还原反应分别发生在两个电极上。阳极发生氧化反应,阴极发生还原反应。因此,电子在阳极中产生,它们通过外部电路从阳极移动到阴极。盐桥有助于保持系统中性(电),通过它转移离子,以平衡电荷。
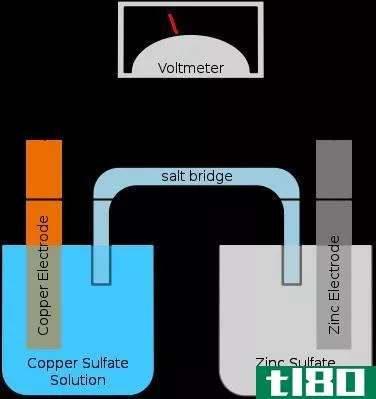
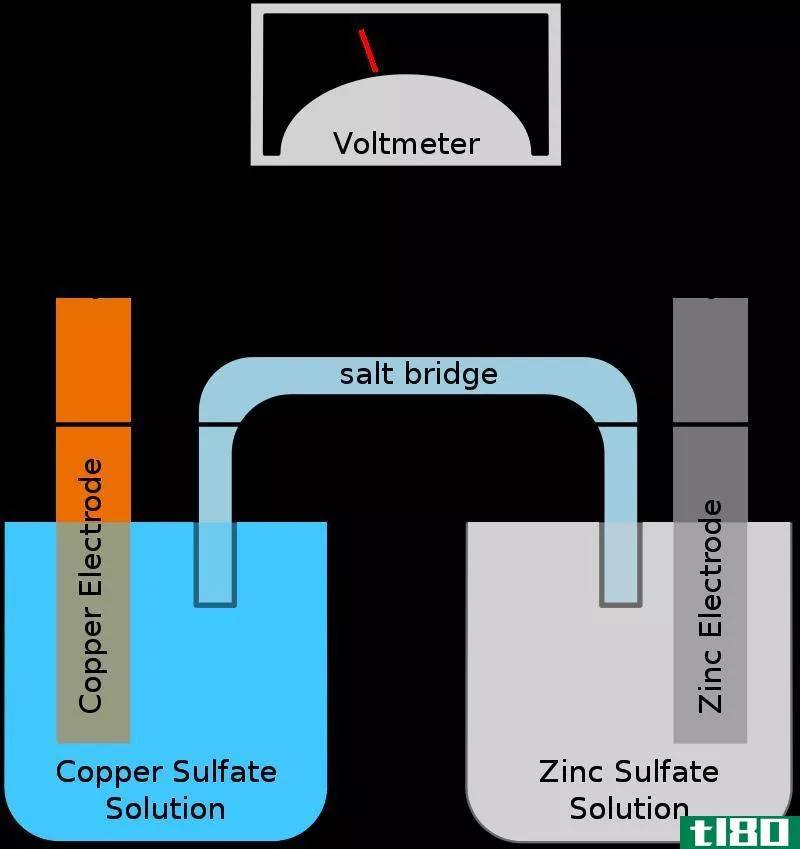
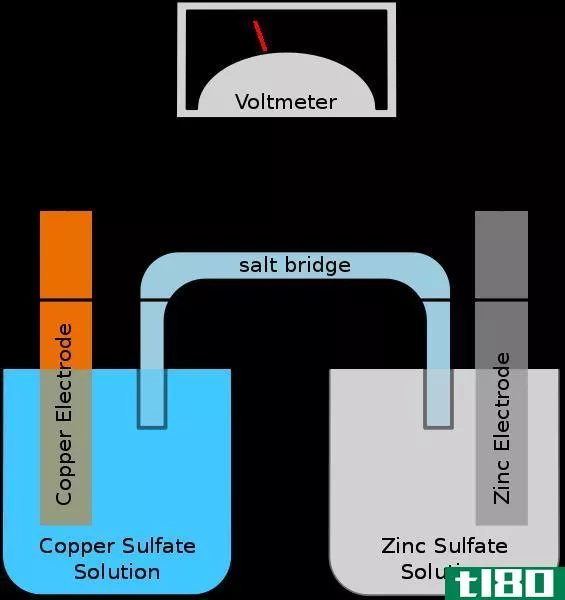
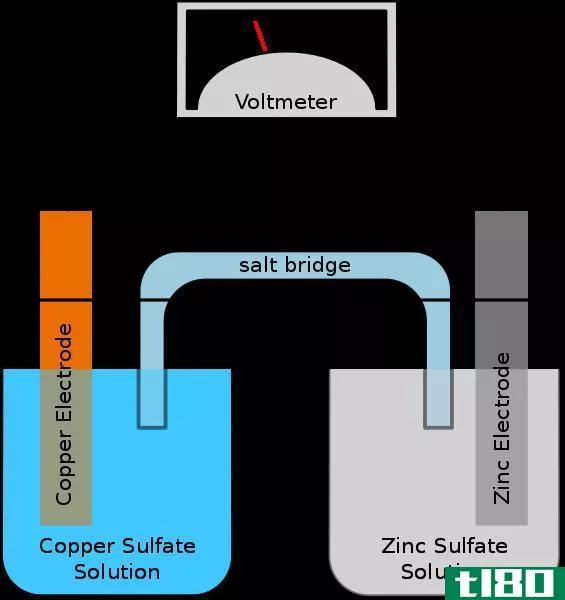
让我们考虑下面的电化学电池。

Figure 1: Electrochemical Cell
这里,阳极是锌电极,阴极是铜电极。锌电极发生氧化反应。在那里,金属锌被氧化成锌离子。释放的电子通过外部导线。产生的Zn+2离子被释放到溶液中。因此,锌电极会随着时间的推移而溶解。还原反应发生在阴极附近。阴极是铜电极。在那里,来自外部电路的电子被溶液中的Cu2+离子吸收,并被还原成Cu金属。因此,铜电极的质量会随着时间的推移而增加。通过外部导线的电子流可以测量为氧化还原反应产生的电流。这是电化学电池的典型结构。
反应
- 阳极反应(氧化)
锌(s)→ 锌+2(aq)+2e
- 阴极反应(还原)
铜+2(aq)+2e→ 铜(s)
什么是电解槽(an electrolytic cell)?
电解槽是一种电化学槽,其中电能可用于引起化学反应。换句话说,电能应该由外部电源供应。然后可以引发非自发反应。电解槽最常用于化合物的电解。
电解槽也由固体金属作为电极组成。有两个电极与外部电路相连。一个电极作为阳极,而另一个作为阴极。阳极发生氧化反应,阴极发生还原反应。
外部电能供应(来自连接到两个电极的电池)提供了通过阴极的电子流。这些电子随后进入电解溶液。然后,溶液中的阳离子**在阴极周围,获得通过阴极的电子。因此,这些阳离子在阴极被还原。阴极中的电子排斥溶液中的阴离子。这些阴离子向阳极迁移。在那里,这些阴离子释放电子并被氧化。因此,阳极带正电荷,阴极带负电荷。
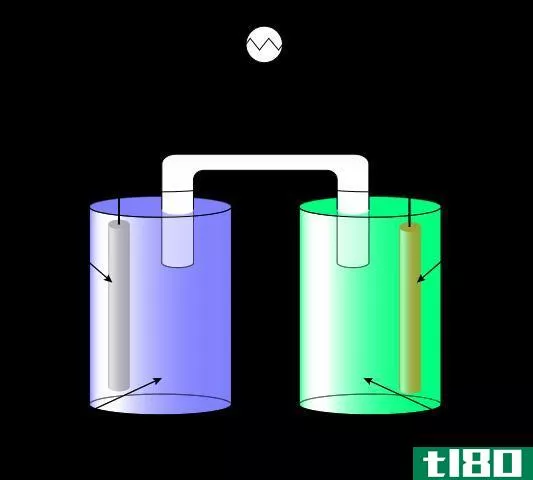
让我们考虑下面的例子。

Figure 2: The Electrolysis of Copper Chloride Solution
在上述电解槽中,电池向阴极提供电子,而Cu+2离子**在阴极周围从阴极获取电子。然后将Cu+2离子还原为Cu金属,沉积在阴极上。然后氯离子向阳极迁移,释放出多余的电子。在那里,Cl-氧化形成Cl2(g)。
反应
- 阳极反应(氧化)
2毫升-(水)→ Cl2(g)+2e
- 阴极反应(还原)
铜+2(aq)+2e→ 铜(s)
电化学电池(electrochemical cell)和电解槽(electrolytic cell)的区别
定义
电化学电池:电化学电池是通过自发的化学反应产生电能的系统。
电解槽:电解槽是一种电化学槽,电能可用于产生化学反应。
能量转换
电化学电池:在电化学电池中,化学能被转换成电能。
电解槽:在电解槽中,电能被转换成化学能。
外部电流
电化学电池:电化学电池不需要外部电源。
电解槽:电解槽需要外部电能源。
化学反应
电化学电池:在电化学电池中,发生自发的化学反应。
电解槽:在电解槽中,发生非自发的化学反应。
电极
电化学电池:在电化学电池中,阳极为负极,阴极为正。
电解槽:在电解槽中,阳极是正的,阴极是负的。
电子运动
电化学电池:电子在电化学电池中从阳极传递到阴极。
电解槽:电子从电池传递到阴极,然后电子通过电解槽中的电解液进入阳极。
结论
电解槽是一种电化学槽。因此,电解槽是由典型的电化学槽所具有的所有成分组成的。电化学电池和电解电池都涉及电子在系统中的循环。然而,在电化学电池中,会发生自发的化学反应,而在电解电池中则会发生非自发的化学反应。这就是电化学电池和电解电池的区别。
引用
1.“电化学电池”,维基百科。维基媒体基金会,2017年7月24日。这里有。2017年7月26日。 2.“电解槽”,化学剧本。Libretexts,2016年7月21日,网络。这里有。2017年7月26日。 2.“电解槽”,化学剧本。Libretexts,2016年7月21日,网络。
- 发表于 2021-06-29 09:10
- 阅读 ( 620 )
- 分类:科学
你可能感兴趣的文章
电极电位(electrode potential)和细胞电位(cell potential)的区别
...电位是指电池内电极还原或氧化的能力,而电池电位是指电化学电池中电极的电极电位之差。 电极电位和电池电位是解释电化学电池电动势的术语。电极电位给出了单个电极的电位,而电池电位则考虑了两个电极的电极电位。 ...
- 发布于 2020-10-04 17:49
- 阅读 ( 504 )
盐桥(salt bridge)和氢键(hydrogen bond)的区别
...the galvanic cell. The purpose of using a salt bridge is to facilitate the electrochemical reaction reaching the equilibrium quickly. If there is no salt bridge, then one half-cell will accumulate positive charges, and the other half cell accumulates negative charges. C***equently, the generation of...
- 发布于 2020-10-14 03:27
- 阅读 ( 1011 )
浓缩池(concentration cell)和化学电池(chemical cell)的区别
...半池的组成可能相似,也可能不相似。 浓差电池是一种电化学电池。有两种类型的电化学电池或化学电池,如原电池和电解电池。浓缩池是一种原电池。 目录 1. 概述和主要区别 2. 什么是浓缩池 3. 什么是化学细胞 4. 并列比较-...
- 发布于 2020-10-15 01:36
- 阅读 ( 568 )
原电池(galvanic cell)和浓缩池(concentration cell)的区别
...池有两个具有相同成分的半电池。 原电池和浓电池都是电化学电池。电化学电池是一种利用化学反应产生电能或利用电使化学反应发生的装置。 目录 1. 概述和主要区别 2. 什么是原电池 3. 什么是浓缩池 4. 并列比较-原电池与浓...
- 发布于 2020-10-15 20:58
- 阅读 ( 559 )
干电池(dry cell)和湿电池(wet cell)的区别
干电池和湿电池的关键区别在于,在干电池中,无论是多孔容器还是与凝胶介质混合都会限制电解液的流动,而湿电池有液体,液体可以自由移动。 一种能产生电动势并随后通过化学反应产生电流的装置称为电池。电池的集...
- 发布于 2020-10-20 08:09
- 阅读 ( 820 )
电化学电池(electrochemical cell)和原电池(galvanic cell)的区别
...电池和原电池的表格形式 5. 摘要 什么是电化学电池(an electrochemical cell)? 电化学电池是还原剂和氧化剂的组合,它们在物理上彼此分离。通常,我们用盐桥来分离。虽然它们在物理上是分开的,但两个半细胞都是相互化学接触...
- 发布于 2020-11-04 20:06
- 阅读 ( 604 )
初级的(primary)和次级细胞(secondary cells)的区别
...y)和次级细胞(secondary cells)的区别 当需要储存电力时使用电池。当需要电流时,它们积累并释放电荷。电池由一次电池或二次电池组成。主单元和辅助单元之间的关键区别是可重用性。次级细胞可以反复使用,而原细胞只能使用...
- 发布于 2020-11-09 22:27
- 阅读 ( 511 )
原电池(primary cell)和次级电池(secondary cell)的区别
电池,或称电化学电池串并联组合,是一种储能装置,至今仍在广泛使用。根据电池的使用情况,电池的基本分类是指电池的充电能力。 所以有原电池-不能充电和二次(充电)电池。 什么是原电池(primary cell)? 原电池是那...
- 发布于 2021-06-25 07:12
- 阅读 ( 457 )
原电池(galvanic cells)和电解槽(electrolytic cells)的区别
...决于金属的反应性,即其溶解倾向。 什么是电解槽(electrolytic cell)? 通过电化学电池的电流可以通过两种方式启动。第一种方法是将电极和导体连接成闭合电路。通过闭合电路,可以在金属/电解液的两相上自发地诱发电极反...
- 发布于 2021-06-25 07:57
- 阅读 ( 632 )
初级的(primary)和次级细胞(secondary cells)的区别
...ry cell) 电池是能发电的电池。一个电池可以有一个或多个电化学电池,它是由端子组成的,这些端子可以与使用电源的外部设备连接。一次电池和二次电池是两种类型的电池。初级细胞和次级细胞之间的主要区别是初级细胞只能...
- 发布于 2021-06-28 18:50
- 阅读 ( 540 )