壳次壳(shell subshell)和轨道(orbital)的区别
主要区别壳(main difference shell) vs. 子壳(subshell)
原子是构成物质的基本单位。过去,科学家们认为原子不能进一步分裂。但后来的发现揭示了有关亚原子粒子的信息,这表明原子可以进一步分为亚原子粒子。三种主要的亚原子粒子是电子、质子和中子。质子和中子共同构成原子核,原子核是原子的中心核心。电子在这个原子核周围不停地运动。我们不能确定电子的确切位置;然而,电子在某些路径中运动。壳层、次壳层和轨道是指电子运动的最可能路径。壳层-子壳层和轨道的主要区别在于壳层由共享相同主量子数的电子组成,子壳层由共享相同角动量量子数的电子组成,而轨道由处于相同能级但自旋不同的电子组成。
覆盖的关键领域
1.什么是壳-定义、结构和属性2.什么是子壳-定义、结构和属性3.什么是轨道-定义、结构和属性4.壳-子壳和轨道的区别是什么-关键区别的比较
Key Terms: Atom, Electr***, Orbital, Quantum Number, Shell, Subshell
什么是贝壳(a shell)?
壳层是电子围绕原子核的路径。这些也被称为能级,因为这些壳层是根据壳层中电子的能量排列在原子核周围的。能量最低的壳层离原子核最近。下一个能级位于那个壳层之外。
为了识别这些壳层,将它们命名为K、L、M、N等,最低能级的壳层是K壳层。但是,科学家们用量子数给这些贝壳命名。每个壳层都有自己的量子数。给出的壳层量子数称为主量子数。那么最低能级的壳层是n=1。
并非所有的壳层都含有相同数量的电子。最低能级最多只能容纳2个电子。下一个能级最多可以容纳8个电子。一个壳层所能容纳的电子数是有规律的。下面给出了这种模式。
| 主量子数(n) | 最大电子数 |
| n=1 | 2 |
| n=2个 | 8 |
| n=3个 | 18 |
| n=4 | 32 |
| n=5个 | 32 |
| n=6个 | 32 |
因此,任何壳层所能容纳的电子的最大数目是32个。任何壳层的电子数都不能超过32个。高壳层比低壳层能容纳更多的电子。
这些壳层的存在表明原子的能量是量子化的。换句话说,在原子核周围运动的电子有离散的能量值。

Figure 1: Atomic Shells
这些壳层中的电子可以通过吸收或释放能量从一个壳层转移到另一个壳层。被吸收或释放的能量应该等于两个壳之间的能量差。否则,这种转变就不会发生。
什么是一个亚层(a subshell)?
次壳层是电子在壳层中运动的区域。它们是根据角动量量子数命名的。在一个shell中可以找到4种主要的子shell类型。它们被命名为s,p,d,f。每个子壳层由几个轨道组成。下面给出了子壳层中的轨道数。
| 子壳 | 轨道数 | 最大电子数 |
| s | 1 | 2 |
| p | 三 | 6 |
| d | 5 | 10 |
| f | 7 | 14 |
这些子壳层也是根据它们所组成的能量来排列的。在下壳层,次壳层能量的升序为s<p<d<f。但在更高的炮弹,这个顺序将是不同的。

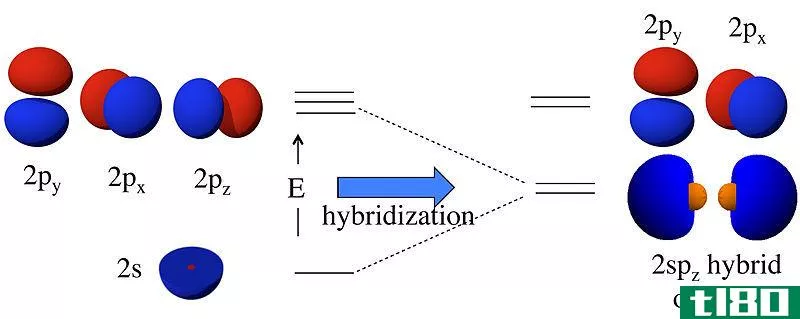
Figure 02: Shapes of Subshells
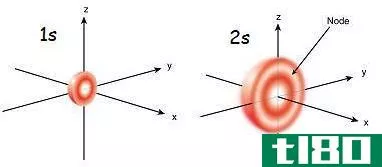
这些子壳具有独特的三维结构。s子壳是球形的。潜壳是哑铃形的。以上给出了这些形状。
什么是轨道(an orbital)?
轨道是描述电子类波行为的数学函数。换句话说,轨道这个术语解释了电子的精确运动。子地狱由轨道组成。子地狱所拥有的轨道数取决于子地狱。这意味着子地狱中存在的轨道数是子地狱的一个独特特性。
| 子壳 | 轨道数 |
| s | 1 |
| p | 三 |
| d | 5 |
| f | 10 |
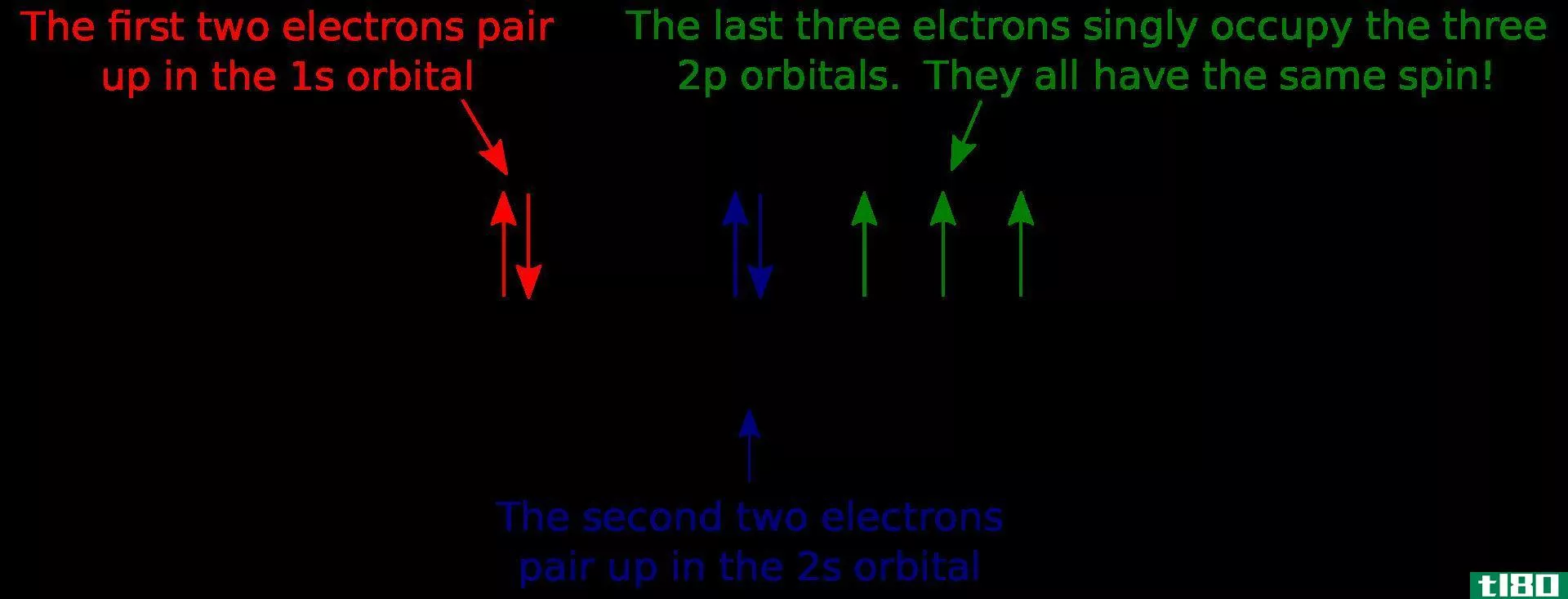
然而,一个轨道最多只能容纳两个电子。这些电子处于相同的能级,但根据它们的自旋不同。他们总是有相反的旋转。当电子被填充到轨道中时,它们是按照洪德定律被填充的。这个规律表明,在任何轨道被双耦合之前,子壳层中的每个轨道都被电子单独占据。

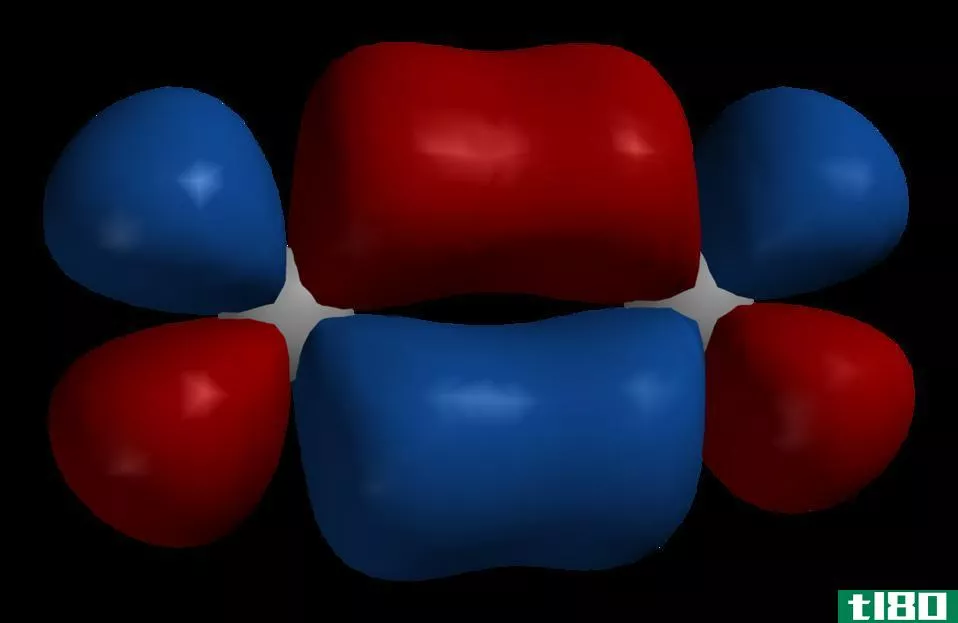
Figure 3: Shapes of d Orbitals
上图显示了d轨道的形状。由于一个d子壳层由5个轨道组成,上图显示了这些轨道的5种不同形状。
壳次壳(shell subshell)和轨道(orbital)的区别
定义
壳层:壳层是原子核周围电子的路径。
子壳层:子壳层是电子在壳层中运动的路径。
轨道:轨道是一个数学函数,它描述了电子的类波行为。
量子数的名称
壳层:壳层被赋予主量子数。
子壳层:子壳层被赋予角动量量子数。
轨道:一个轨道被赋予磁量子数。
最大电子数
壳层:一个壳层最多能容纳32个电子。
子壳层:子壳层能容纳的最大电子数取决于子壳层的类型。
轨道:一个轨道能容纳的最大电子数是2。
结论
原子由电子、质子和中子组成。质子和中子在原子核中。电子在原子核周围形成一团云。这个电子云有不断运动的电子。进一步的发现发现,这不仅仅是一片云。电子在量子化能级中运动。它们看起来像电子运动的路径。用壳层、子壳层和轨道来描述这些路径。壳层-子壳层和轨道的主要区别在于壳层由共享相同主量子数的电子组成,子壳层由共享相同角动量量子数的电子组成,而轨道由处于相同能级但自旋不同的电子组成。
引用
1.安德鲁·雷德。”化学基础,这里提供。查阅日期:2017年8月25日。2.“GCSE Bitesize:原子的结构”,BBC,BBC,可在此处查阅。查阅日期:2017年8月25日。 2.《普通中等教育证书:原子的结构》,英国广播公司,英国广播公司,
- 发表于 2021-06-29 12:03
- 阅读 ( 1294 )
- 分类:科学
你可能感兴趣的文章
轨道图(orbital diagram)和电子组态(electron configuration)的区别
轨道图和电子构型的关键区别在于,轨道图用箭头表示电子,表示电子的自旋。但是,电子组态没有显示电子自旋的细节。 轨道图显示了由电子组态给出的电子排列。电子组态给出了电子在整个原子轨道上分布的细节。但是...
- 发布于 2020-10-14 00:32
- 阅读 ( 768 )
px py公司(px py)和pz轨道(pz orbitals)的区别
Px-Py和Pz轨道的关键区别在于Px轨道有两个沿x轴方向的波瓣,Py轨道有两个沿y轴方向的波瓣,而Pz轨道有两个沿z轴方向的波瓣。因此,Px-Py和Pz轨道之间的差异源于它们在空间中的取向。 An atomic orbital is a region around an atomic nucleu...
- 发布于 2020-10-14 02:27
- 阅读 ( 983 )
分子轨道理论(molecular orbital theory)和杂交理论(hybridization theory)的区别
分子轨道理论和杂化理论的主要区别在于分子轨道理论描述了成键轨道和反键轨道的形成,而杂交理论描述了杂化轨道的形成。 有不同的理论发展来确定分子的电子结构和轨道结构。VSEPR理论、Lewis理论、价键理论、杂化理论...
- 发布于 2020-10-15 22:50
- 阅读 ( 869 )
混合的(hybrid)和简并轨道(degenerate orbitals)的区别
混合轨道和退化轨道的关键区别在于,混合轨道是两个或多个轨道混合形成的新轨道,而退化轨道最初存在于原子中。 正如它的名字所暗示的,混合轨道是两个或更多轨道的混合。虽然简并轨道的名称看起来是一样的,但它...
- 发布于 2020-10-16 17:47
- 阅读 ( 928 )
纯净的(pure)和杂化轨道(hybrid orbitals)的区别
纯轨道和杂化轨道的关键区别在于,纯轨道是原始原子轨道,而杂化轨道是由两个或多个原子轨道混合而成。 在简单分子的化学键形成过程中,我们可以简单地考虑原子轨道的重叠。但是如果我们要讨论复杂分子中的化学键...
- 发布于 2020-10-17 13:43
- 阅读 ( 603 )
轨道(orbit)和轨道(orbital)的区别
轨道与轨道的关键区别在于,轨道是一条围绕中心点有固定路径的环形路径,而轨道是围绕原子核的不确定区域。 虽然术语“轨道”和“轨道”听起来相似,但这是两个不同的术语。轨道一词主要与行星有关,而轨道一词则...
- 发布于 2020-10-23 03:43
- 阅读 ( 486 )
分子轨道(molecular orbital)和原子轨道(atomic orbital)的区别
分子轨道和原子轨道的关键区别在于,原子轨道描述的是原子中找到电子的概率很高的位置,而分子轨道描述的是分子中电子的可能位置。 利用薛定谔、海森堡和保罗·狄拉克提出的新理论,人们以一种新的方式来理解分子...
- 发布于 2020-10-24 07:58
- 阅读 ( 594 )
1秒(1s)和2s轨道(2s orbital)的区别
1秒(1s)和2s轨道(2s orbital)的区别 原子是物质的最小单位。换句话说,所有物质都是由原子构成的。原子由亚原子粒子组成,主要是质子、电子和中子。质子和电子使原子核位于原子中心。但是电子被定位在位于原子核外的轨道...
- 发布于 2020-10-25 04:49
- 阅读 ( 616 )
结合(bonding)和反键分子轨道(antibonding molecular orbitals)的区别
成键与反键分子轨道 这两种分子轨道间的化学键可以用化学键和分子轨道键的不同来解释。键和反键分子轨道之间最显著的区别是它们相对于母原子轨道的能级。这种能级差异导致了两个分子轨道之间的其他差异。 成键和反...
- 发布于 2020-10-26 19:13
- 阅读 ( 678 )
分子轨道理论(molecular orbital theory)和价键理论(valence bond theory)的区别
分子轨道理论和价键理论的主要区别在于,分子轨道理论描述的是分子轨道的形成,而价键理论描述的是原子轨道的形成。 不同的分子具有不同的化学和物理性质,不同的原子连接起来形成这些分子。为了了解原子和分子性...
- 发布于 2020-11-03 20:05
- 阅读 ( 499 )