主要区别
价和共价的主要区别在于,价是原子最外层的电子数,而共价是原子能共享的电子对的数目。
价(valency) vs. 共价(covalency)
价态被认为是原子获得或失去稳定的电子数,共价性是原子利用自由轨道产生的最高共价键。价态可以等于价壳层中存在的电子数,反之亦然,而共价性仅由价壳中存在的电子数决定。
价态通常提供完成所有自由轨道所需的电子数;另一方面,共价性由原子中存在的自由电子数决定。对于可以形成共价键或离子键的元素,可以设置其价态;相反,共价只能存在于能够在它们之间形成共价键的元素。
价可以是正值,也可以是负值;相反,共价通常都是正值。硫在SF6中的价态是2;在SF6中硫的共价性是6。
比较图
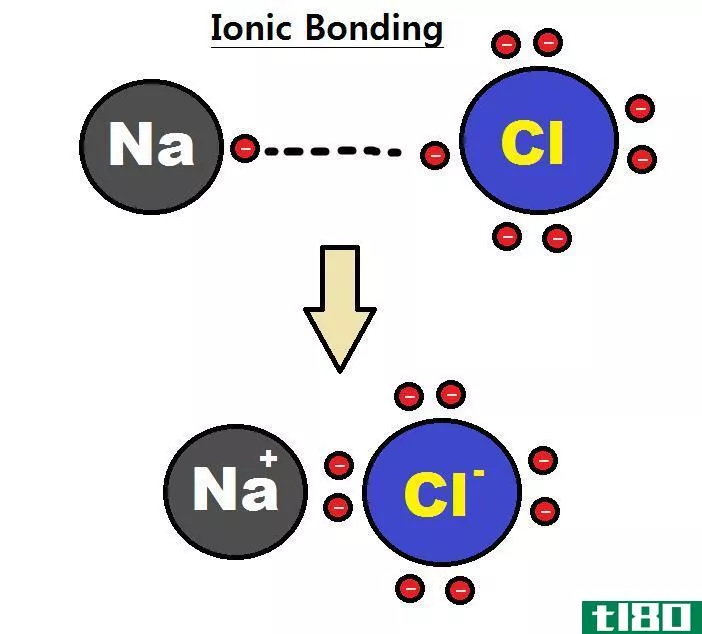
什么是价(valency)?
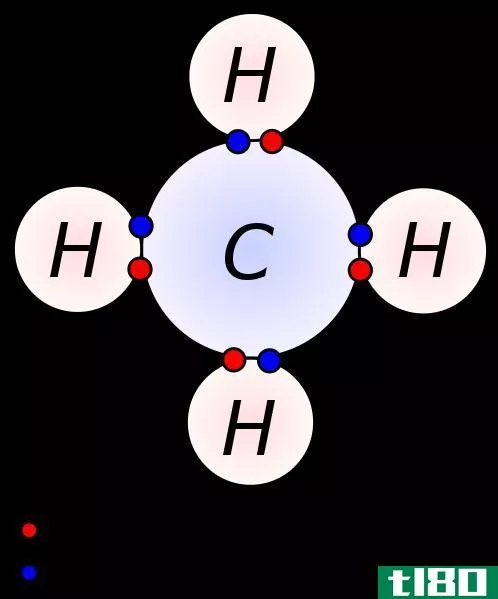
价是指原子为了完成八重态壳层而损失或获得的电子数。原子最外层的电子是价电子。所以,原子价壳层中的电子数被认为是某个原子的价。例如,考虑氢原子H,它的价态是一个可以从另一个原子失去或共享更多电子的原子,从而变得稳定。
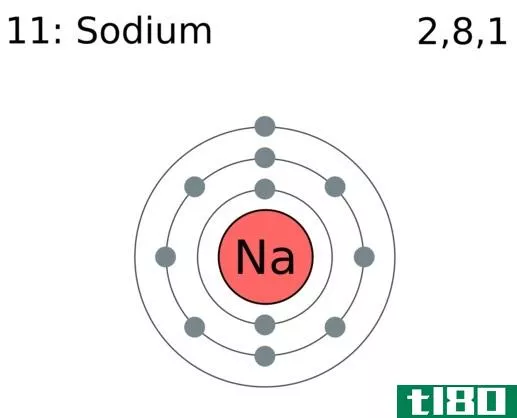
氯的价态是1,它的最外层有7个电子,但氯原子从另一个元素中多获得一个电子,以获得惰性气体的性质,并变得更加稳定,因为氯原子很容易从另一个元素获得一个电子,而不是失去它的电子。电子组态法还可以观察到特定原子或元素的价态。
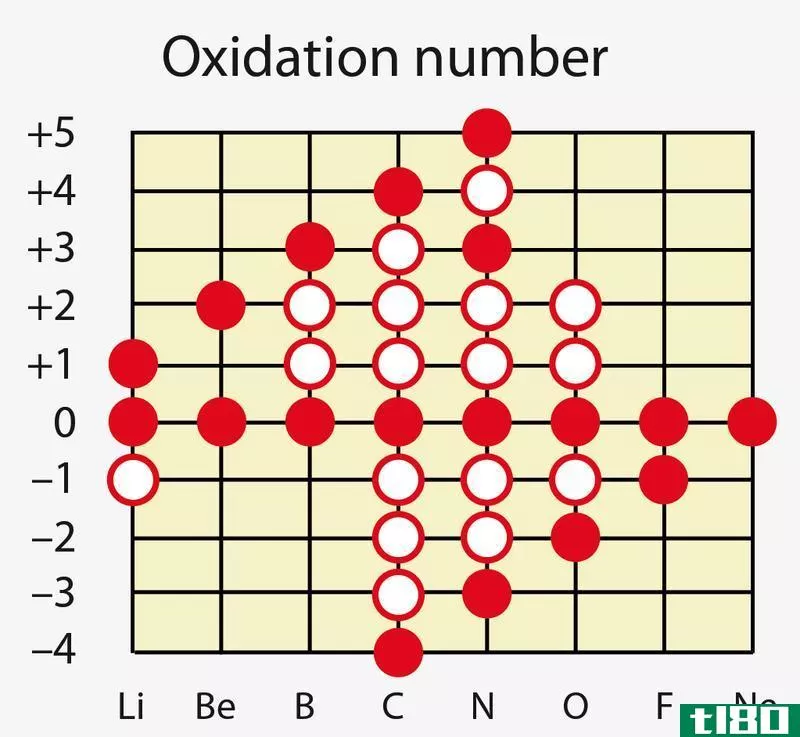
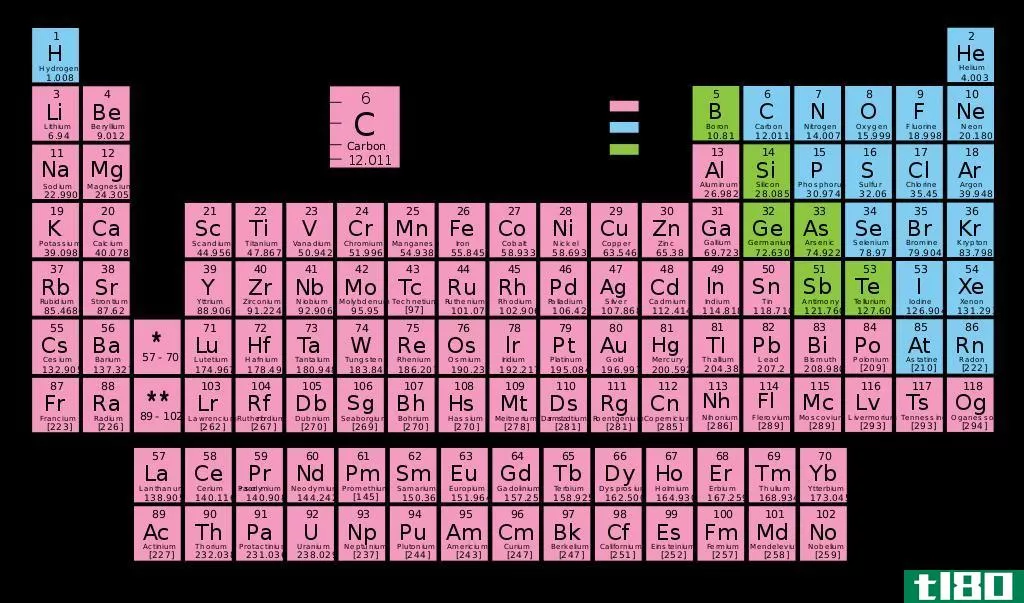
价可以是正值也可以是负值,这意味着原子上的正号表示原子将获得电子以使其稳定,而原子上的负号表示原子将移除其电子以变得稳定。化学中的周期表也表示原子的价态。硫在SF6中的价态为2;在H1中的价为1,以此类推。
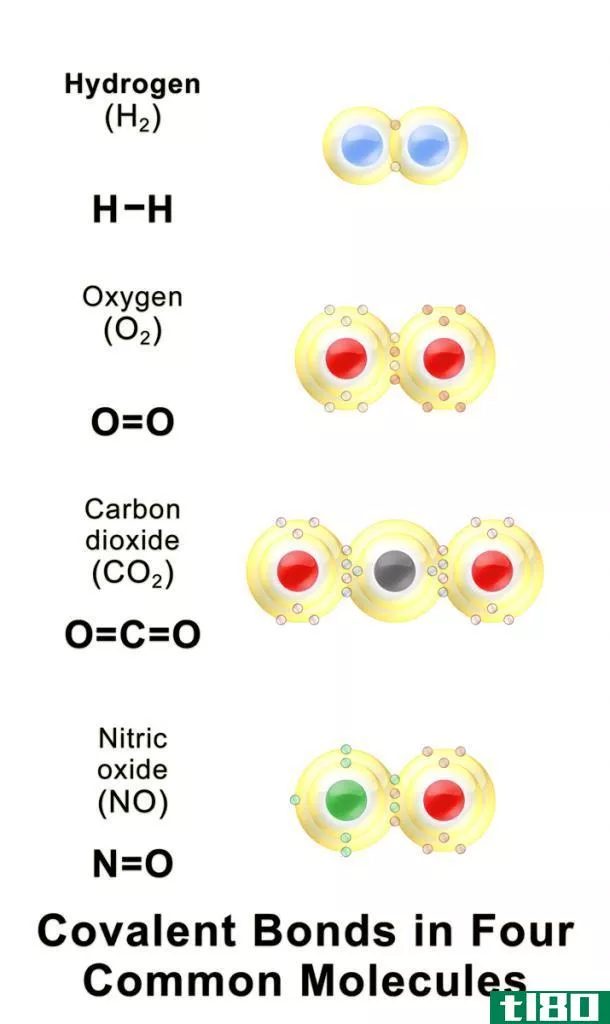
什么是共价性(covalency)?
共价一词的定义是这样的:它是原子利用其自由轨道所能产生的最高数量的共价键。原子最外层的价电子数是共价依赖性的原因。例如,氢的价壳层中的电子数为1,它的共价性也被认为是与其他原子共享形成共价键的电子。
共价性通常为正值。由于原子的共价能力有限是导致共价键饱和的主要原因。因此,一个元素的共价性是由价壳层中存在的促进共价键发展的电子总数来描述的。
在确定共价性时,不仅价壳层中存在的电子数,而且原子的自由轨道数也是必不可少的。共价的类型有恒定共价和可变共价。硫在SF6**价性的例子是6。
主要区别
- 价态是原子获得或失去以稳定的电子的性质,而共价是原子与其自由轨道共享电子而产生的最高共价键量。
- 价态可以等于价壳层中的电子数,反之亦然,而共价性只由价壳层中的电子数决定。
- 价态通常提供完成所有自由轨道所需的全部电子量;另一方面,共价性由原子中存在的自由电子数决定。
- 价是指那些可以形成共价键或离子键的元素;相反,共价只能存在于能在它们之间形成共价键的元素中。
- 价可以是正值,也可以是负值;相反,共价通常都是正值。
- 在SF6中,硫的价态是2;在SF6中,硫的共价性是6。
结论
上述讨论的结论是,价是原子最外层的电子数,获得或失去电子以使其稳定,而共价是原子能共享以形成共价键的结合电子数。