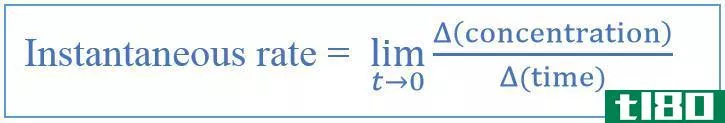主要区别
反应速率与速率常数的主要区别是反应速率指反应物和产物摩尔浓度随时间的变化而每秒摩尔数,而速率常数指特定化学反应的比例常数。
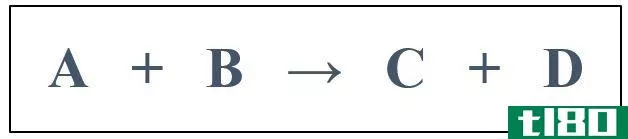
反应速率(rate of reaction) vs. 速率常数(rate c***tant)
反应速率定义为反应物和产物的数量随时间的变化,而速率常数定义为特定化学反应的比例常数。反应速率直接取决于反应物和产物的摩尔浓度,而速率常数不取决于反应物和产物的摩尔浓度。另一方面,和温度一样,反应速率也直接取决于物理性质。
反应速率主要需要反应完成的时间,速率常数不需要反应完成的时间。反应速率取决于压力,而速率常数不取决于压力。在催化剂的作用下,反应速率可以发生变化,而反应速率常数在催化剂的存在下没有任何变化。
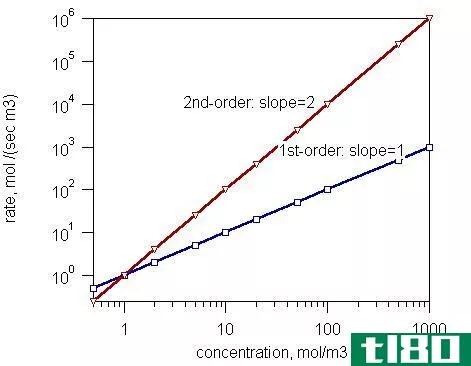
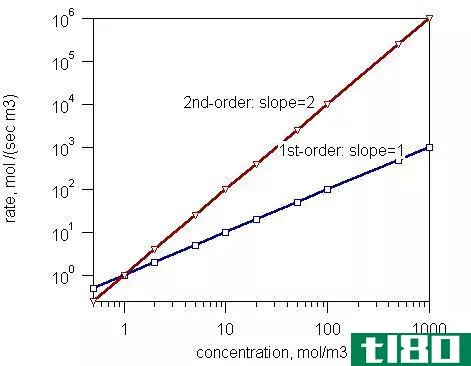
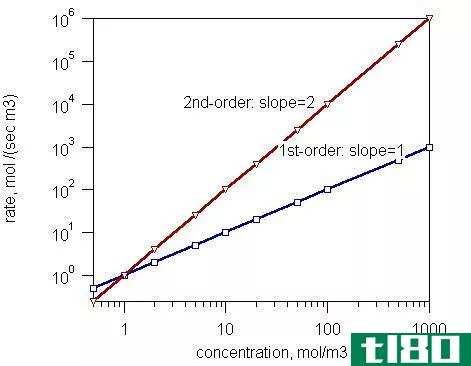
反应速率总是用摩尔每秒表示,而速率常数则直接取自反应。反应速率的单位不受反应级数的限制,而恒速单位受反应级数的限制,或借助反应的一个阶数可以求出。反应速率直接或间接地取决于碰撞的频率,而速率常数并不主要取决于碰撞频率。
比较图
什么是反应速率(the rate of reaction)?
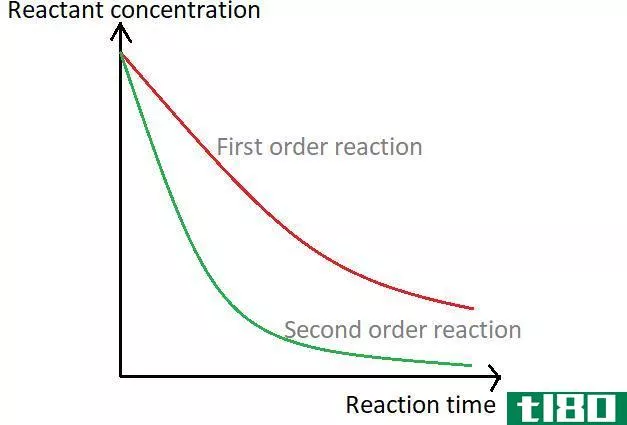
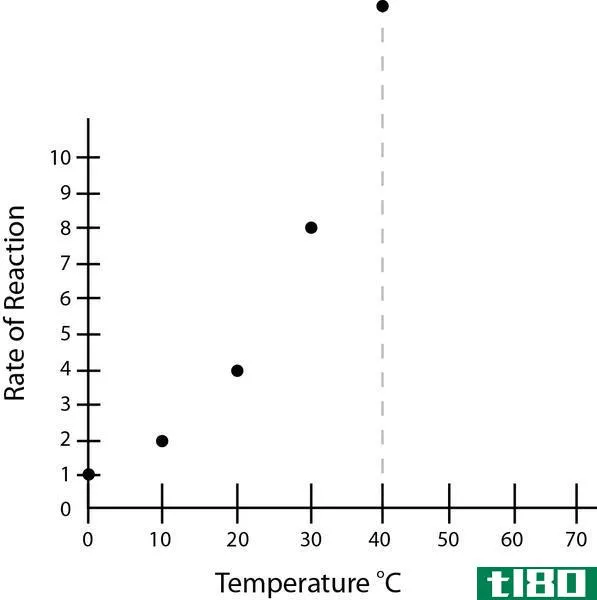
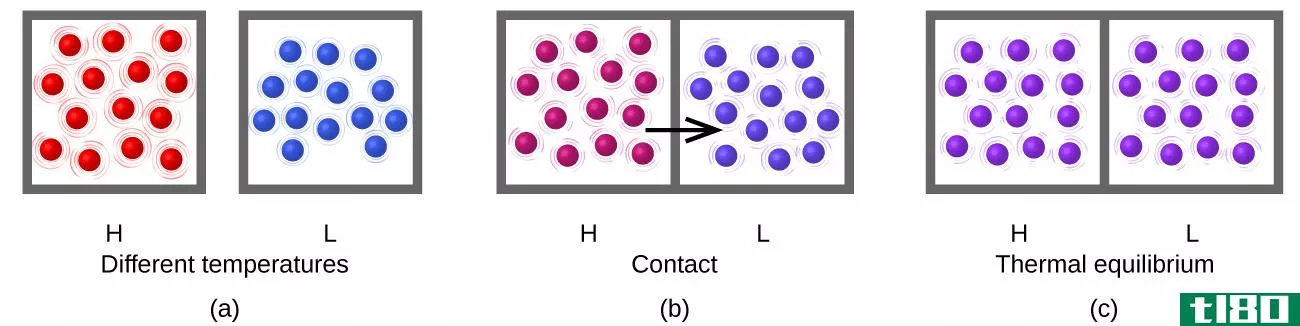
反应速率是指反应物和产物浓度随时间的摩尔每秒变化。它还取决于物理性质,如温度。它随温度的偏差而波动。它还取决于反应完成的时间。时间越长,反应速率的值越大。
它间接地取决于温度。它可以随着压力和催化剂的变化而改变。增加反应速率值的主要因素是反应分子碰撞频率的增加。反应速率的单位可以根据反应的顺序来确定。
当反应物的摩尔浓度降低,产物的摩尔浓度增加时,反应速率总是增加。同样地,反应速率总是随着反应物摩尔浓度的增加而降低,而产物的摩尔浓度却在降低。
什么是速率常数(rate c***tant)?
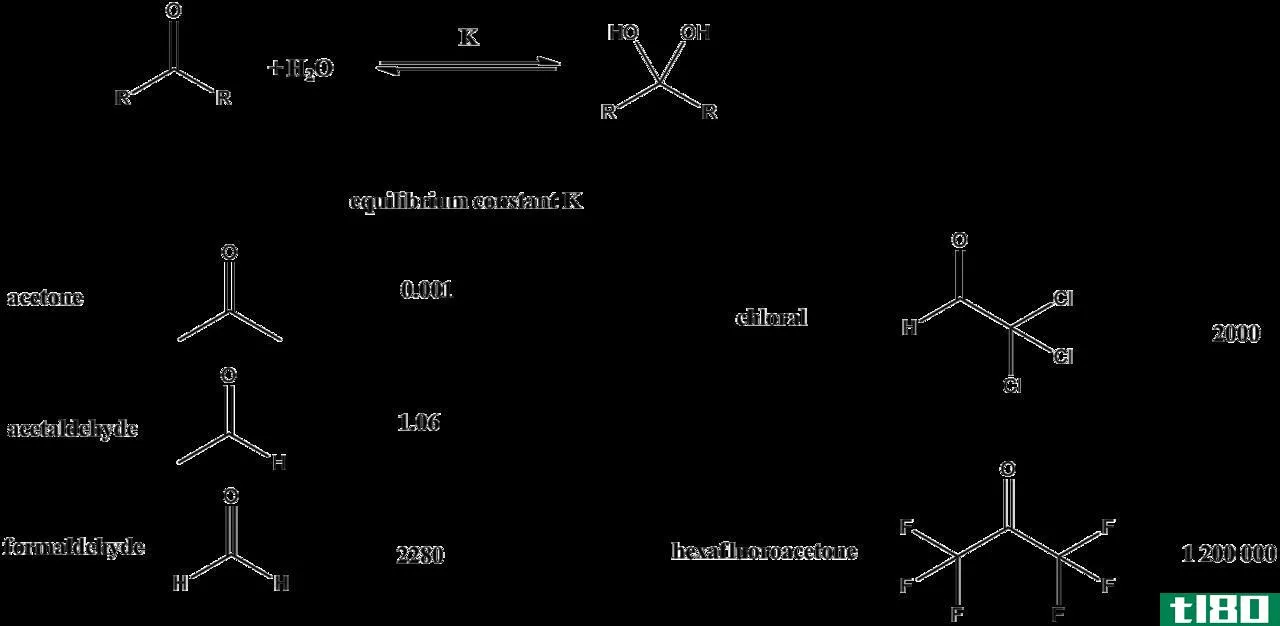
比率常数定义为比例的特定常数。它不取决于摩尔浓度。它主要取决于物理性质,如温度。它只能随着温度的变化而变化。其他量不影响速率常数,如压力和催化剂。
它也不取决于反应完成的时间。它不会改变反应是立即发生还是突然发生。反应分子碰撞的频率不影响速率常数的变化。K可以表示。
这个常数有助于确定反应过程中任何时候的反应速率。速率常数的增减只能由物理性质如温度决定。
关键区别
- 反应速率是反应物和产物的数量随时间的增加而变化,而速率常数是在某种化学反应中存在的比例常数。
- 反应速率主要取决于反应物和产物的摩尔浓度,而速率常数不取决于反应物和产物的摩尔浓度。
- 反应速率不直接取决于物理性质,如温度;另一方面,速率常数直接取决于物理性质,如温度。
- 反应速率主要用以实现一个反应的时间;另一方面,速率常数不需要花时间来完成一个反应。
- 反应速率与压力有关,而速率常数与压力无关。
- 在催化剂的作用下,反应速率可以改变反应机理,而在催化剂的存在下,反应速率常数并没有改变反应机理。
- 反应速率用摩尔每秒来表示,而速率常数是从反应右边带出来的。
- 反应速率完全取决于碰撞频率,而速率常数不取决于碰撞频率。
结论
以上讨论得出反应速率是反应物的摩尔变化和单位时间的产物浓度,而速率常数是特定反应的比例常数。