主要区别
价态和氧化态的主要区别在于,价态是原子价壳层中电子的位数,而氧化态是原子在原子化合物中失去或获得电子的能力。
价(valency) vs. 氧化态(oxidation state)
价态是原子最外层电子的整数,而氧化态是原子获得或损失的电荷数。价态并不表示化合物中的电荷;另一方面,氧化态表示化合物原子上的电荷。价态决定了一个原子生成的键的数目,而氧化态并不表示任何类型的键。纯元素的价态是指存在于最外层壳层中的电子数,而纯元素的氧化态由于其中性而为零。价态用来表示价壳层中的电子数,而氧化态用来表示原子上的电荷价态没有任何电荷指示,而氧化态则表示原子上的电荷。原子的价态不变,而氧化态则因化合物而异。价态表示键的数目,而氧化态并不表示这种行为。
比较图
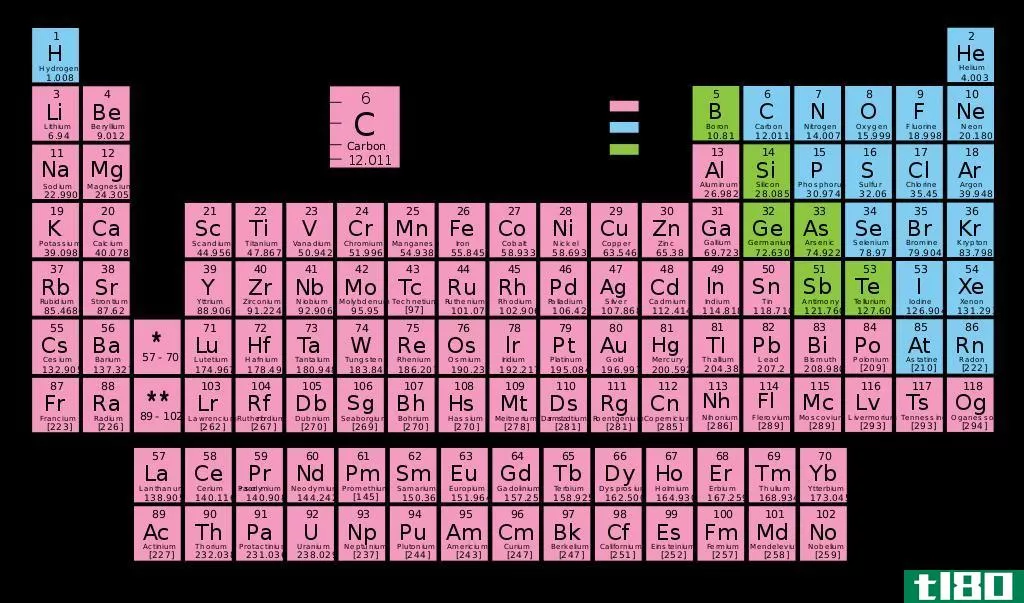
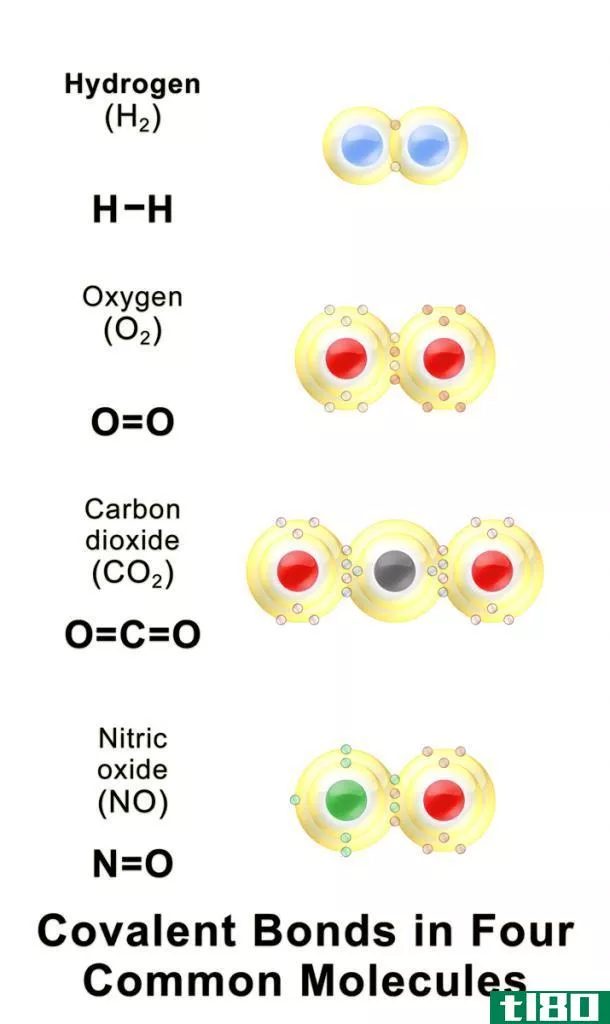
什么是价(valency)?
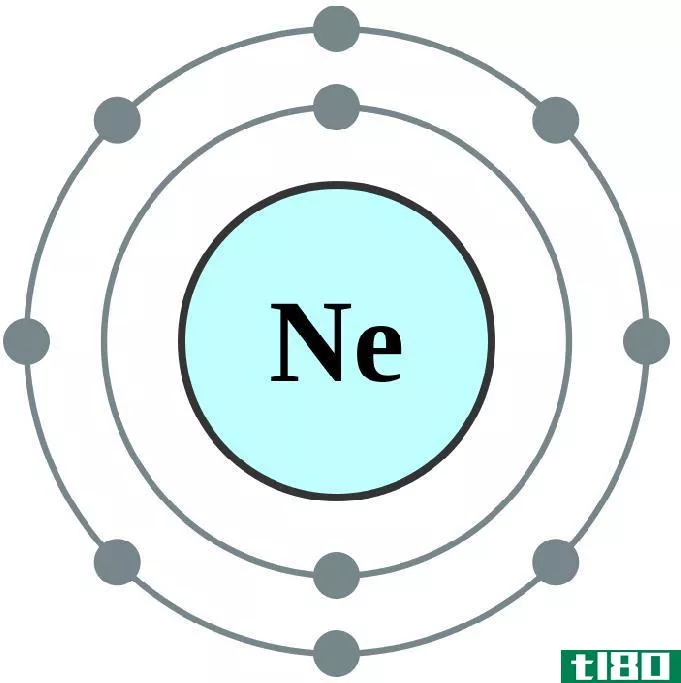
指原子最外层的电子数。它用电荷来表示,因为每个原子的价壳层中都有它的电子。它的数目还表明它可以与其他元素结合以满足其电荷的键数。纯元素的价态也有一些电荷,因为它有电子。一个原子的价态不变,即原子是否成键。原子的价是一个原子获得或失去一个电子的程度的指标。每一组元素都有相同的价态。价态用来确定价壳层电子。价态被认为是原子中的电荷。价是数字指示符。价壳层电子可以改变或保持不变。稀有气体元素的价态为零,因为稀有气体已经完成了价壳层并变得稳定。价是绝缘原子的性质。价是一个原子为达到稳定状态而形成的键的数目。价态是基于单个电荷的电子组态。价永远不可能是零。例如,钠的价是1,镁的价是2,因为它们存在于1A和2A族中。
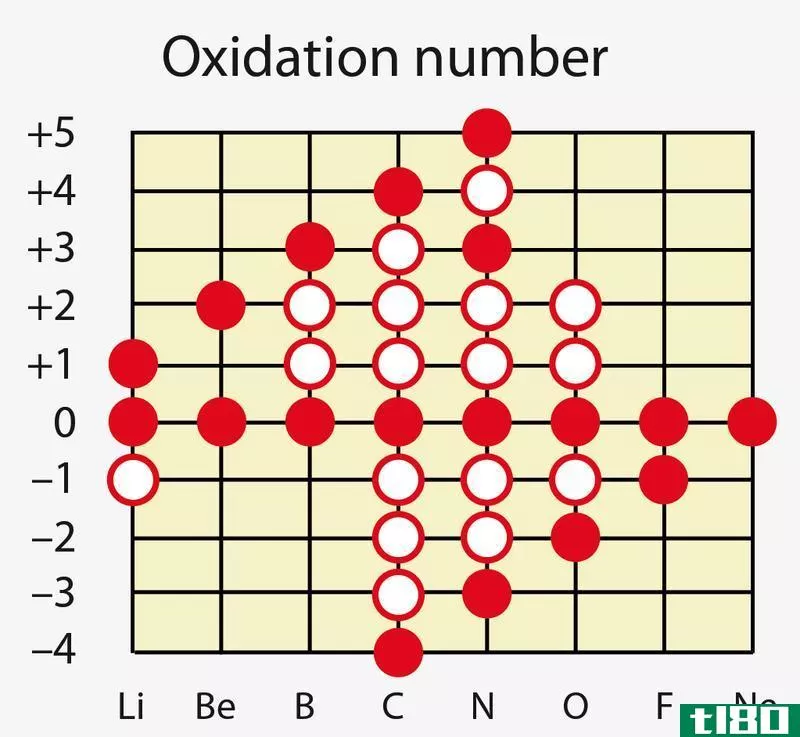
什么是氧化态(oxidation state)?
原子的最大电子数是一个原子的增益或损失。原子上的电荷表示。氧化数并没有给出它与其他元素之间的几个键的信息。原子的不同性质有不同的氧化数。它是在不同化合物中原子上存在电荷。纯或中性元素的氧化数为零。氧化数是原子能获得或丢失的电子的特定数量。元素的氧化数有各种各样的规律。不同化合物中的元素具有不同的氧化数,如氧原子具有氧化数-2,过氧化物+1和超氧体中的元素的氧化量为-½。氧化数,简单地说是原子的电子增益或损耗的数量。它是在符号的右上角带电荷的。氧化状态只是指原子过去稳定的电子。元素的氧化数是分配给元素的编号。氧化状态原子中计算的数。氧化状态可以为零。氧化次数的增加称为氧化,而氧化数的减少称为还原。
主要区别
- 价是价壳层中的电子数,而氧化数则是原子能获得或损失的最大数。
- 价态不是用电荷表示的;另一方面,氧化状态是由电荷指示的。
- 价态告诉我们键的数目;相反,氧化态并不表示键的数目。
- 纯元素的价态不同,可以是任何电荷;另一方面,纯元素的氧化态为零。
- 原子的价态不变,而氧化数随不同化合物的存在而变化。
- 化合物的价态不变,而元素的氧化态则不同。
- 价永远不可能是零,而氧化可以是零。
结论
价态是价轨道上的电子数,而氧化态是电子获得或失去原子能力。