主要区别
可逆过程和不可逆过程的主要区别在于可逆过程可以在两个方向上发生,而不可逆过程只在一个方向上发生。
可逆过程(reversible process) vs. 不可逆过程(irreversible process)
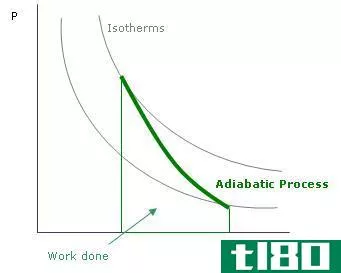
可逆过程是可以改变方向的热力学化学过程,而不可逆过程是不能改变方向的热力学化学过程。可逆过程可以在反面的两个方向进行;不可逆过程只能在一个方向上发生。可逆过程用于获得化学反应的初始状态;另一方面,不可逆过程不能给出化学反应的初始状态。
可逆过程是反应物可以重新获得的过程,而不可逆过程是所有反应物完全消耗的过程。可逆过程是一种化学反应,可以发生在正向和反向,而不可逆过程是只发生在正向的化学反应。
可逆反应总是发生在封闭系统中,而不可逆过程发生在开放系统中。可逆过程是可以建立动态平衡的过程,而不可逆过程是无法建立动态平衡的过程。在可逆过程中,系统中会发生许多变化,而在不可逆过程中,系统中发生的变化是有限的。
启动可逆过程需要少量的力,而启动不可逆过程需要很大的力。在可逆过程中,所做的功较大,而在不可逆过程中,所做的功较少。
比较图
什么是可逆过程(the reversible process)?
可逆过程是热力学的化学过程,可以正向和反向进行。可逆反应可以改变其方向。它是反应物和产物不断改变其浓度的过程。它是反应物转化为产物,产物并排转化为反应物的过程。
在可逆过程中,需要少量的力来启动反应,反应是由许多较小的步骤组成的。这就是为什么在这个过程中要做更多的工作。可逆过程永远不会完成,在反应物和产物的量相等的过程中可以建立动态平衡。
它是我们可以得到系统或化学反应的初始状态的过程。在可逆过程中会出现一些偏差。
什么是不可逆过程(irreversible process)?
不可逆过程是热力学的化学过程,它只能向前发展。这个过程永远不会改变它的程序方向。反应物完全消耗并转化为产物的过程。
在一个不可逆的过程中,开始化学反应需要大量的能量。它只能在一个步骤中发生。为什么在这个过程中所做的工作量很小。不可逆过程可以假设为完成反应。
这是一个不可能建立动态平衡的过程,在这个过程中,反应物和产物的数量相等。这是一个反应一旦开始就永远不能回到原来阶段的过程。在整个过程中出现的偏差非常有限。
主要区别
- 可逆过程可以在反应的两边改变方向,而不可逆过程不能在化学反应的两边改变方向。
- 可逆过程可以从两侧进行;在另一侧,不可逆过程只能从一侧发生。
- 可逆过程用于寻找生化反应的初始状态;另一方面,不可逆过程不能给出生化反应的初始状态。
- 可逆过程可以回收反应物,而不可逆过程可以消耗所有反应物。
- 可逆过程可以正向和反向进行,而不可逆过程只能在正向进行。
- 可逆过程总是发生在密封系统中,而不可逆过程发生在未锁定系统中。
- 可逆过程是可以建立化学平衡的化学过程,而不可逆过程不能建立化学平衡。
- 在可逆过程中,系统中会发生许多变化,而不可逆过程中,系统中也会发生有限的变化。
- 一个小的能驱动反应的力对于开始可逆过程是必要的,而一个能驱动反应的大力对于开始不可逆过程是必不可少的。
- 在可逆过程中,有大量的功,而在不可逆过程中,有少量的功。
结论
上述讨论表明,可逆过程和不可逆过程都是热力学化学反应的类型。可逆过程是一个可以正向和反向进行的化学过程,而不可逆过程是只能朝着正向进行的过程。