主要区别
键能和键离解能的主要区别在于,键能是指化合物中两个原子间的所有键崩解所需的平均能量,而键离解能是崩解特定键所需的平均能量。
键能(bond energy) vs. 键离解能(bond dissociation energy)
键能是一个术语,用来描述一个化合物中两个原子间所有相连的键被分解所需的平均能量。然而,另一方面,键离解能是在均分解过程中只需要打破一个特定键所需的平均能量。
在键能方面,两个原子之间的每一个键都会以不同的能量消散,而这两个原子之间的其他键所消耗的能量不同。相反,在键离解能的情况下,这两个原子之间的每一个键的分解能值在相互比较时保持不变。
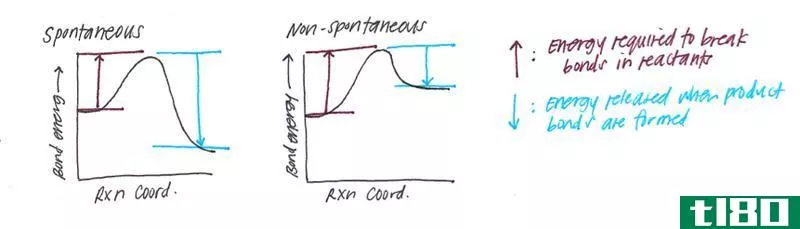
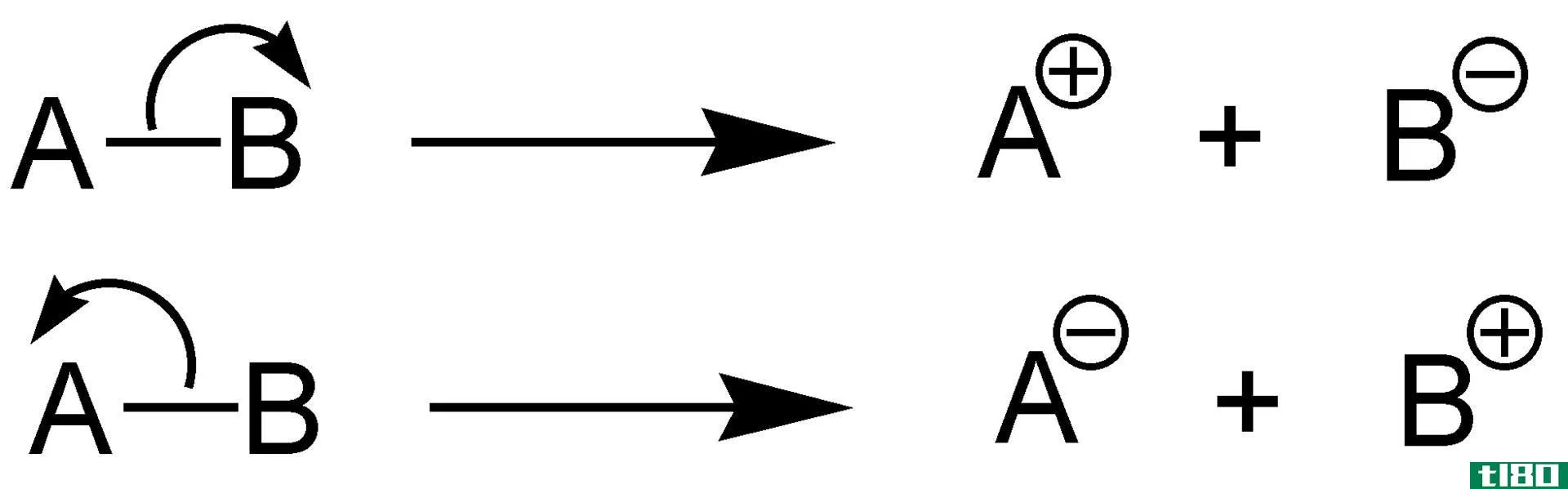
键能给出这两个原子之间形成键时所用的能量。在键离解能的情况下,它是从形成键所用的原子产生自由基所需的能量。在键能的情况下,键可以以任何方式断裂,即对称或不对称,因此称为异溶解离,但对于键离解能,键只以对称的方式断裂,因此称为溶血离解。
键能是分子内某一类型所有键的离解能的平均值,但由于是单个化学键的离解能,键离解能等于双原子分子所需的能量。在键能的情况下,不可能确定分子中较弱或较强的键,因为它是所有键离解的平均能量值,但在键离解能的情况下,可以确定原子中最强和最弱的键,因为它是与单个键相关联的能量。
比较图
什么是键能(bond energy)?
键能用来描述一个化合物中两个原子间所有相连的键被分解所需的平均能量。在这里,两个原子之间的每一个键都将以不同的能量消散,这与这些原子之间的其他键相比,因为它同时涉及到所有键的断裂;因此,键断裂可以以任何方式发生,比如对称或不对称。这就是为什么它被称为异溶解离。
键能给出了在这两个原子之间形成键时所用的能量。因此,一个分子内某一类型的所有键的离解能的平均值是不一样的,并且随每个键的不同而变化。
不可能确定分子中的弱键或强键,因为它是所有键离解的平均能量值。例如,在从甲烷分子中移除氢原子的情况下,甲烷分子中每个氢原子的键离解能都会有所不同。
什么是键离解能(bond dissociation energy)?
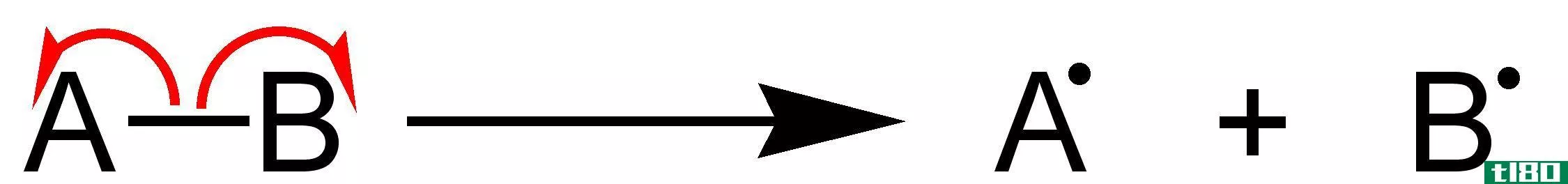
键离解能,键离解能被认为是在均裂过程中只破坏或破坏特定键所需的能量量。在这种情况下,这种断裂被称为溶血性的,因为键的断裂只是对称的。当两个原子之间的每一个键相互比较时,这两个原子之间的每一个键都会消耗相同的分解能量。
在键离解能的情况下,它需要形成原子自由基,这些自由基用于形成键。因此,键离解能等于双原子分子所需的能量,因为它是单个化学键的离解能。在这种情况下,可以确定原子中最强和最弱的键,因为它是与单键相关的能量。
在甲烷的同一个例子中,如上所述,每个双原子分子的离解能对于每个键都是相同的。然而,每个氢原子的键能是不同的。在水分子的另一个例子中,键解离通过均裂形成质子和羟基。
主要区别
- 键能用来描述撕掉两个原子之间所有连接键所需的平均能量量。另一方面,键离解能是在均解过程中只破坏一个特定键所需的平均能量量。
- 键能是指两个原子之间的每一个键,与其他键相比,它们会消耗不同数量的能量;另一方面,键离解能涉及到这两个原子之间存在的每个键的相同的分解能值。
- 键能指的是在这两个原子之间形成一个键的开始所用的能量;然而,键离解能是指在形成键的原子中形成自由基所需的能量。
- 键能包括键的断裂,这种断裂可以是对称的,也可以是不对称的;因此,它们的断裂称为异解离。键离解能包括键的对称断裂,因此,这些键的断裂称为溶血性离解。
- 键能是一个分子内所有该类型键的能量离解平均值;相反,键离解能等于双原子分子所需的能量。
- 在键能的情况下,无法确定分子中较弱或较强的键,但在键离解能的情况下,可以确定原子中最强和最弱的键。
结论
键能是化合物中两个原子间以异溶方式分解所有键所需的能量,而键离解能是以溶血方式破坏特定键所需的能量。