真实电解质和电位电解液的关键区别在于,真正的电解质完全分解成离子,而电位电解质则部分分解成离子。
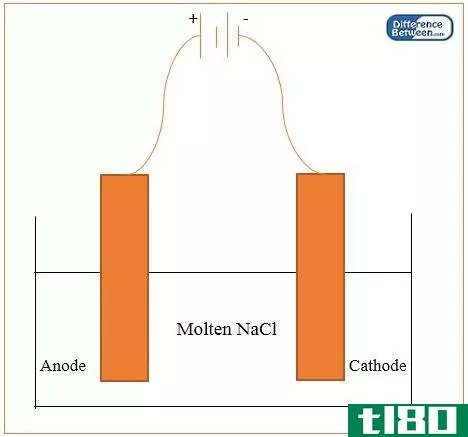
根据它们产生离子和导电的能力,我们可以把所有化合物分为电解质和非电解质两类。电解是将电流通过电解溶液并迫使正负离子向各自的电极移动的过程。非电解质不能参与电解过程。
目录
1. 概述和主要区别
2. 什么是真正的电解质
3. 什么是电解液
4. 并列比较-真实电解液与电位电解液的表格形式
5. 摘要
什么是真电解质(true electrolyte)?
真正的电解质是能完全分解成离子的物质。它们也被称为强电解质。这些化合物溶解在水或其他溶液中时容易产生离子形式。化合物解离后,溶液中既有阳离子,也有阴离子,因此这些离子可以携带电流通过电解溶液。这就是为什么它的名字“电解质”,意思是“导电能力”。
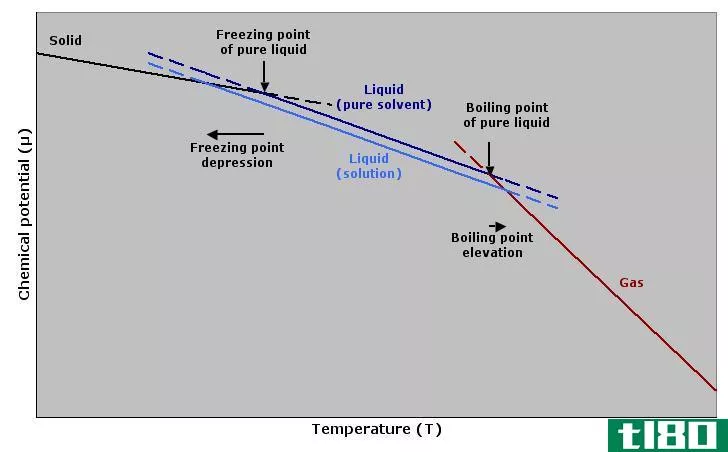
在相同的温度下,真实电解质的浓溶液的蒸汽压比纯水低。强酸、强碱、非弱酸和弱碱的可溶离子盐可归为真正的电解质。
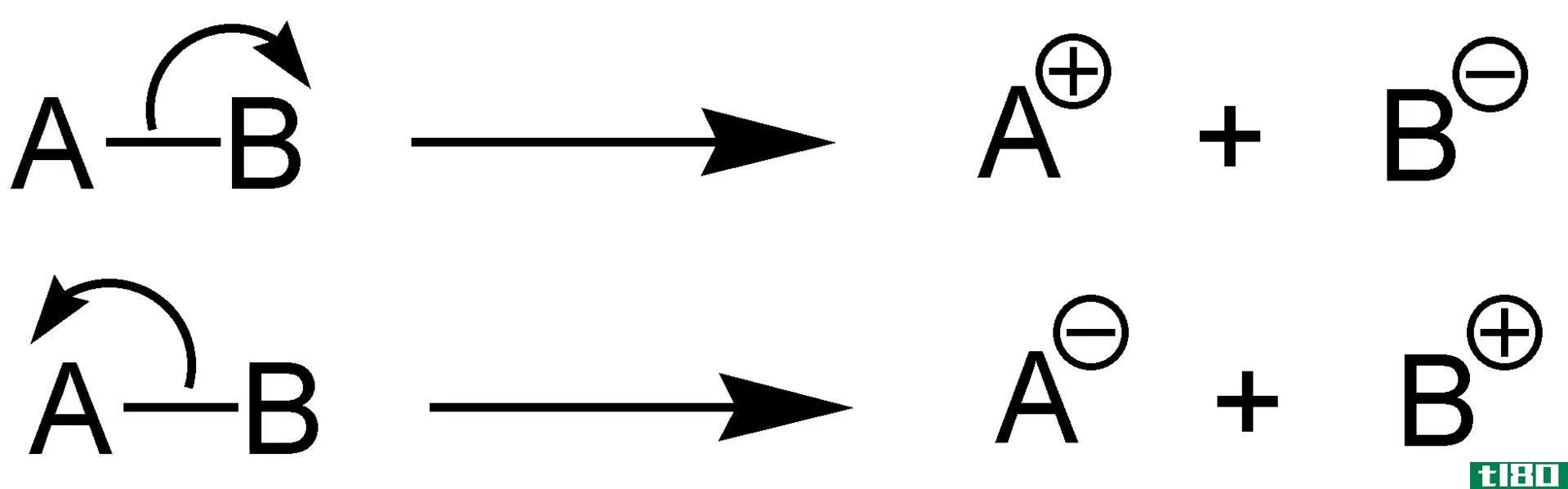
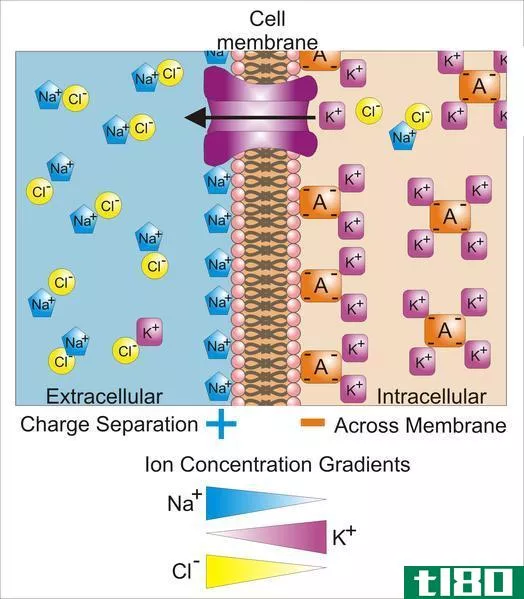
图01:完全分离
在**正电解液电离的化学反应时,我们可以在一个方向上用一个箭头来表示完全的电离反应,而不是电位或弱电解质。这个单箭头表示反应完全发生。真正的电解质只有在熔融或溶液状态下才能导电。由于电离度很高,一个真正的电解液所能产生的电压是非常高的。
什么是电位电解液(potential electrolyte)?
潜在电解质是能部分分解成离子的物质。这意味着它在水溶液中不能完全分解成离子。因此,潜在电解质的水溶液中既含有离子物种,也含有未解离的分子。通常,电位电解液的解离度约为1-10%。它们也被称为弱电解质。一些常见的弱电性电解质包括醋酸、碳酸、氨、磷酸等,它们要么是弱酸,要么是弱碱。

图02:醋酸分解的化学反应
写弱电解质分解的化学反应时,我们用两个指向相反方向的半箭头。这个箭头表示在水溶液中离子种类和结合的分子之间存在平衡。
是的(true)和电位电解液(potential electrolyte)的区别
根据它们产生离子和导电的能力,我们可以把所有化合物分为两类:电解质和非电解质。电解质又分为真实电解质和潜在电解质两部分。真实电解质和电位电解液的关键区别在于,真正的电解质完全分解成离子,而电位电解质则部分分解成离子。真实电解质的离解强度为100%,而电位电解质的离解强度为1~10%。
下表总结了真实电解质和潜在电解质之间的区别。
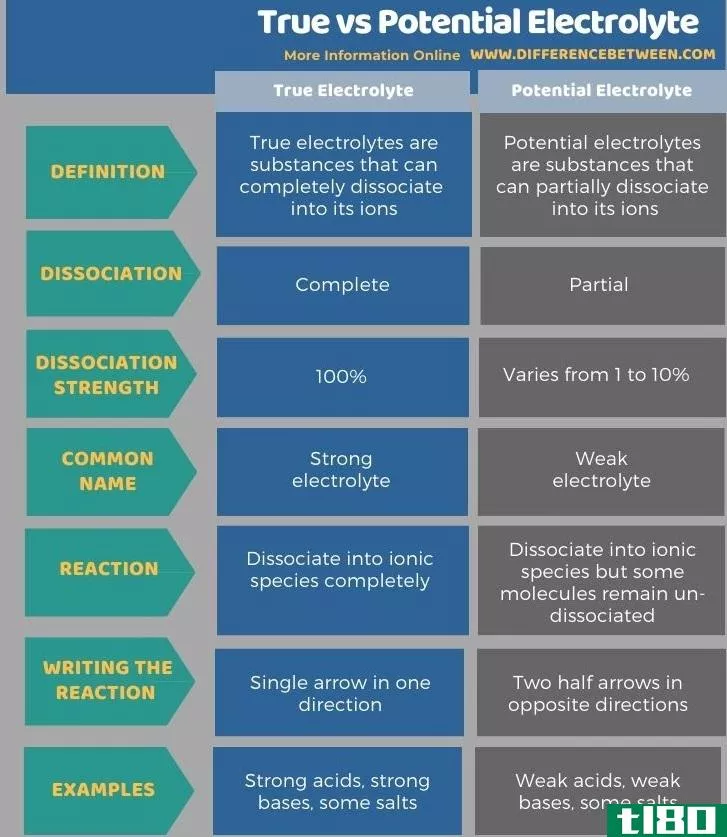
总结 - 是的(true) vs. 电位电解液(potential electrolyte)
真正的电解质是能完全离解成离子的物质,而电位电解质是能部分离解成离子的物质。因此,真实电解质与电位电解液的关键区别在于,真实电解质完全分解成离子,而电位电解质部分分解成离子。
引用
1赫尔曼斯汀,托德。“弱电解质的定义和示例”,ThoughtCo,2020年2月11日,