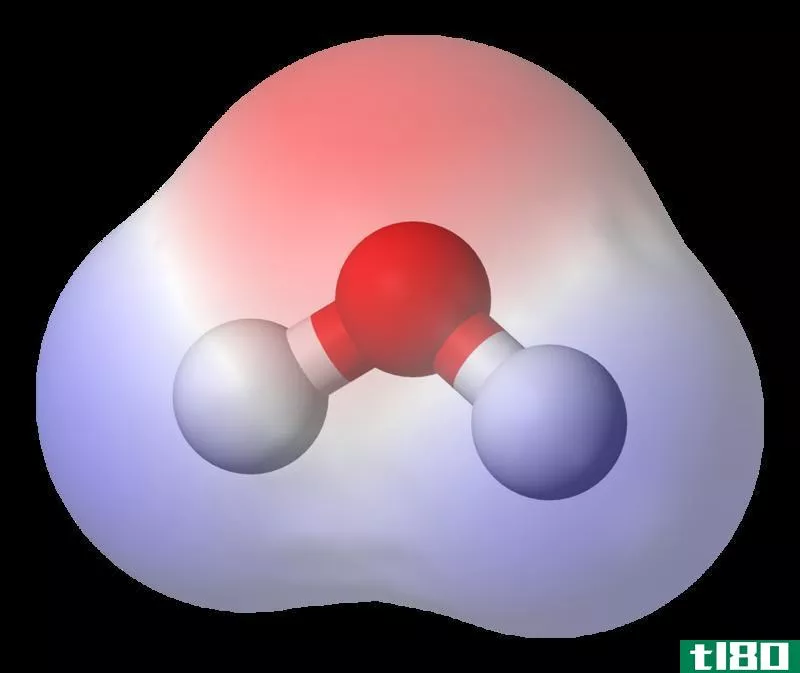
极性分子和偶极分子的关键区别在于,极性分子有两个相反的两端,带着相反的电荷,而极性分子有两个极性。
一般来说,我们可以交替使用极性和偶极两个术语,因为这两个术语都描述了具有两个相反末端的单个分子。这些不同的末端是由于整个分子中电子分布的不同而产生的。
目录
1. 概述和主要区别
2. 什么是极性分子
3. 什么是偶极分子
4. 并列比较-极性与偶极分子的表格形式
5. 摘要
什么是极性分子(polar molecules)?
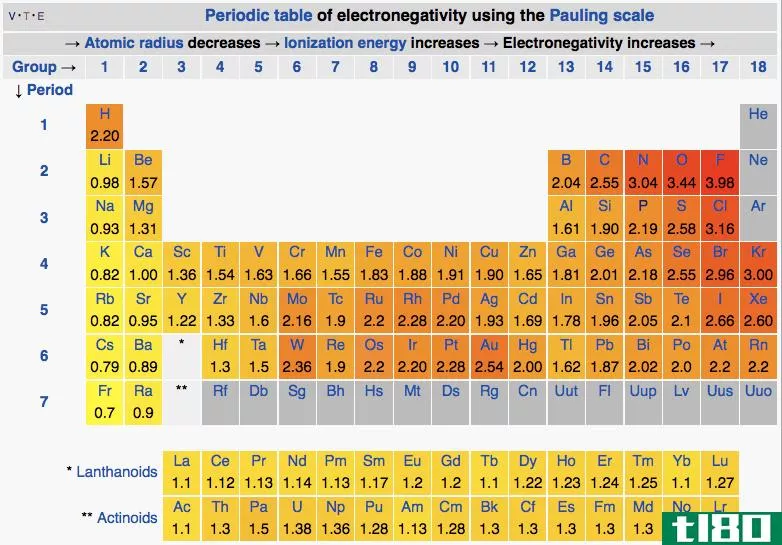
极性分子是具有极性键的化学物质。这些极性键的偶极矩之和不等于零。极性键有部分正电荷端和部分负电荷端。这些电荷是由于整个化学键中电子分布的差异而产生的。电子分布的差异是化学键中原子电负性值不同的结果。在这里,电负性越强的原子将键-电子对的电子吸引到自己身上,这就给这个原子带了部分负电荷。因此,这个键中的另一个原子由于周围缺乏电子密度而获得部分正电荷,这表明原子核中质子的正电荷。
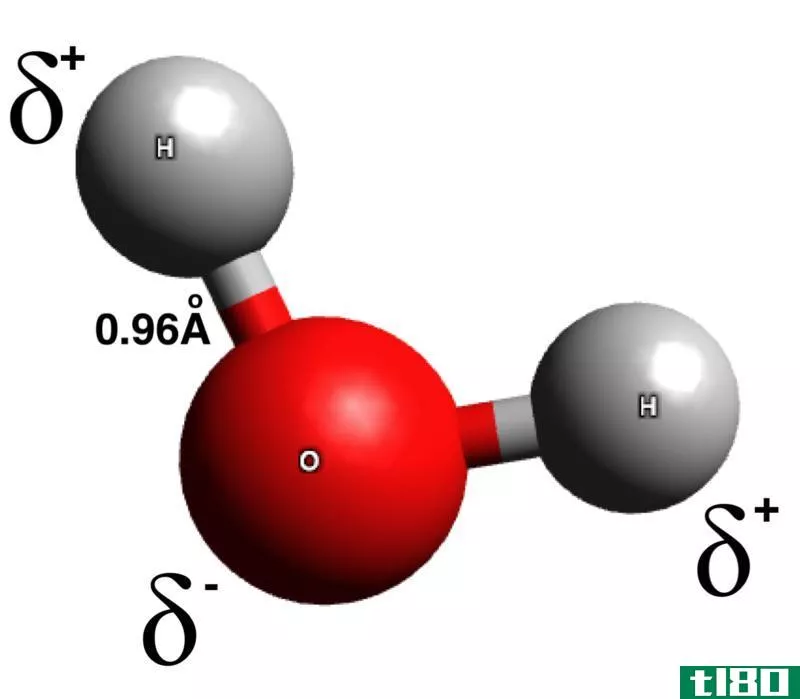
图01:水分子中的电荷分离
此外,当分子的空间排列(几何结构)使正电荷**在分子的一侧,负电荷**在另一侧时,就可以形成极性分子。杨树分子的一些常见例子包括水、氨、乙醇、二氧化硫和硫化氢。
什么是偶极分子(dipolar molecules)?
偶极分子是在同一分子中有两个极的化学物质。当电子在整个分子中的分布不均匀导致电荷分离时,就会产生偶极矩。偶极矩是由于分子中原子的电负性值不同而产生的。与极性化合物不同,偶极分子是电中性的(分子的总电荷为零)。这是因为分子的电荷分离显示出完全相同的电荷值,方向正好相反,相互抵消,因此没有净电荷。

图02:羰基氧化物中电荷的离域
在大多数偶极分子中,电荷在整个分子中是非定域的。一些例子包括羰基氧化物、重氮甲烷、膦叶立德等。
极地的(polar)和偶极分子(dipolar molecules)的区别
极性分子和偶极分子的关键区别在于,极性分子有两个相反的两端,带着相反的电荷,而极性分子有两个极性。然而,一般来说,我们可以交替使用极性和偶极两个术语,因为这两个术语都描述了具有两个相反末端的单个分子。
另外,极性分子与偶极分子的另一个显著区别是,极性分子是在电荷分离时形成的,而偶极分子的形成是由于原子电负性值的不同而形成的。
下面是极性分子和偶极分子之间差异的汇总表。

总结 - 极地的(polar) vs. 偶极分子(dipolar molecules)
简而言之,我们可以交替使用极性和极性两个术语,因为这两个术语都描述了一个具有两个相反末端的单个分子。极性分子和偶极分子的关键区别在于,极性分子有两个相反的两端,带着相反的电荷,而极性分子有两个极性。
参考文献:
1“13.3:键极性和偶极矩。”化学剧本,歌词,2019年6月3日,可在这里查阅。“偶极化合物”,维基百科,维基媒体基金会,2018年7月13日,可在这里查阅。