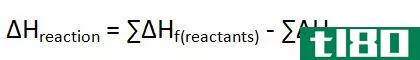焓变示例问题
这个示例问题显示了如何找到过氧化氢分解的焓。

焓回顾
在开始之前,您可能希望复习热化学定律以及吸热和放热反应。焓是一种热力学性质,是添加到系统中的内能与其压力和体积的乘积之和。它是系统释放热量和执行非机械工作的能力的度量。在方程式中,焓用大写字母H表示,而比焓用小写字母H表示。它的单位通常是焦耳、卡路里或BTU。
焓的变化与反应物和产物的数量成正比,所以你可以利用反应的焓的变化来解决这类问题,或者通过反应物和产物的生成热来计算焓的变化,然后将该值乘以存在的物质的实际量(摩尔)。
焓问题
过氧化氢根据以下热化学反应分解:H2O2(l)→ H2O(l)+1/2o2(g);ΔH=-98.2 kJ计算1.00 g过氧化氢分解时的焓变化ΔH。
解决方案
这类问题可以通过使用一个表格来查找焓的变化来解决,除非它被提供给你(这里就是这样)。热化学方程式告诉我们ΔH因为1摩尔H2O2的分解为-98.2 kJ,因此该关系可用作转换因子。
一旦你知道焓的变化,你就需要知道相关化合物的摩尔数来计算答案。使用周期表将过氧化氢中氢原子和氧原子的质量相加,你会发现H2O2的分子质量为34.0(氢为2x1+氧为2x16),这意味着1mol H2O2=34.0g H2O2。
使用这些值:
ΔH=1.00 g H2O2 x 1 mol H2O2/34.0 g H2O2 x-98.2 kJ/1 mol H2O2ΔH=-2.89 kJ
回答
当1.00 g过氧化氢分解时,焓变化ΔH=-2.89 kJ
这是一个好主意,检查你的工作,以确保所有的转换系数抵消了,留下一个答案,在能源单位。计算中最常见的错误是意外地切换转换因子的分子和分母。另一个陷阱是重要的数字。在这个问题中,样品的焓和质量的变化都是用3个有效数字给出的,所以答案应该用相同的数字来报告。
- 发表于 2021-09-15 09:47
- 阅读 ( 154 )
- 分类:化学
你可能感兴趣的文章
生成热(heat of formation)和反应热(heat of reaction)的区别
...别在于,生成热是在标准条件下形成一摩尔物质过程中的焓变化,而反应热是在恒压下发生的化学反应过程中焓的变化。 生成热和反应热是化学反应的重要焓值。我们将这些术语定义为标准条件,即标准压力和标准温度。在这...
- 发布于 2020-10-18 06:22
- 阅读 ( 535 )
放热的(exothermic)和吸热的(endothermic)的区别
...或其他类似的能源,这个反应就无法完成。 放热反应的焓变总是负的,而吸热反应的焓变总是正的。这分别是由于反应中热能的释放和吸收。最终产物在放热反应中是稳定的。吸热反应的最终产物不太稳定。这是由于形成的弱...
- 发布于 2021-06-22 11:50
- 阅读 ( 455 )
键能(bond energy)和键离解能焓(bond dissociation energy enthalpy)的区别
...享)被均裂(分解为相等的碎片)裂解产生碎片时的标准焓变;通常是激进的物种。因此,键能和键离解能之间的主要区别是键能是平均值,而键离解能是特定键的特定值。 什么是键能和键离解能(焓)(bond energy and bond dissoci...
- 发布于 2021-06-26 10:13
- 阅读 ( 482 )
焓(enthalpy)和内能(internal energy)的区别
...。但是如果∆H为负值,表示反应向外释放能量。 此外,焓变发生在物质的相态变化中。例如,如果固体转化为液体,焓就会改变。这叫做熔合热。当液体转化为气态时,焓变称为汽化热。 Figure 01: The change in state or phase of substanc...
- 发布于 2021-06-29 08:17
- 阅读 ( 944 )
吸热的(endothermic)和放热反应(exothermic reactions)的区别
...吸热反应和放热反应,我们可以计算反应物和产物之间的焓变。如果没有,我们可以观察反应混合物的温度变化。吸热反应和放热反应的主要区别在于,吸热反应从周围吸收能量,而放热反应向周围释放能量。 覆盖的关键领域 1...
- 发布于 2021-06-29 08:53
- 阅读 ( 1320 )
疏水的(hydrophobic)和亲水分子(hydrophilic molecules)的区别
...相互作用和混合,以进一步减少与水的接触。这个反应的焓变是正值,因为团块周围的水分子之间的氢键被分解了。由于团块所在的笼被分解释放出疏水分子,系统的熵增加。当考虑到整个过程时ΔG值取负值。因此,疏水键的形...
- 发布于 2021-06-29 14:28
- 阅读 ( 305 )
常见的一般化学问题列表
...焦耳转换 电负性 经验公式 计算化合物的经验和分子式 焓变-反应的焓变 焓变-给定质量反应的焓变 焓变-水的焓变 熵计算 熵变 反应熵 直线方程 平衡常数 气体反应的平衡常数 平衡浓度 实验误差 英尺到英寸的换算 自由能与压...
- 发布于 2021-09-08 10:26
- 阅读 ( 268 )
冰对水蒸气的焓变
这个焓变示例问题是当冰的状态从固态转变为液态水,最后转变为水蒸气时的焓变。 焓回顾 在开始之前,您可能希望复习热化学定律以及吸热和放热反应。 问题 给出:冰的熔化热为333 J/g(即当1克冰融化时,333 J被吸收...
- 发布于 2021-09-15 09:46
- 阅读 ( 201 )
利用键能求焓变
你可以用键能来计算化学反应的焓变。这个示例问题说明了该怎么做。 回顾 在开始之前,您可能希望复习热化学定律以及吸热和放热反应。单键能量表可以帮助您。 焓变问题 估算以下反应的焓变化ΔH: H2(g)+Cl2(g...
- 发布于 2021-09-15 09:49
- 阅读 ( 159 )
用hess定律计算焓变
...“恒热和赫斯定律”,指出化学反应的总焓是反应步骤的焓变化之和。因此,可以通过将反应分解为具有已知焓值的组分步骤来发现焓变化。这个示例问题演示了如何使用赫斯定律,使用类似反应的焓数据来发现反应的焓变化的...
- 发布于 2021-09-15 09:51
- 阅读 ( 286 )