为什么水是万能溶剂?
水被称为通用溶剂。这里解释了为什么水被称为万能溶剂,以及什么性质使它能很好地溶解其他物质。

化学使水成为一种很好的溶剂
水被称为通用溶剂,因为溶于水的物质比溶于任何其他化学物质的都多。这与每个水分子的极性有关。每个水(H2O)分子的氢侧带有轻微的正电荷,而氧侧带有轻微的负电荷。这有助于水将离子化合物分解成正离子和负离子。离子化合物的正部分被吸引到水的氧侧,而化合物的负部分被吸引到水的氢侧。
为什么盐溶于水
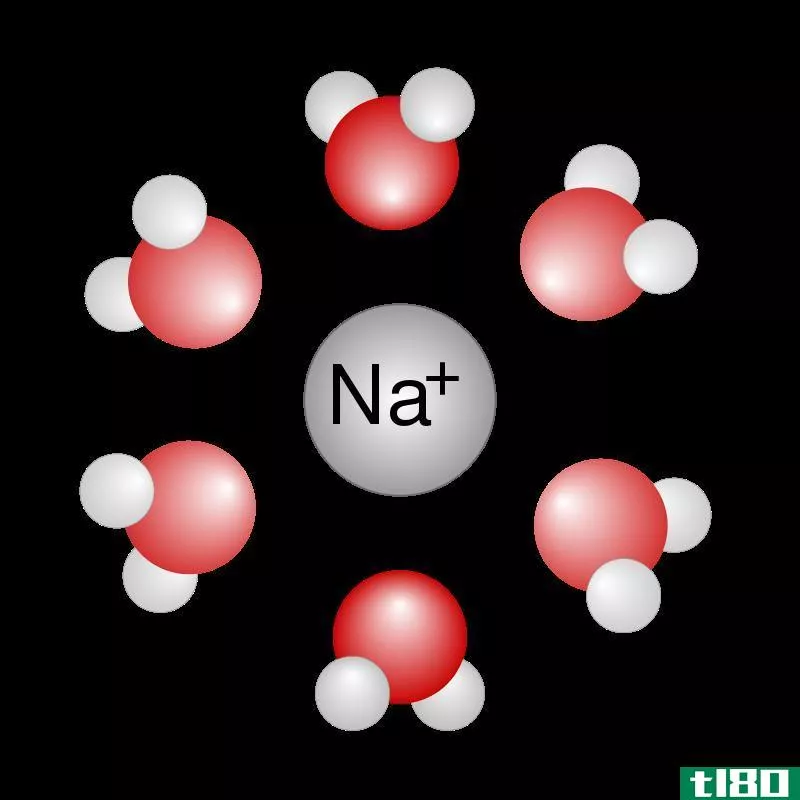
例如,考虑盐在水中溶解时会发生什么。盐是氯化钠。化合物的钠部分带正电荷,而氯部分带负电荷。这两个离子通过离子键相连。另一方面,水中的氢和氧通过共价键连接。来自不同水分子的氢和氧原子也通过氢键连接。当盐与水混合时,水分子定向,使带负电荷的氧阴离子面对钠离子,而带正电荷的氢阳离子面对氯离子。尽管离子键很强,但所有水分子极性的净效应足以将钠和氯原子拉开。一旦盐被拉开,它的离子就会均匀分布,形成均匀的溶液。
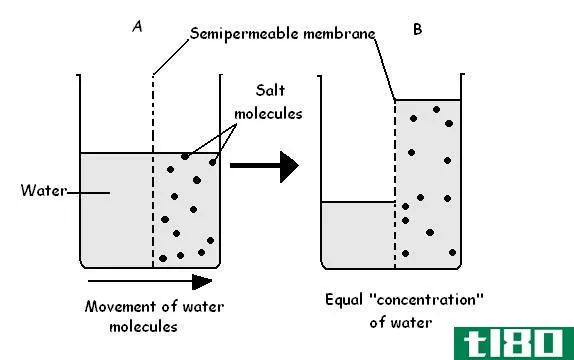
如果大量的盐与水混合,就不会全部溶解。在这种情况下,溶解继续进行,直到混合物中有太多的钠和氯离子,水才能赢得与未溶解盐的拔河比赛。这些离子会阻碍水分子完全包围氯化钠化合物。提高温度会增加颗粒的动能,从而增加可溶解在水中的盐量。
水不能溶解一切
尽管它被称为“通用溶剂”,但有许多化合物是水不能溶解或不能很好溶解的。如果化合物中带相反电荷的离子之间的吸引力很大,那么溶解度就会很低。例如,大多数氢氧化物在水中的溶解度较低。此外,非极性分子在水中溶解不好,包括许多有机化合物,如脂肪和蜡。
总之,水之所以被称为万能溶剂,是因为它能溶解大多数物质,而不是因为它能溶解每一种化合物。
- 发表于 2021-10-04 05:22
- 阅读 ( 423 )
- 分类:化学
你可能感兴趣的文章
离解(dissociation)和溶剂化(solvation)的区别
...离子化合物与极性溶剂之间存在离子-偶极相互作用。E、 水是极性溶剂。当氯化钠加入水中时,极性水分子分别吸引钠离子和氯离子,导致钠离子和氯离子分开。这导致氯化钠离子化合物分解。 离解(dissociation)和溶剂化(solvation)...
- 发布于 2020-09-21 23:34
- 阅读 ( 1072 )
极地的(polar)和非极性溶剂(nonpolar solvents)的区别
...得到部分负电荷,而两个氢原子得到部分正电荷。 图01:水是极性溶剂 此外,我们还将极性溶剂分为极性质子溶剂和极性非质子溶剂两大类。极性质子溶剂含有不稳定的H+离子。这意味着这些溶剂的分子可以提供氢原子。然而,...
- 发布于 2020-10-12 14:40
- 阅读 ( 508 )
水的(aqueous)和非水溶液(nonaqueous solution)的区别
...和极性的,才能溶解在水中形成水溶液。虽然我们称水为万能溶剂,但我们不能溶解几乎所有的东西。例如,我们不能将脂肪溶解在水里,所以任何地方都没有脂肪水溶液。 图01:水中钠离子 在写化学方程式时,我们用符号(aq...
- 发布于 2020-10-16 19:11
- 阅读 ( 784 )
一氧化二氢(dihydrogen monoxide)和水(water)的区别
...或二氢钼是一种可以存在于物质的所有三种相中的水,而水是我们用来命名水的液态的术语。 一氧化二氢是H2O,它有两个氢原子与一个氧原子共价键合。它是许多已知有毒物质、疾病和致病因子的组成部分,对我们有害。水是...
- 发布于 2020-10-17 13:33
- 阅读 ( 902 )
溶剂(solvent)和溶质(solute)的区别
...最常见的是,我们使用液体作为溶剂。此外,在液体中,水是一种普遍的溶剂,因为它比任何其他溶剂都能溶解许多物质。此外,我们可以在液体溶剂中溶解气体、固体或任何其他液体溶质。但是,在气体溶剂中,只有气体溶质...
- 发布于 2020-10-19 19:02
- 阅读 ( 677 )
渗透(osmosis)和生物学中的扩散(diffusion in biology)的区别
...质两部分组成。溶液是通过溶解溶质在溶剂中制成的。盐水是最好的例子,其中盐是溶质,水是溶剂。有三种类型的溶液,如等渗、低渗和高渗。在等渗溶液中,细胞内外的溶质浓度相等。在这些条件下,没有溶剂分子通过细胞...
- 发布于 2020-10-20 05:27
- 阅读 ( 534 )
水(water)和液体(liquid)的区别
水和液体的关键区别在于,水是指处于液态阶段的化合物,而液体是物质的物理状态。 水和液体是两个经常被混淆为意义相似的词。然而,水和液体有明显的区别。水是地球表面发现最多的化合物。它覆盖了地球表面的70%。...
- 发布于 2020-11-06 16:31
- 阅读 ( 337 )
溶解(dissolution)和崩解(disintegration)的区别
...如,极性物质不能溶解在非极性溶剂中。在其他溶剂中,水是一种通用溶剂,能很好地溶解许多物质。气体溶剂只能溶解气体溶质。 溶解过程形成的溶液通常是均匀的。有一些因素可以加速溶解,其中包括温度。溶解是一个动...
- 发布于 2021-06-25 16:21
- 阅读 ( 446 )
溶剂(solvent)和溶质(solute)的区别
...在这里,茶是解决办法。糖和奶粉溶于热水中。因此,热水是这里的溶剂。在有机化学实验室中,通过重结晶来纯化化合物是一种常见的实验。在这个实验中,不纯的化合物在溶剂中,溶剂只溶解混合物中需要纯化的化合物,通...
- 发布于 2021-06-29 11:15
- 阅读 ( 937 )
溶质(solute)和溶剂(solvent)的区别
...可以通过一杯茶来澄清。奶粉和糖在温水中溶解。这里温水是溶剂,糖和奶粉是溶质。 溶质特性 溶质的沸点比溶剂高。 它们可以是固体、液体或气体。 通过增加溶质颗粒的表面积,溶解度增加。固体颗粒被破碎成小块。 对于...
- 发布于 2021-07-08 07:32
- 阅读 ( 526 )