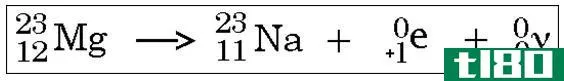如何原子中的质子、中子和电子?(protons, neutrons, and electrons in an atom?)
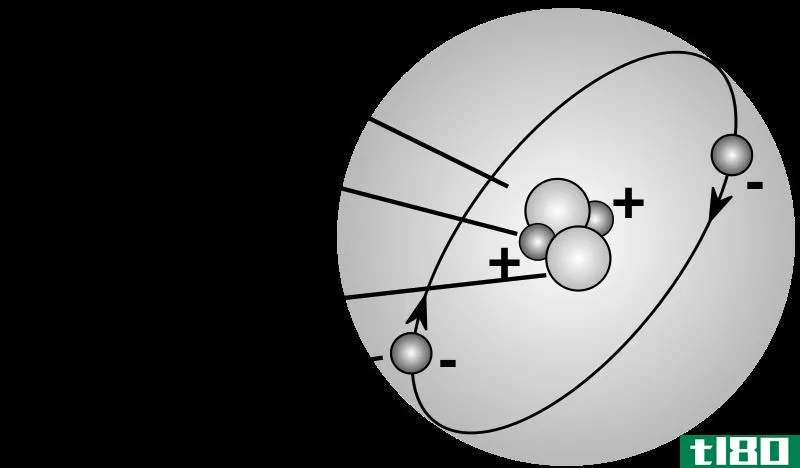
原子的三个部分是带正电荷的质子、带负电荷的电子和中性中子。按照这些简单的步骤找出任何元素原子的质子、中子和电子数。

关键收获:质子、中子和电子的数量
- 原子由质子、中子和电子组成。
- 质子带正电荷,而电子带负电荷,中子带中性。
- 中性原子具有相同数量的质子和电子(电荷相互抵消)。
- 离子的质子和电子数不相等。如果电荷为正,则质子比电子多。如果电荷为负,则电子过剩。
- 如果你知道原子的同位素,你可以找到中子的数目。只需从质量数中减去质子数(原子序数),即可找到剩余的中子。
获取有关元素的基本信息
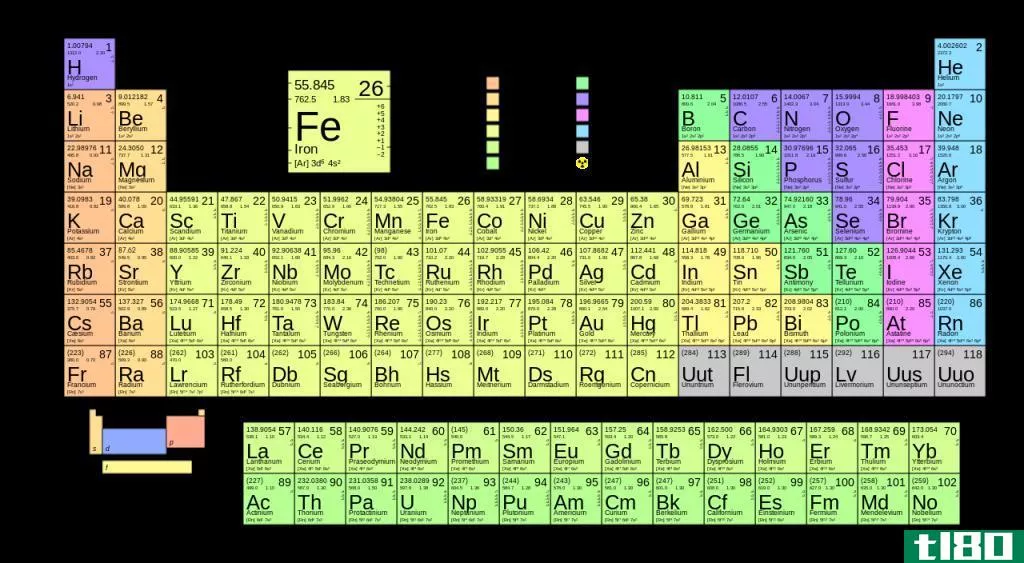
您需要收集有关元素的基本信息,以找到质子、中子和电子的数量。幸运的是,您只需要一个元素周期表。
对于任何原子,您需要记住的是:
质子数=元素的原子序数
电子数=质子数
中子数=质量数-原子数
找出质子的数目
每种元素都是由其原子中发现的质子数来定义的。无论一个原子有多少电子或中子,元素都是由它的质子数决定的。事实上,它实际上可能有一个只由质子(电离氢)组成的原子。元素周期表是按原子序数递增的顺序排列的,所以质子数就是元素数。氢的质子数是1。对于锌,质子的数目是30。含有两个质子的原子的元素总是氦。
如果给你一个原子的原子量,你需要减去中子数得到质子数。有时,如果你只有原子量,你就可以分辨出样品的元素特征。例如,如果你有一个原子量为2的样品,你可以非常肯定元素是氢。为什么?很容易得到一个氢原子有一个质子和一个中子(氘),但是你找不到一个原子量为2的氦原子,因为这意味着氦原子有两个质子和零个中子!
如果原子量是4.001,你可以确信原子是氦,有2个质子和2个中子。原子量接近5更麻烦。是锂,有3个质子和2个中子吗?是含4个质子和1个中子的铍吗?如果没有人告诉你元素的名称或原子序数,你很难知道正确的答案。
找出电子的数目
对于中性原子,电子数与质子数相同。
通常,质子和电子的数量是不一样的,因此原子携带一个净正电荷或负电荷。如果你知道一个离子的电荷,你就可以确定它的电子数。阳离子带正电荷,质子比电子多。负离子带负电荷,电子比质子多。中子没有净电荷,因此中子的数量在计算中并不重要。一个原子的质子数不能通过任何化学反应来改变,所以你可以加上或减去电子来获得正确的电荷。如果一个离子带有2+电荷,比如Zn2+,这意味着质子比电子多两个。
30-2=28个电子
如果离子的电荷为1(简单地写上一个负上标),那么电子的数量就超过了质子的数量。对于F-,质子数(来自周期表)为9,电子数为:
9+1=10个电子
求中子数
要计算原子中的中子数,你需要计算每个元素的质量数。周期表列出了每种元素的原子量,可以用来计算质量数,例如,氢的原子量为1.008。每个原子都有一个整数个中子数,但周期表给出了一个十进制值,因为它是每个元素同位素中子数的加权平均数。所以,你需要做的是将原子量四舍五入到最接近的整数,得到一个质量数,用于你的计算。对于氢,1.008比2更接近1,所以我们称它为1。
中子数=质量数-质子数=1-1=0
对于锌,原子量为65.39,因此质量数最接近65。
中子数=65-30=35
- 发表于 2021-10-04 12:15
- 阅读 ( 382 )
- 分类:化学
你可能感兴趣的文章
中子俘获(neutron capture)和吸收(absorption)的区别
...较-中子俘获与吸收的表格形式 5. 摘要 什么是中子俘获(neutron capture)? 中子俘获是在原子核与高速中子碰撞的核反应堆中使用的一种技术。在这里,一个重元素的原子核与一个或多个中子碰撞并合并形成一个更重的原子核。因此...
- 发布于 2020-10-05 00:11
- 阅读 ( 335 )
质子(proton)和电子(electron)的区别
...的电子数和带正电荷的质子数是相似的。 什么是电子(an electron)? 电子的符号是e,带负电荷(-1)。电子的质量为9.1093×10−31kg,是最轻的亚原子粒子。1897年J.J.Thompson发现了电子,名字由Stoney给出。电子的发现是科学界的一个转...
- 发布于 2020-10-24 20:27
- 阅读 ( 581 )
中子(neutron)和中微子(neutrino)的区别
.... 并列比较-中子与中微子的表格形式 5. 摘要 什么是中子(neutron)? 中子是原子核中的亚原子粒子。我们用n来表示,中子没有电荷。它的质量为1.674927×10−27kg,略高于质子的质量。原子核也含有带正电荷的质子。如果原子核中只...
- 发布于 2020-10-26 15:06
- 阅读 ( 541 )
原子(atom)和离子(ion)的区别
原子和离子的主要区别在于它们的电荷;原子是中性的,而离子则带正电荷或负电荷。 原子是能形成键的最小中性单元,而离子是任何带电分子。离子可以由几个原子或单个原子组成。原子是唯一的,不分为各种类型,而离...
- 发布于 2020-10-26 18:32
- 阅读 ( 1354 )
正电子发射(positron emission)和电子俘获(electron capture)的区别
正电子发射(positron emission)和电子俘获(electron capture)的区别 正电子发射和电子俘获是两种类型的核过程。尽管这两个过程会导致细胞核的变化,但这两个过程以两种不同的方式发生。这两种放射性过程都发生在不稳定的核中,...
- 发布于 2020-10-28 06:02
- 阅读 ( 468 )
什么是三种类型的核辐射(the three types of nuclear radiation)
...tom – Nucle*** are found in the central region. In the gray region, the electron may be found. 质子、中子和电子的性质 微粒 颗粒分类 质量 充电 质子() 重子 中子() 重子 电子() 轻子 注意,中子比质子稍重。 离子是失去或...
- 发布于 2021-06-27 03:10
- 阅读 ( 307 )
中子(neutrons)和中微子(neutrinos)的区别
...一种基本粒子,不由任何其他粒子构成。 什么是中子(a neutron)? 到20世纪30年代初,物理学家已经发现了质子和电子。他们知道质子存在于原子核内。然而,他们意识到原子核的质量与原子核的电荷量并不相符。为了解释这种差...
- 发布于 2021-06-27 08:51
- 阅读 ( 395 )
质量数(mass number)和原子质量(atomic mass)的区别
主要差异质量数(main difference mass number) vs. 原子质量(atomic mass) 质量数和原子质量之间有着密切的联系,它们反映了元素的重量。它们的定义方式不同。质量数和原子质量之间的主要区别在于,质量数处理的是单独考虑的...
- 发布于 2021-06-27 11:19
- 阅读 ( 1046 )
氢(hydrogen)和氧气(oxygen)的区别
...别是什么-关键区别的比较 Key Terms: Allotropes, Atomic Number, Electron, Hydrogen, Isotopes, Neutron, Oxygen, Proton, Protium 什么是氢(hydrogen)? 氢是一种原子序数为1,符号为H的元素。它是元素周期表顶部的元素。氢有三种天然存在的同位素。它们...
- 发布于 2021-06-28 20:26
- 阅读 ( 461 )
同位素(isotopes)和等压线(isobars)的区别
...比较 Key Terms: Atomic Mass, Atomic number, Isobars, Isotopes, Nucleon, Neutron, Proton 什么是同位素(isotopes)? 同位素是同一元素的不同原子结构。这意味着同位素有相同的原子数,但原子质量不同。这是因为原子数是一个化学元素的唯一性质,...
- 发布于 2021-06-29 08:40
- 阅读 ( 581 )