化学中周期性的定义
周期性定义

在化学和周期表的上下文中,周期性是指元素属性随原子序数增加的趋势或反复变化。周期性是由元素原子结构的规则和可预测的变化引起的。
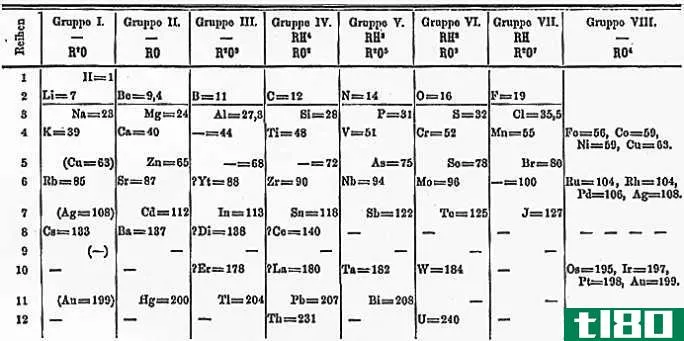
门捷列夫根据元素的循环性质组织元素,形成元素周期表。组(列)中的元素显示类似的特征。周期表中的行(周期)反映了原子核周围电子壳层的填充情况,因此,当一个新行开始时,元素以相似的性质相互叠加。例如,氦和氖都是相当不活泼的气体,当电流通过它们时会发光。锂和钠都有+1氧化状态,是反应性的闪亮金属。
周期的使用
周期性对门捷列夫很有帮助,因为它显示了他周期表中元素应该在哪里的空白。这有助于科学家发现新的元素,因为根据元素在元素周期表中的位置,可以预期它们会显示某些特征。既然这些元素已经被发现,科学家和学生们就利用周期性来预测元素在化学反应中的行为及其物理性质。周期性有助于化学家预测新的超重元素的外观和行为。
显示周期性的属性
周期性可以包括许多不同的属性,但关键的重复趋势是:
- 电离能-这是从原子或离子中完全移除电子所需的能量。电离能随着从左向右移动而增加,随着移动一组而减少。
- 电负性——衡量一个原子形成化学键的容易程度。电负性在一段时间内从左向右移动会增加,而在一个基团向下移动时会减少。
- 原子半径-这是两个相互接触的原子中间距离的一半。原子半径在一个周期内从左向右移动时减小,在一个组中向下移动时增大。离子半径是原子离子的距离,并且遵循相同的趋势。虽然增加原子中质子和电子的数量似乎总是会增加原子的大小,但在添加新的电子壳层之前,原子的大小不会增加。原子和离子的尺寸在一段时间内缩小,因为原子核的正电荷不断增加,拉入了电子壳层。
- 电子亲和力-这是一个衡量原子是否容易接受电子的指标。电子亲和力在一个周期内增加,在一个群内减少。非金属通常比金属具有更高的电子亲和力。惰性气体是这一趋势的一个例外,因为这些元素填充了电子价壳层,电子亲和性值接近零。然而,惰性气体的行为是周期性的。换句话说,即使元素组可能会破坏趋势,组中的元素也会显示周期性属性。
如果您仍然感到困惑或需要更多信息,还可以提供更详细的周期概述。
- 发表于 2021-10-05 13:08
- 阅读 ( 365 )
- 分类:化学
你可能感兴趣的文章
门捷列夫(mendeleev)和现代周期表(modern periodic table)的区别
...家致力于将元素的信息制成表格,然而,他是第一个提出周期性趋势来预测当时没有发现的元素性质的科学家。因此,门捷列夫的元素周期表有空的空间/间隙,因此这些元素一旦被发现,就可以被包括在内。镓和天竺葵就是这...
- 发布于 2021-06-27 12:49
- 阅读 ( 258 )
卤素(halogen)和氙(xenon)的区别
.... 氙(xenon) 卤素和氙是分别包含在周期表第7组和第8组中的化学元素。卤素是非常活泼的元素。但氙气是一种反应性较弱的元素。卤素是周期表第7组中的化学元素,包括F、Cl、Br、I和At。它们具有不同的物理和化学性质。氙是周期...
- 发布于 2021-06-29 10:46
- 阅读 ( 485 )
锰(manganese)和镁(magnesium)的区别
... 锰的主要区别(main difference manganese) vs. 镁(magnesium) 化学元素是一种化学物质,代表原子核中质子数相同的原子。迄今为止发现的所有化学元素都被列入元素周期表。这个元素周期表根据原子核中质子数量的升序来显示化学...
- 发布于 2021-06-29 11:38
- 阅读 ( 522 )
锕系元素(actinides)和镧系元素(lanthanides)的区别
...系元素(lanthanides) 锕系元素和镧系元素是元素周期表f区的化学元素。这意味着它们的价电子在原子的f轨道上。这些化学元素以金属形式存在,被称为内过渡金属。f区块仅由镧系和锕系组成。因为锕系元素是从一种叫做锕的化学...
- 发布于 2021-06-29 13:14
- 阅读 ( 560 )
原子半径(atomic radius)和离子半径(ionic radius)的区别
...阳离子半径。 Figure 2: Atomic and Ionic Radii of Some Elements 同一化学元素的离子可以根据电荷的大小而有不同的大小。求离子半径最常用的方法是X射线晶体学。和原子半径一样,离子半径在周期表中也有变化趋势。当我们向下移动周...
- 发布于 2021-06-29 14:30
- 阅读 ( 1010 )
d(d)和f块元素(f block elements)的区别
主要差异d(main difference d) vs. f块元素(f block elements) 化学元素是任何不能用化学方法分解或改变的物质。已知的化学元素有118种。这些化学元素是物质的组成部分。所有化学元素都按原子序数递增的顺序排列在元素周期表中。周...
- 发布于 2021-06-29 23:23
- 阅读 ( 485 )
电子增益焓(electron gain enthalpy)和电负性(electronegativity)的区别
...子之间,原子之间的电负性差别很小。 元素的电负性是周期性变化的。元素周期表根据元素的电负性值对元素进行了更好的排列。当考虑周期表中的一个周期时,每个元素的原子大小从周期的左边到右边递减。这是因为价壳层...
- 发布于 2021-06-30 00:25
- 阅读 ( 264 )
电子亲和力(electron affinity)和电离能(ionization energy)的区别
...X(g)–+e–→ X(g)-2个 电子亲和力在周期表中显示出周期性的变化。这是因为入射电子被加到原子的最外层轨道上。元素周期表的元素是按照原子序数的升序排列的。当原子序数增加时,它们最外层轨道上的电子数增加。 Figu...
- 发布于 2021-06-30 00:27
- 阅读 ( 694 )
钠(sodium)和钾(potassium)的区别
...异钠(main difference sodium) vs. 钾(potassium) 钠和钾是高活性的化学元素,可以在周期表的第1组中找到。它们是s块元素,因为它们的价电子位于最外层的s轨道。钠和钾都是非常有用的化学元素,因为它们形成多种化合物。然而,钠和...
- 发布于 2021-06-30 09:06
- 阅读 ( 592 )
铑(rhodium)和银(silver)的区别
...金属,具有非常高的熔点和沸点。它的外观与银相似,但化学性质却截然不同。银是一种非常有光泽和贵重的金属,自古就有人知道。铑和银的主要区别在于铑是一种非常硬的金属,而银是一种软金属。 覆盖的关键领域 1.什么...
- 发布于 2021-06-30 11:45
- 阅读 ( 960 )