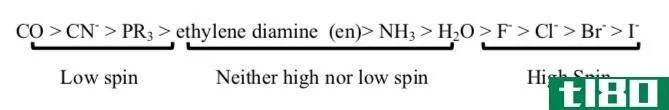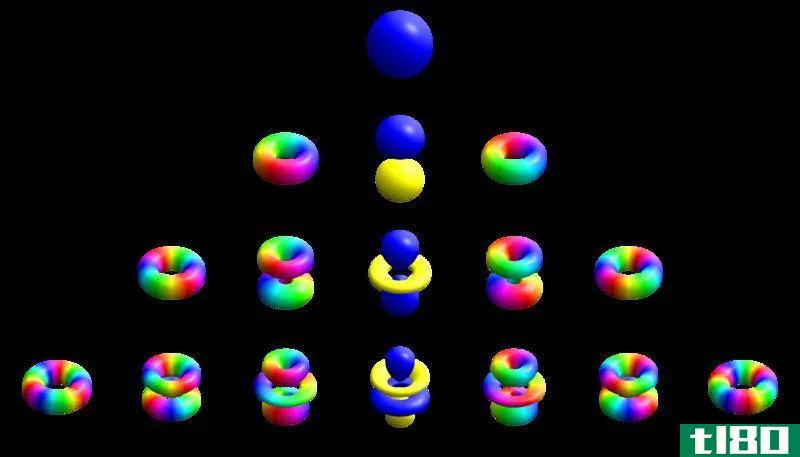自旋-轨道耦合与拉塞尔-桑德斯效应的关键区别在于,自旋-轨道耦合描述的是粒子的自旋与其轨道运动之间的相互作用,而罗素-桑德斯耦合效应描述的是多个电子的轨道角动量的耦合。
分析化学中的耦合主要是指轨道和电子等化学成分之间的相互作用。自旋轨道耦合和拉塞尔-桑德斯效应就是这两种耦合形式。罗素-桑德斯效应一般称为LS耦合,是指L轨道和S轨道角动量之间的相互作用。
目录
1. 概述和主要区别
2. 什么是自旋轨道耦合
3. 什么是拉塞尔桑德斯效应
4. 并列比较-自旋轨道耦合与罗素-桑德斯效应的表格形式
5. 摘要
什么是自旋轨道耦合(spin-orbit coupling)?
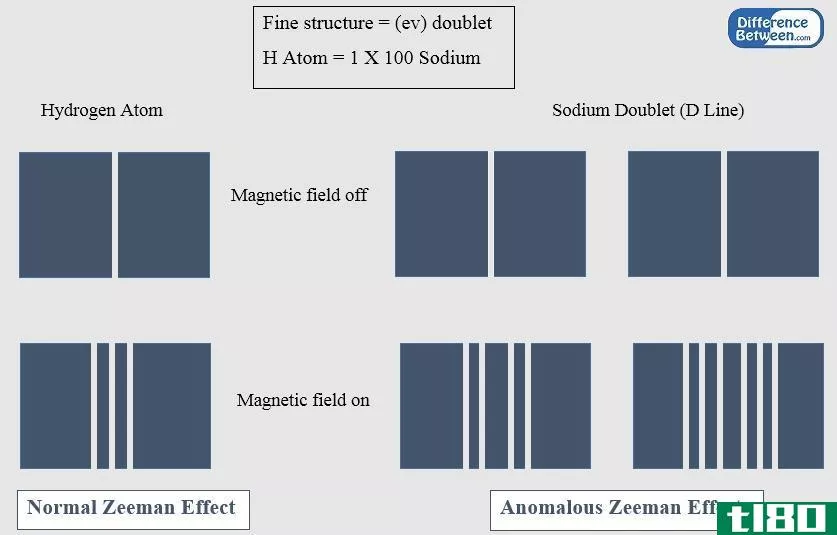
自旋-轨道耦合是粒子的自旋与其在势内部的运动之间的一种相互作用。这是一种相对论性的相互作用。化学中一个常见的自旋-轨道耦合例子是自旋-轨道相互作用,由于电子的磁偶极子与其轨道运动之间的电磁相互作用,以及带正电荷的原子核的静电场,导致电子的原子能级发生变化。我们可以探测到自旋-轨道耦合是光谱线的分裂。它表现为塞曼效应,由两种相对论效应产生:从电子的角度看,表观磁场和电子的磁矩。
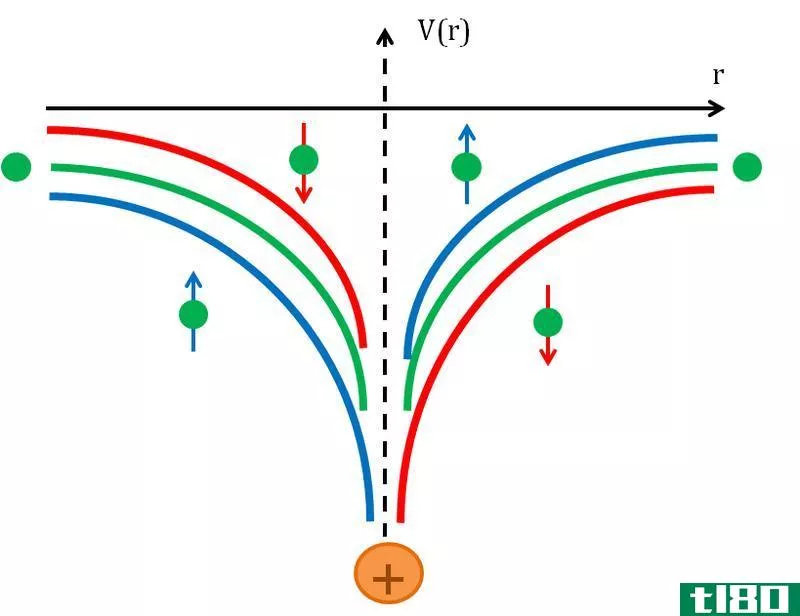
图01:自旋轨道耦合势
自旋-轨道耦合现象是自旋电子学领域中的一个重要现象,它能在半导体和其它材料中传导电子。此外,自旋-轨道耦合是导致磁晶各向**和自旋霍尔效应的原因。我们可以观察到原子能级和固体中的自旋-轨道耦合。
什么是拉塞尔桑德斯效应(russell-saunders effect)?
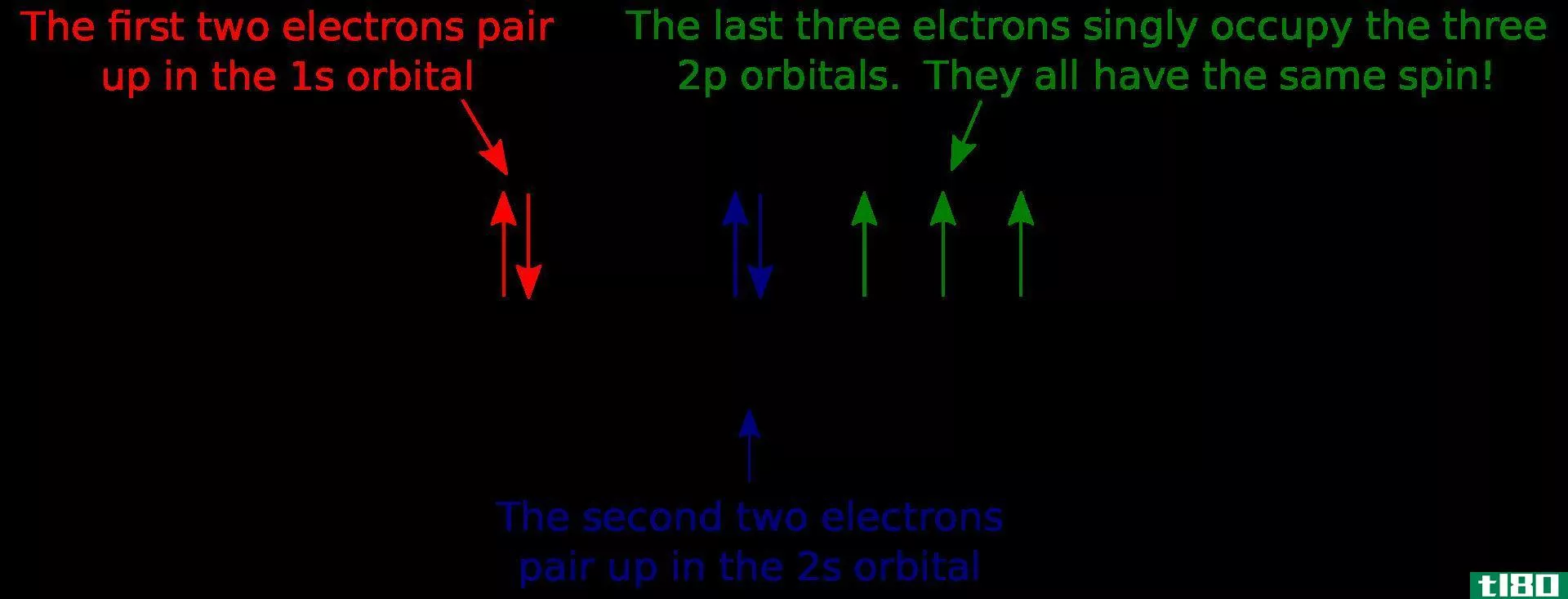
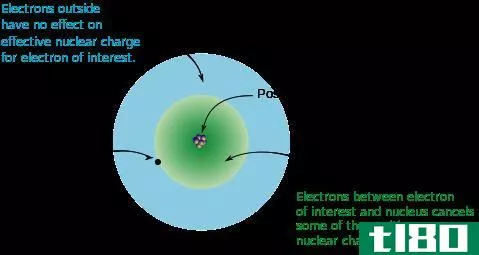
Russell-Saunders效应是分析化学中的一种耦合效应,它将多个电子的角动量强耦合在一起,形成原子的总电子轨道角动量。这种现象通常被称为LS耦合,因为L代表轨道角动量,S代表自旋角动量。这是化学中最简单的耦合方案之一。
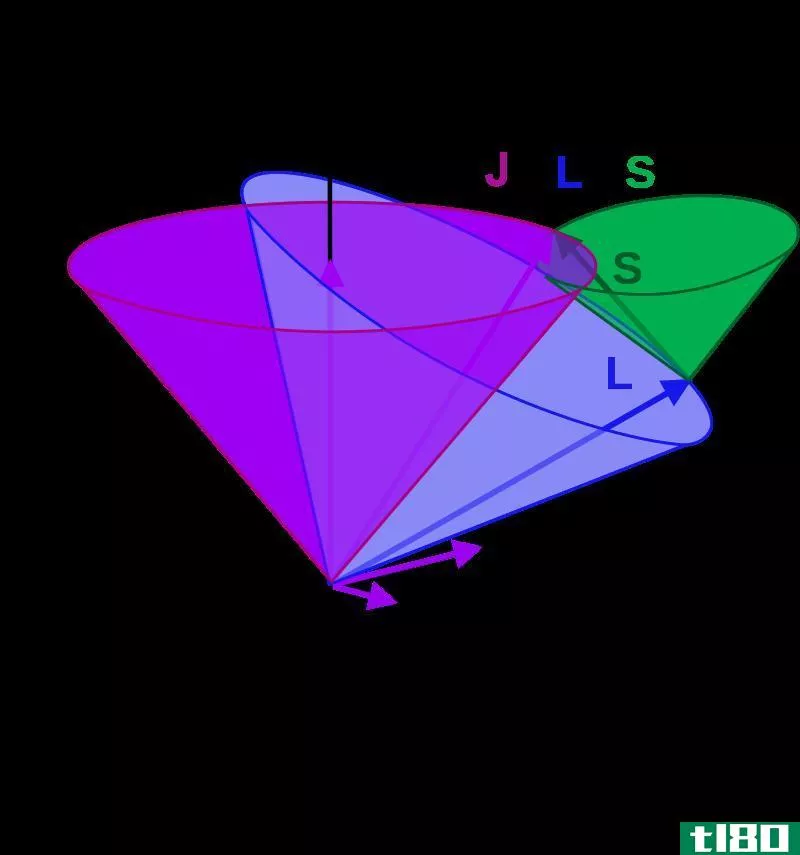
图02:LS联轴器
Russell-Saunders耦合主要在原子序数小于30的轻原子中观察到。在这些小原子中,电子自旋相互作用,形成总的自旋角动量。同样的过程发生在电子轨道(l)形成总轨道角动量(l)上。这些L和S动量之间的相互作用称为LS耦合或Russell-Saunders效应。然而,在大磁场中,我们可以观察到这两个动量的解耦。因此,这种现象适用于外部磁场较小且较弱的系统。
自旋轨道耦合(spin-orbit coupling)和罗素桑德斯效应(russell-saunders effect)的区别
分析化学中的耦合主要是指轨道和电子等化学成分之间的相互作用。自旋-轨道耦合与拉塞尔-桑德斯效应的关键区别在于,自旋-轨道耦合描述的是粒子的自旋与其轨道运动之间的相互作用,而罗素-桑德斯耦合效应描述的是多个电子的轨道角动量的耦合。
下面以表格形式总结了自旋轨道耦合和拉塞尔-桑德斯效应之间的区别。
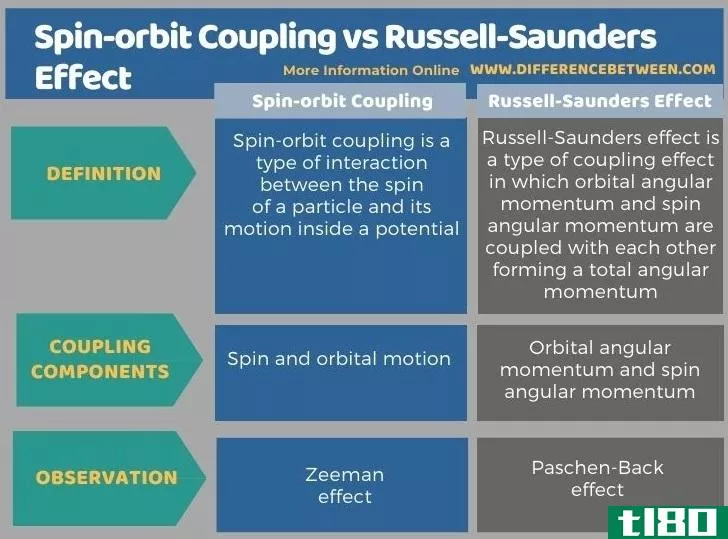
总结 - 自旋轨道耦合(spinorbit coupling) vs. 拉塞尔桑德斯效应(russellsaunders effect)
分析化学中的耦合主要是指轨道和电子等化学成分之间的相互作用。自旋-轨道耦合与拉塞尔-桑德斯效应的关键区别在于,自旋-轨道耦合描述的是粒子的自旋与其轨道运动之间的相互作用,而罗素-桑德斯耦合效应描述的是多个电子的轨道角动量的耦合。
引用
1“自旋轨道耦合”,化学图书馆,图书馆,2020年8月15日,可在这里查阅。