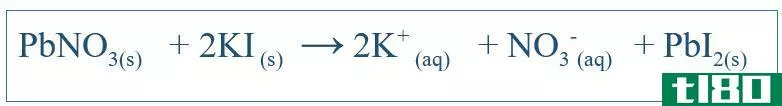组成与反应化学计量的关键区别在于,组成化学计量是指化合物的原子组成,而反应化学计量学是指化学反应过程中消耗或产生的化合物量。
化学计量学是一个化学术语,用来描述一种化合物或一种化学反应的定量数据。如果这个数据是关于一种化合物,那么我们称之为组成化学计量;如果是关于化学反应,我们可以称之为反应化学计量。
目录
1. 概述和主要区别
2. 什么是成分化学计量学
3. 什么是反应化学计量学
4. 并列比较-组成与反应化学计量的表格形式
5. 摘要
什么是成分化学计量学(composition stoichiometry)?
化学计量学是对一种化合物的原子组成进行定量分析。这个术语是指在一种特定化合物中存在的原子的类型及其数量。我们可以用化合物的化学式来确定。分子的原子性表示化合物中存在的原子总数。但它并没有提供化合物原子所属的化学元素及其数量的任何细节。然而,我们可以利用某一特定化合物的化学计量来预测化学式。因此,组分化学计量学只是一种化学物质的化学组成。
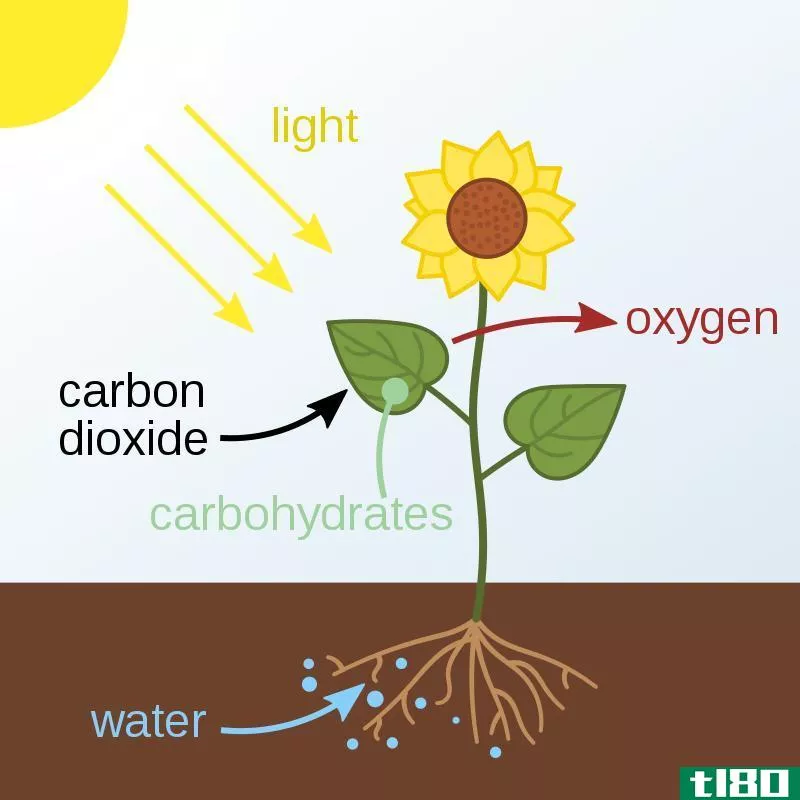
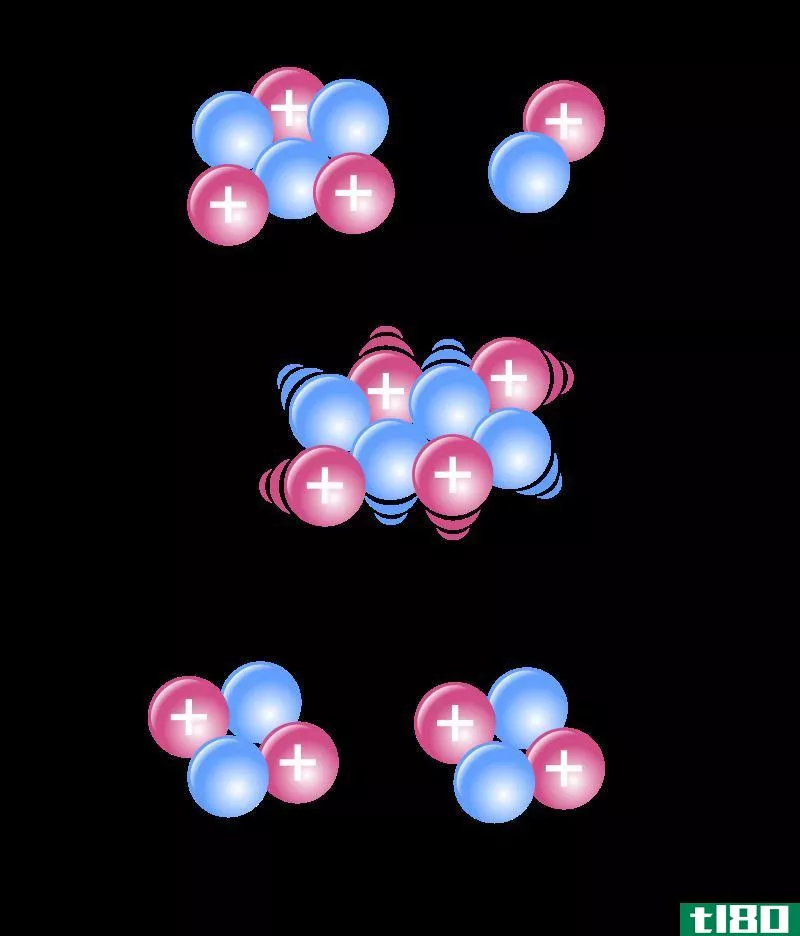
例如,葡萄糖分子的化学计量学是六个碳原子,十二个氢原子和六个氧原子。因此,我们可以确定一个葡萄糖分子含有碳、氢和氧原子,其比例为6:12:6。这是葡萄糖的化学计量。

图01:葡萄糖分子的化学成分
有不同的方法来确定一种未知化合物的化学计量比。未知化合物的样品可以用来确定样品中化学元素的类型以及每种元素的质量。然后利用这些质量可以计算出每个样品中每个元素的摩尔数。摩尔值可以四舍五入得到样品中不同类型原子之间的最大可能比值,以预测分子式。
什么是反应化学计量学(reaction stoichiometry)?
反应化学计量学是反应物与某种化学反应产物的比值。这一现象对于平衡化学反应非常重要,以获得反应物之间的关系,以及我们可以从这些物质反应中得到多少产物。
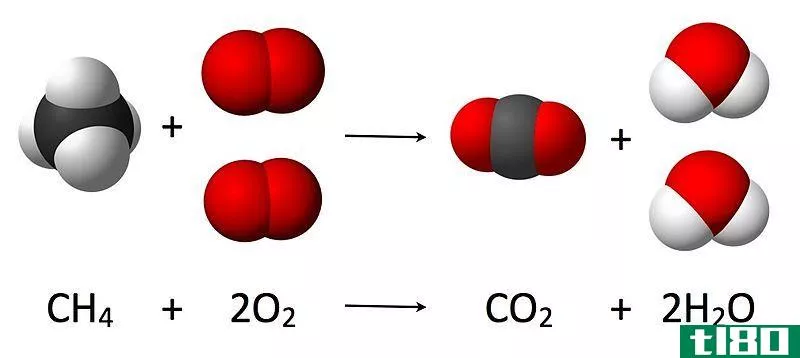
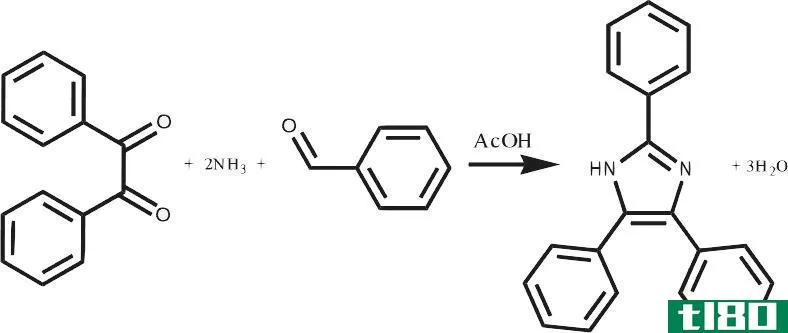
图02:反应化学计量学示例
反应化学计量的概念是基于质量守恒定律,它表明,反应物的总质量应等于产品的总质量,因为质量不能产生或破坏,只能转化为其他形式,就像能量一样。
让我们考虑一个例子来理解反应化学计量学背后的理论。碱金属和水的反应产生热能、金属氢氧化物和氢气。这里,我们知道的细节是碱金属的质量和用于反应的水的数量。反应完成后,可以收集氢气的量,利用氢气的体积计算出氢气的摩尔数。因此,假设所有碱金属都与水反应,我们可以得到反应物与反应产物的比值。这是碱金属在水反应中的反应化学计量。
作文(composition)和反应化学计量学(reaction stoichiometry)的区别
组成与反应化学计量的关键区别在于,组成化学计量是指化合物的原子组成,而反应化学计量是指化学反应过程中消耗或产生的化合物量。组成化学计量法给出了化合物中每种化学元素的原子数之比,而反应化学计量学给出了特定反应中反应物和产物之间的比率。
下面的信息图总结了组成和反应化学计量之间的区别。

总结 - 作文(composition) vs. 反应化学计量学(reaction stoichiometry)
化学计量学是一种对化合物或化学反应进行定量分析的方法。组成与反应化学计量的关键区别在于,组成化学计量是指化合物的原子组成,而反应化学计量是指化学反应过程中消耗或产生的化合物量。
引用
1“化学计量和平衡反应”,化学图书馆,图书馆,2019年9月25日,可在这里查阅。