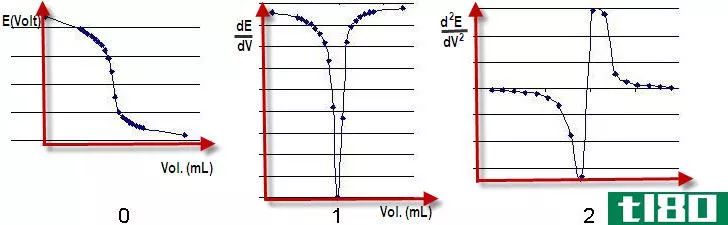
主要区别-酸碱滴定与氧化还原滴定
通常,滴定法用于测定未知溶液(分析物)的浓度。最常用的两种滴定方法是酸碱滴定法和氧化还原滴定法。酸碱滴定和氧化还原滴定的关键区别在于滴定过程中滴定剂和被分析物之间发生的反应的性质。在酸碱滴定中,发生中和反应;在氧化还原滴定中,发生氧化还原反应(氧化反应和还原反应)。使用指示剂是确定反应终点的最常用方法。
什么是酸碱滴定法(an acid-base titration)?
在酸碱滴定中,酸(酸性滴定)或碱(碱性滴定)被用作滴定剂。酸性滴定中使用的酸有H2SO4、HCl或HNO3。主要使用的碱性滴定剂是NaOH、K2CO3或Na2CO3。根据酸碱强度,酸碱滴定可分为以下几种。
- 强酸-强碱滴定
- 强酸弱碱滴定法
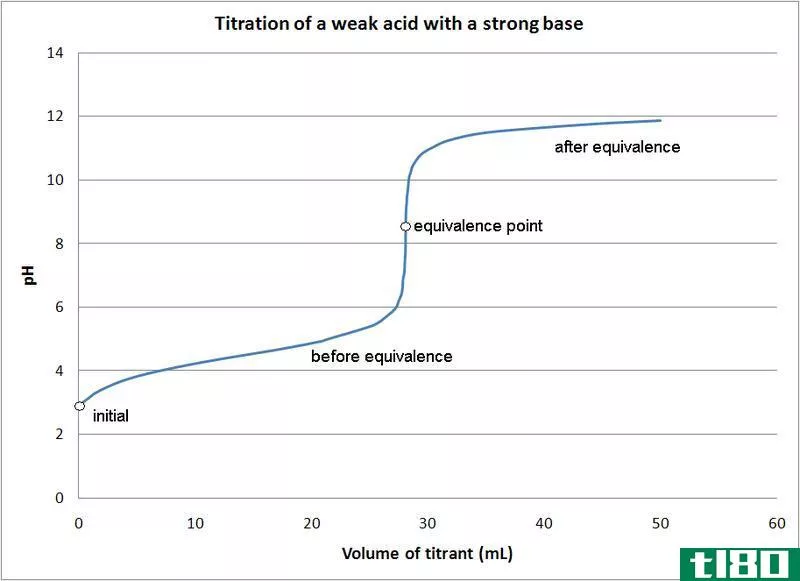
- 弱酸-强碱滴定
- 弱酸-弱碱滴定
在大多数酸碱滴定法中,指示剂用于确定反应终点。根据上述滴定类型使用不同的指示剂。
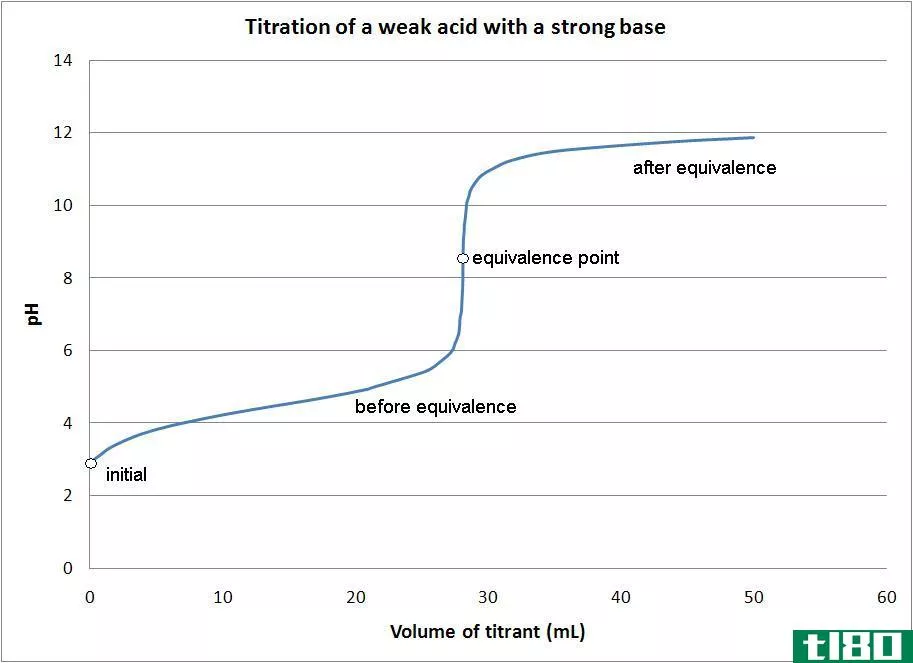
什么是氧化还原滴定法(a redox titration)?
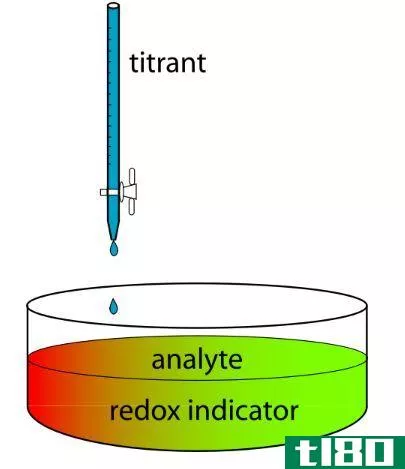
氧化还原滴定涉及氧化还原反应。氧化还原反应有两个反应:氧化反应和还原反应。氧化和还原过程同时发生,我们可以确定反应的完成。这也被称为滴定终点。这可以通过几种方法来确定:使用指示电极、氧化还原指示剂(该指示剂在氧化还原状态下产生不同的颜色)和非氧化还原指示剂(当添加过量的滴定剂时,指示剂会产生颜色)。

酸碱滴定法(acid-base titration)和氧化还原滴定(redox titration)的区别
反应性质:
酸碱滴定:酸碱滴定包括被分析物(未知浓度的溶液)与酸性或碱性滴定剂之间的中和反应。
氧化还原滴定:氧化还原反应包括分析物和滴定剂之间的氧化和还原反应。没有这样一个规则,成分氧化,哪个减少。分析物或滴定液氧化,剩余成分相应减少。
终点的确定:
酸碱滴定:一般用pH计、pH计或电导计测定酸碱滴定终点。
氧化还原滴定:测定氧化还原反应终点最常用的方法是使用电位差计或氧化还原指示剂。但是,通常分析物或滴定液在终点产生颜色。因此,在这些情况下不需要额外的指标。
示例:
酸碱滴定法:
| 类型 | 反应(指示剂) |
| 强酸强碱滴定法 | HCl+NaOHáNaCl+H2O(酚酞/甲基橙) |
| 强酸弱碱滴定法 | HCl+NH3áNH3Cl(甲基橙) |
| 弱酸-强碱滴定法 | CH3COOH+NaOHáCH3COONa+H2O(酚酞) |
| 弱酸-弱碱滴定法 | CH3COOH+NH3áCH3COO–+NH4+(无合适指标) |
氧化还原滴定:
2 KMnO4+5 H2C2O4+6 HCl→2 MnCl2+2KCl+10 CO2+8 H2O
(+7)(+3)(+2)(+4)
在上述反应中,高锰酸盐被还原,草酸被氧化。反应完成后,高锰酸盐的紫色变成无色。
KMnO4+5FeCl2+8HCl→5FeCl3+MnCl2+KCl+4H2O(+7)(+2)(+3)(+2)
Image Courtesy:
1. Titration of weak acid with strong base By Quantumkinetics (Own work) [CC BY 3.0], via Wikimedia Comm***