铀与钚
铀和钚是锕系元素中的放射性元素。
铀
铀的符号是U,它是元素周期表中的第92个元素。所以它有92个电子和92个质子。铀的电子构型可以写成[Rn]5f3 6d17s2。它有六个价电子,分别在s,d和f轨道上。铀属于锕系元素。它是银白色的固体。铀被认为是一种金属化学元素。铀是硬的,有延展性和延展性。虽然它被认为是一种金属,但它是一种不良的导电体。但它是强阳性的。此外,铀有轻微的顺磁性。铀的密度非常高,约为19.1g·cm−3。铀是一种金属,与大多数非金属元素及其化合物发生反应。反应性随温度升高而增加。像盐酸和硝酸这样的强酸也会与铀发生反应并溶解铀。当铀暴露在空气中时,会形成一层颜色较深的铀氧化物层(当铀是小颗粒时就会发生这种情况)。
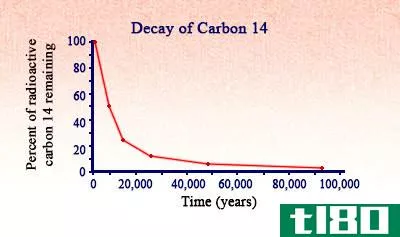
铀有六种同位素,范围从U-233到U-238。所以它们有141到146个中子,但大多数常见的同位素是U-238和U-235。众所周知,铀是一种放射性金属。当它衰变时,它会释放出α粒子,铀的放射性非常缓慢。所以U-238的半衰期约为44.7亿年,U-235的半衰期约为740万年。铀自然存在于地球上的矿石中,但浓度很小,它被提取并转化为二氧化铀或其他化学形式,以便用于工业。由于铀慢慢衰变,它被用来确定地球的年龄。U-235有能力引发核连锁反应。它是可裂变的。所以当它被中子轰击时,U-235原子核被分成两个更小的原子核,释放出结合能和更多的原子核。由于这种连锁反应,可能会发生爆炸。所以铀被用于核反应堆、核电站和***。
钚
钚的化学符号是钚。它的原子序数是94。钚是锕系元素中的一种反铀放射性元素。它是一种银灰色的固体金属。钚的电子构型为[Rn]5f6 7s2,表现出四种氧化态。钚有六个同素异形体。在室温下,α型是钚最常见和最稳定的同素异形体。它又硬又脆。虽然它是一种金属,但它不是一种好的导热体或导电体。钚与卤素、碳、硅等非金属发生反应,暴露在空气中会迅速氧化,氧化层呈暗灰色。钚的沸点异常高,约为3228°C。熔点为639.4°C,相对较低。在钚同位素中,钚239是裂变同位素。所以这种同位素用于核武器和其他***。它也被用来发电和供热。
| 铀和钚有什么区别?•铀的原子序数为92,钚的原子序数为94。•钚有6个f电子,而铀只有3个。•钚同位素的寿命比铀同位素低得多。•钚可以通过铀人工获得。 |