方形平面配合物与四面体配合物的主要区别在于,方形平面配合物具有四层晶场图,而四面体配合物具有两层晶场图。
晶体场理论是描述原子周围的阴离子电荷产生的静电场导致电子轨道(主要是d和f轨道)断裂的理论。这一理论对于描述过渡金属配合物的性质是非常重要的。我们也可以描述正方形平面和四面体配合物的结构。
目录
1. 概述和主要区别
2. 什么是正方形平面复合物
3. 什么是四面体复合体
4. 并列比较-方形平面与四面体的表格形式的复合物
5. 摘要
什么是平面配合物(square planar complexes)?
Square planar complexes are coordination complexes that have a central metal atom surrounded by four c***tituent atoms in corners of the same square plane. The bond angles of the bonds in this structure are 90°. Transition metals having the electron configuration ending d8 form coordination complexes having this molecular geometry. For example, Rh(I), Ir(I), Pd(II), etc. The coordination number for a square planar complex is four.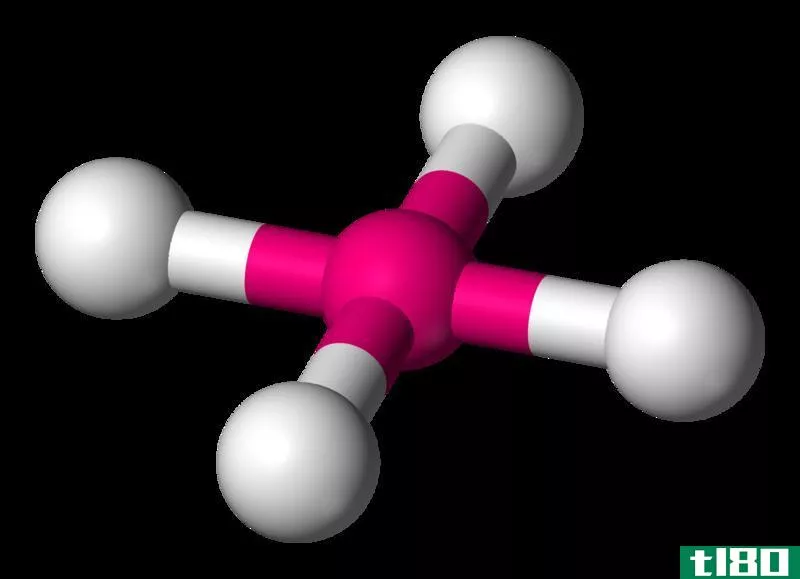
我们可以用晶体场理论来描述这些配合物的结构。根据这个理论,一个正方形的平面复合物有一个四层晶体场图。这个四层分裂被命名为D4h,由此产生的四个能级被命名为dx2-y2,dxy,dz2和[dxz,dyz]。此外,正方形平面几何和四面体几何之间有着特殊的关系。我们可以通过展平四面体来将四面体几何体转换为正方形平面几何体。这种转化为四面体配合物的异构化提供了途径。
什么是四面体配合物(tetrahedral complexes)?
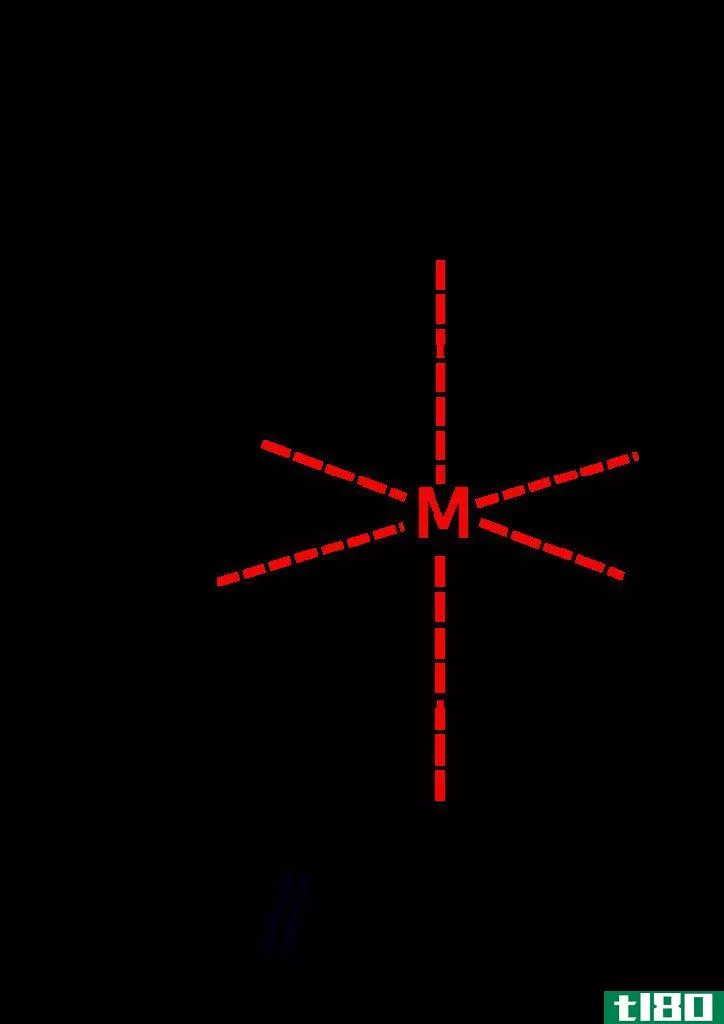
Tetrahedral complexes are coordination complexes that have a central metal atom surrounded by four c***tituent atoms in corners of a tetrahedron. The bond angles of the bonds in this structure are about 109.5°. However, if the c***tituents are different from each other, the bond angles vary. There are two types of transition metals that can form this type of complex: metals having d0 configuration and d10 configuration.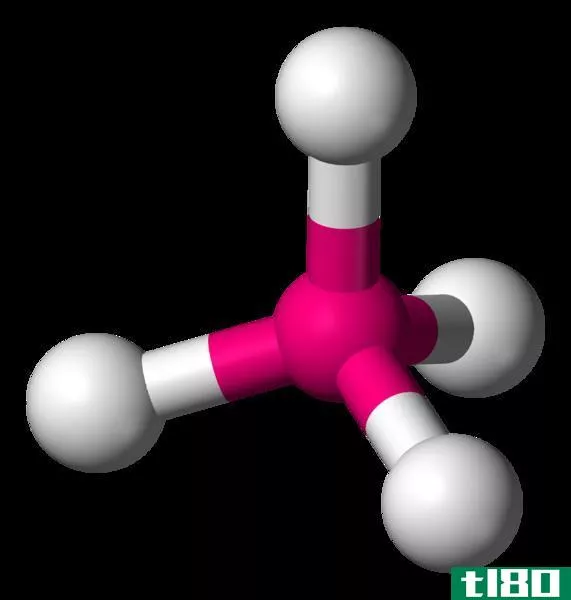
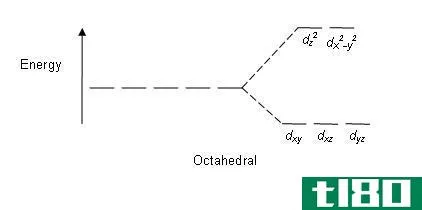
此外,根据晶体场理论,四面体配合物具有双层晶场图。这张图的两个能级包括两组轨道:一个能级上的dxy,dxz,dyz,另一个能级上的dx2-y2,dz2。
正方形平面(square planar)和四面体配合物(tetrahedral complexes)的区别
晶体场理论对于描述过渡金属配合物的性质以及正方形平面和四面体配合物的结构都是非常重要的。方形平面配合物与四面体配合物的主要区别在于,方形平面配合物具有四层晶场图,而四面体配合物具有两层晶场图。
此外,电子构型以d8构型结束的过渡金属倾向于形成方形平面配合物,而d0构型和d10构型的过渡金属倾向于形成四面体配合物。
下面的信息图显示了更多关于方形平面和四面体复合体之间差异的比较。
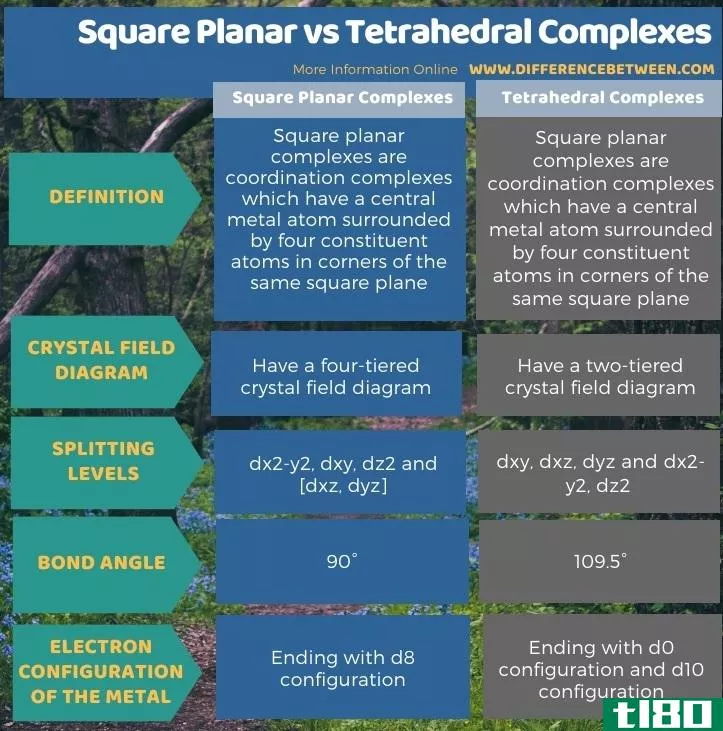
总结 - 正方形平面(square planar) vs. 四面体配合物(tetrahedral complexes)
晶体场理论是描述过渡金属配合物性质的重要理论。我们也可以描述正方形平面和四面体配合物的结构。方形平面配合物与四面体配合物的主要区别在于,方形平面配合物具有四层晶场图,而四面体配合物具有两层晶场图。
引用
1莫特,瓦莱丽。“化学导论”,Lumen,这里有。“配位化合物中的键合:晶体场理论”,无限化学,管腔,可在这里查阅。“水晶场理论”,歌词,这里有。
2“配位化合物中的键合:晶体场理论”,无限化学,流明,
三。“水晶场理论”,歌词,