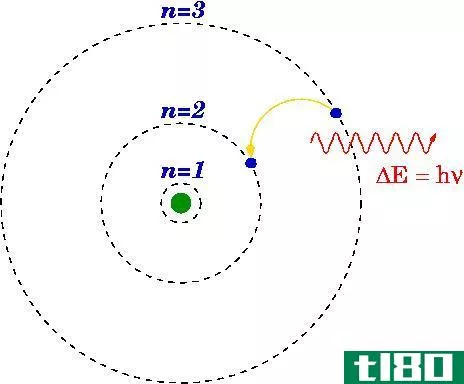
磁性量子数和自旋量子数的关键区别在于,磁量子数在区分子壳层内可用的轨道时很有用,而自旋量子数则描述了轨道的能量、形状和方向。
量子数是描述原子中电子的唯一量子态的一组值。具体的量子数有四种:主量子数、角量子数、磁量子数和自旋量子数。
目录
1. 概述和主要区别
2. 什么是磁量子数
3. 什么是自旋量子数
4. 并列比较-磁性量子数与自旋量子数的表格形式
5. 摘要
什么是磁量子数(magnetic quantum number)?
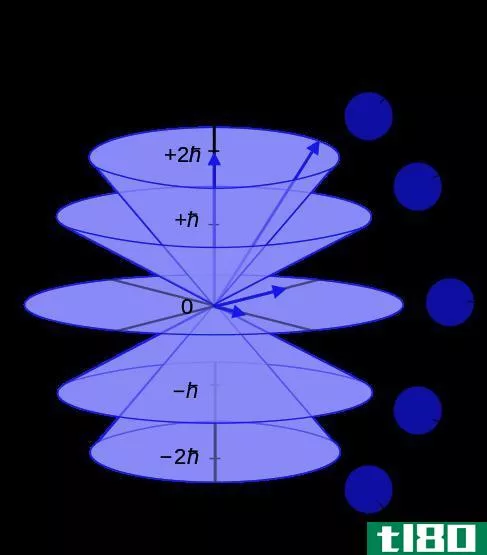
磁量子数区分了子壳层中可用的轨道。这个值的符号是mi。根据它的定义,这个量子数表明每个特定子壳层中的电子都有角量子数,范围从-l到+l加零。因此,s,p,d和f子壳层包含不同数量的轨道。下表显示了每个子壳层中存在的轨道数。
| 子外壳 | 磁量子数的值 | 轨道数 |
| s | mi=0 | 1 |
| p | mi=-1,0,+1 | 三 |
| d | mi=-2,-1,0,+1,+2 | 5 |
| f | mi=-3,-2,-1,0,+1,+2,+3 | 7 |
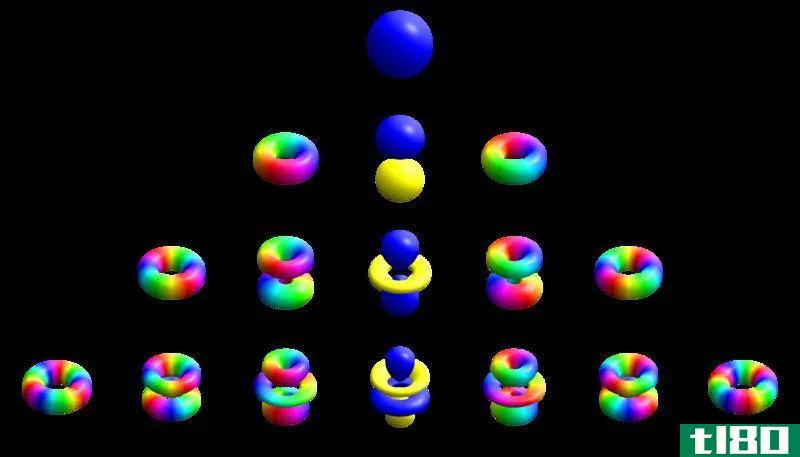
磁性量子数决定了由于外加磁场而发生的轨道能量转移。我们称这种效应为“塞曼效应”。实际磁矩由两个因素产生:电子角动量和电子自旋,这两个因素由磁量子数描述。
什么是自旋量子数(spin quantum number)?
自旋量子数描述了轨道的能量、形状和方向。此值的符号为“s”。自旋量子数是原子固有角动量的一个参数。电子在轨道上的自旋角动量为s=1/2。
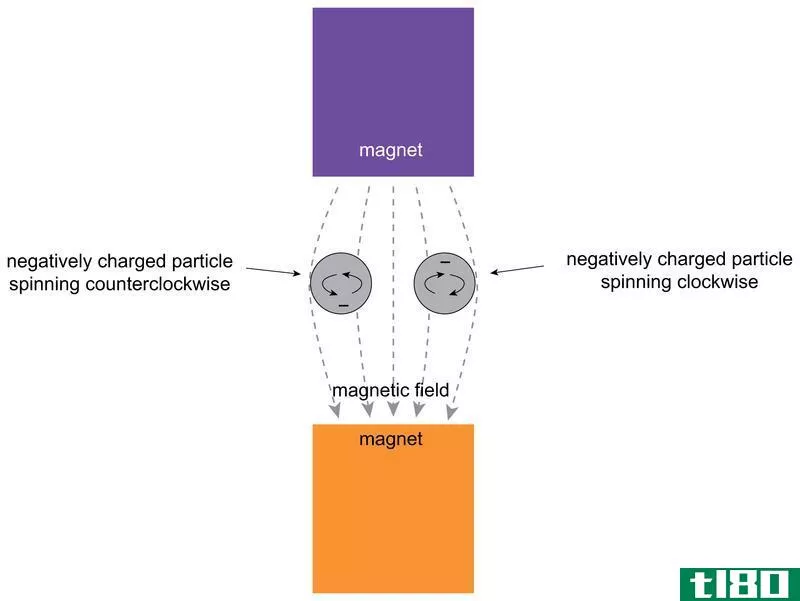
图02:外部磁场对电子的影响
一个轨道可以包含一对电子;因此,这两个电子有s=-1/2和s=+1/2的自旋量子数。它指的是电子的“自旋向上”和“自旋向下”的方向。量子数表示原子中某一特定电子的量子态。此外,我们还可以给出一个“总自旋量子数”(S),它耦合了某些特定原子的几个未成对电子的自旋。
磁量子数(magnetic quantum number)和自旋量子数(spin quantum number)的区别
量子数是描述原子中电子的唯一量子态的一组值。磁性量子数和自旋量子数的关键区别在于,磁量子数在区分子壳层内可用的轨道时很有用,而自旋量子数则描述了轨道的能量、形状和方向。磁量子数的值表示为–l、0和+l。该值的符号为mi。但是,自旋量子数是-1/2和+1/2。此值的符号为“s”。
此外,磁量子数和自旋量子数的另一个区别是,磁量子数描述了由于外加磁场而发生的轨道能量转移,而自旋量子数描述的是原子的固有角动量。

总结 - 磁量子数(magnetic quantum number) vs. 自旋量子数(spin quantum number)
量子数是描述原子中电子的唯一量子态的一组值。磁性量子数和自旋量子数的关键区别在于,磁量子数在区分子壳层内可用的轨道时很有用,而自旋量子数则描述了轨道的能量、形状和方向。
引用
1“原子的量子数”,化学图书馆,图书馆,2019年9月27日,可在这里查阅。“磁性量子数”,维基百科,维基媒体基金会,2019年11月16日,可在这里查阅。“自旋量子数”,维基百科,维基媒体基金会,2019年9月1日,可在这里查阅。赫尔曼斯汀,安妮·玛丽。“自旋量子数定义”,ThoughtCo,2018年12月7日,可在这里查阅。
2“磁性量子数”,维基百科,维基媒体基金会,2019年11月16日,
三。“自旋量子数”,维基百科,维基媒体基金会,2019年9月1日,
4赫尔曼斯汀,安妮·玛丽。“自旋量子数定义”,ThoughtCo,2018年12月7日,