第1组元素和第2组元素的关键区别在于,所有第1组元素的最外层轨道上都有不成对的电子,而第2组元素的最外层轨道上都有成对电子。
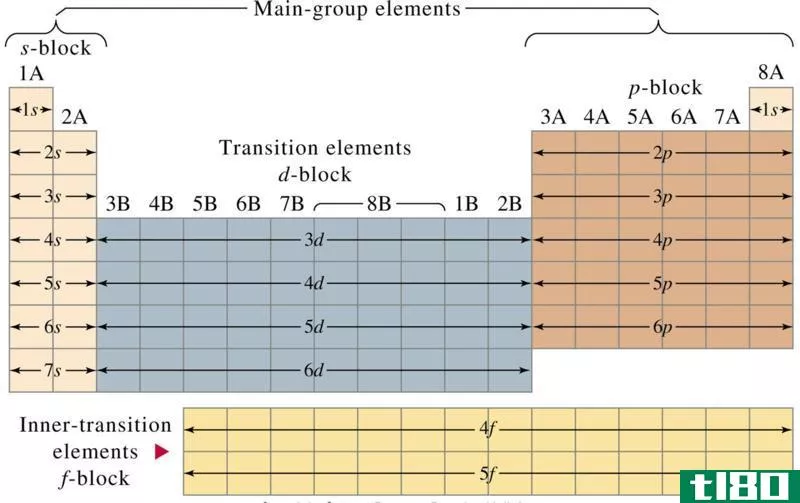
周期表的第1组和第2组包含s块元素。这意味着,这些元素的最外层电子在s轨道上。第1组和第2组的区别取决于它们最外层轨道上的电子数。一个s轨道只能包含两个电子,因为这个轨道的磁量子数是0。
目录
1. 概述和主要区别
2. 什么是Group1元素
3. 什么是第二组元素
4. 并列比较——第1组与第2组元素的表格形式
5. 摘要
什么是第1组元素(group 1 elements)?
第1族元素是在s轨道最外层有一个不成对电子的化学元素。它是周期表s块的第一列。它含有氢和碱金属。第1组成员如下:
- 氢(H)
- 锂(Li)
- 钠(Na)
- 钾(K)
- Rhubidium(Rh)
- 铯(Cs)
- 弗朗(法国)
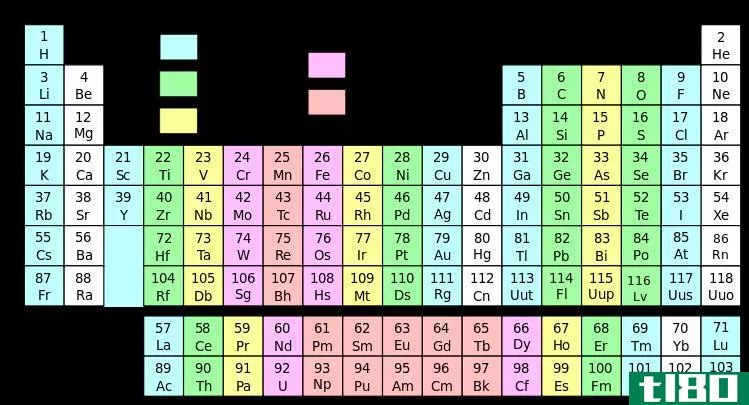
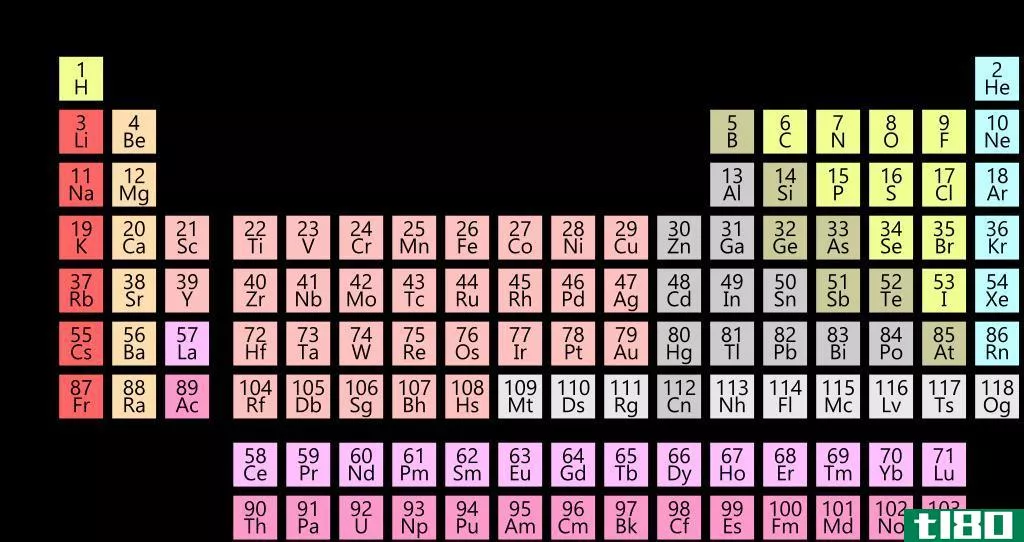
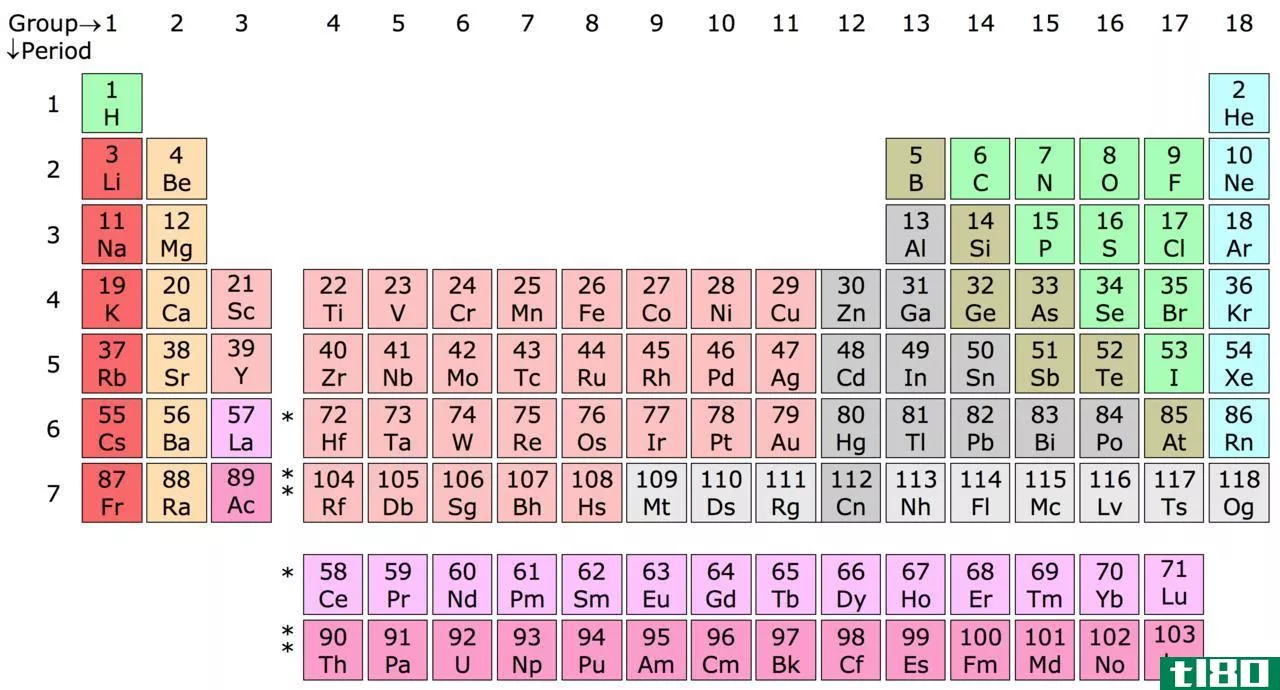
图01:不同颜色组的元素周期表
虽然氢是由于它的电子结构而属于这一类,但它具有不同于碱金属的特性。例如,氢以气体的形式存在,而这一组中的其他元素是金属。这些金属都有光泽,反应性强,非常柔软(我们可以用一把简单的刀很容易地切割它们)。
一般来说,1族元素具有低密度、低熔点、低沸点和体心立方晶体结构。此外,它们有不同的火焰颜色,所以我们可以很容易地将样品暴露在本生灯下加以区分。当进入碱金属组时,会有如下所列的周期性变化。
- 原子尺寸增大
- 熔点和沸点降低是因为形成强键的能力降低了(当原子变大时,形成的键变弱)。
- 密度增加。
- 第一电离能降低是因为在大原子中,最外层的电子束缚得很松,很容易被移除。
- 电负性
- 反应性降低。
- 碱金属的电子亲和力比其他元素低。
什么是第2组元素(group 2 elements)?
第2族元素是在s轨道上有最外层电子对的化学元素。因此,它们的价电子以ns2的形式存在。此外,该组是s块的第二列。我们把它们命名为碱土金属。该小组成员如下:
- 铍(Be)
- 镁(Mg)
- 钙(Ca)
- 锶(Sr)
- 钡(Ba)
- 镭(Ra)
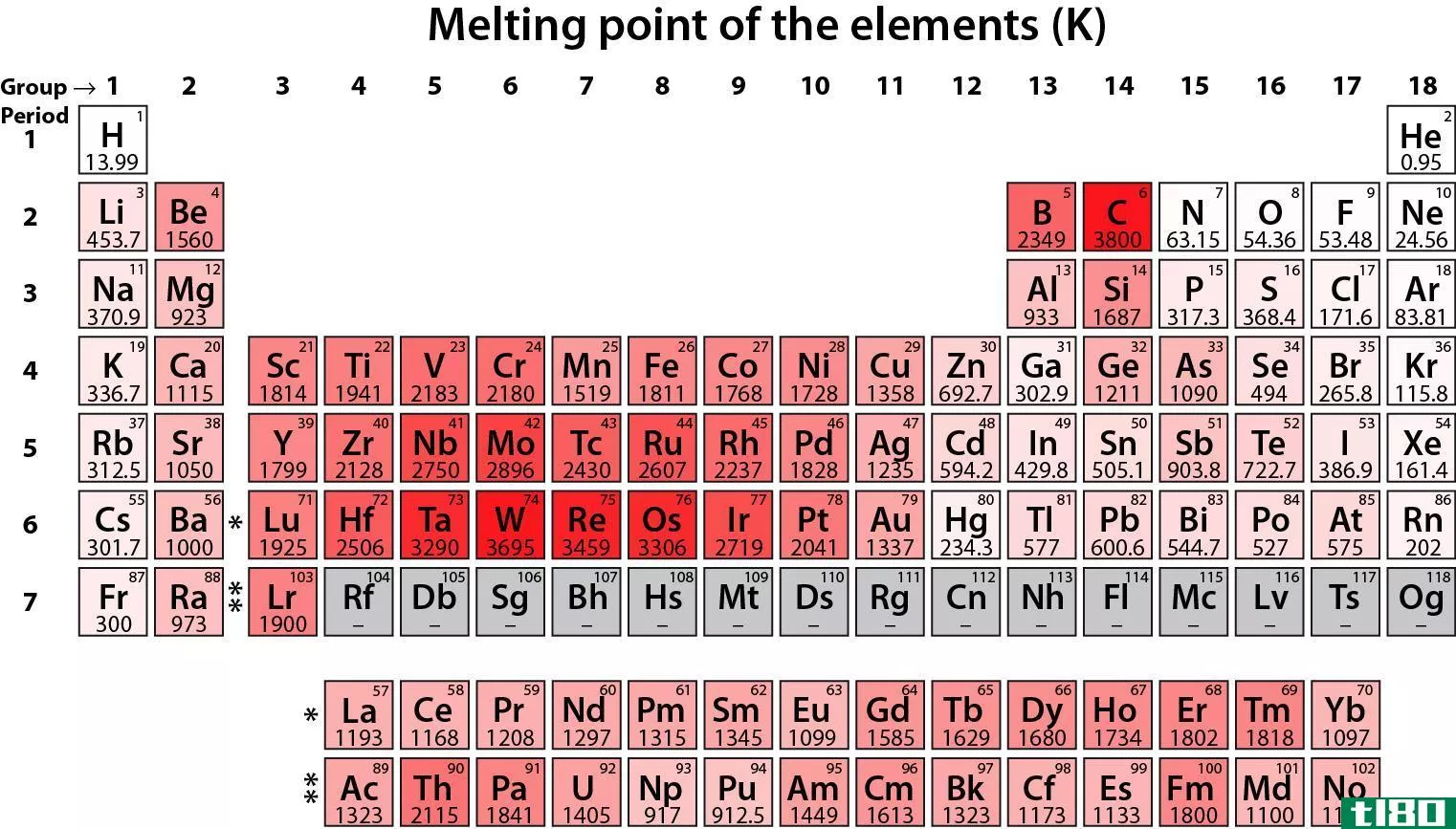
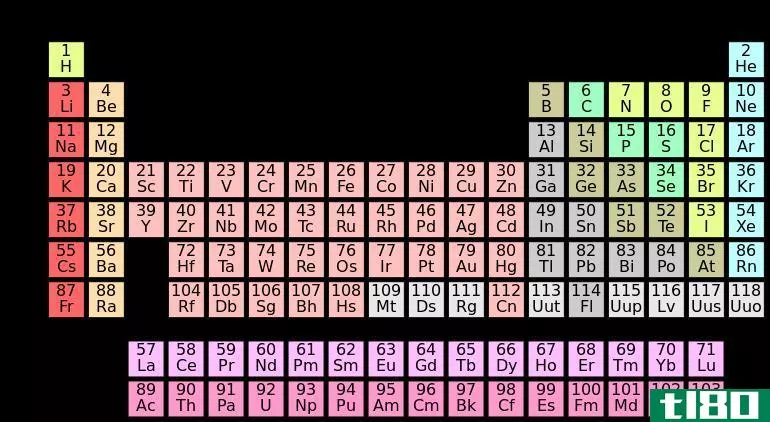
图02:元素熔点
这些金属元素倾向于通过移除两个最外层的s电子来稳定它们的电子组态,从而获得稀有气体电子组态。因此,这些元素倾向于形成+2阳离子。与这些活性元素相比,第1组的活性元素较少。此外,与第1族元素相比,这些元素的熔点更高,其氢氧化物的碱性相对较低。
第1组(group 1)和第2组元素(group 2 elements)的区别
第1组和第2组的区别取决于它们最外层轨道上的电子数。第1组元素和第2组元素的关键区别在于,所有第1组元素的最外层轨道上都有不成对的电子,而第2组元素的最外层轨道上都有成对电子。
下面的信息图显示了关于第1组和第2组元素之间差异的更多比较。
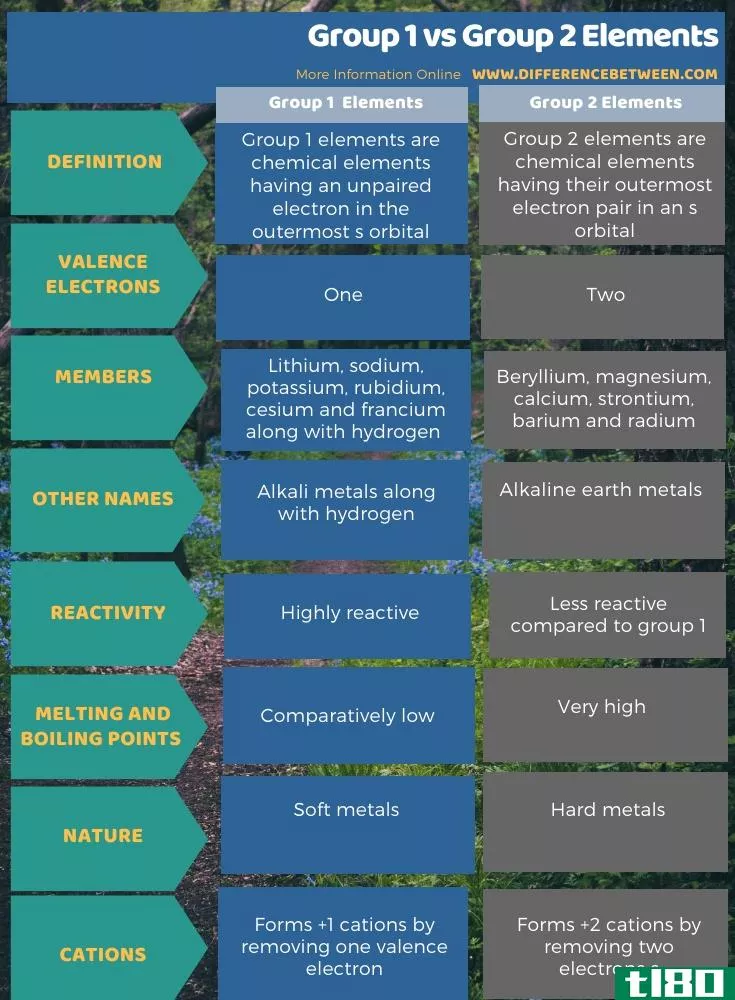
总结 - 第1组(group 1) vs. 第2组元素(group 2 elements)
第1组和第2组的区别取决于它们最外层轨道上的电子数。第1组元素和第2组元素的关键区别在于,所有第1组元素的最外层轨道上都有不成对的电子,而第2组元素的最外层轨道上都有成对电子。
引用
1.“第1组:氢和碱金属。”化学歌词,歌词,2019年6月23日,可在此处查阅。赫尔曼斯汀,安妮·玛丽。“元素群周期表”,ThoughtCo,2019年11月11日,可在这里查阅。
2赫尔曼斯汀,安妮·玛丽。“元素群周期表”,ThoughtCo,2019年11月11日,