可溶盐和不溶盐的关键区别在于,可溶盐在室温下能溶于水,而不溶盐在室温下不能溶于水。
盐是酸和碱反应形成的任何化合物。因此,盐本质上包含一个阴离子(来自酸)和一个阳离子(来自碱)。根据它们在室温下的水溶性,我们可以将盐化合物分为两类。它们是可溶和不溶的盐。盐的溶解度取决于它们与水分子的相互作用类型。
目录
1. 概述和主要区别
2. 什么是可溶盐
3. 什么是不溶盐
4. 并列比较-表格形式的可溶盐和不溶盐
5. 摘要
什么是可溶性盐(soluble salts)?
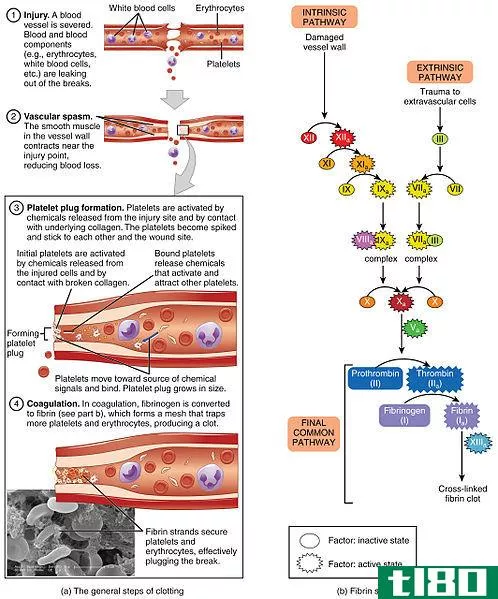
可溶盐是在室温下可溶于水的盐化合物。这些盐类化合物溶于水,因为它们能与水分子形成分子间的吸引力。水分子是极性的。因此,水是极性溶剂,极性盐能溶于水。

图01:氯化钠是可溶盐
由于盐是离子化合物,它们溶于水,因为水分子会吸引化合物中的离子,使它们彼此分离,从而导致盐的溶解。在这里,盐的溶解在水中形成离子物种,这使得新形成的水溶液具有很高的导电性。溶解在水中的离子能通过它传导电。可溶盐的一个例子是食盐或氯化钠。食盐的水溶液含有钠离子和氯离子。
什么是不溶性盐(insoluble salts)?
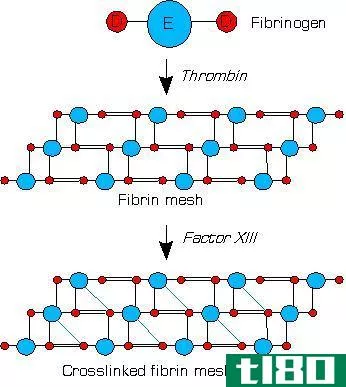
不溶盐是在室温下不溶于水的盐化合物。它们不溶于水,因为水分子不能吸引盐化合物中的离子。因此,水分子与不溶性盐化合物之间没有分子间的相互作用。

图02:氯化银沉淀在水中
此外,不溶性盐是非极性化合物。与可溶盐不同,不溶性盐与水的混合不会使溶液导电,因为盐不会分离成离子。不溶性盐的一个很好的例子是氯化银(AgCl)。
可溶的(soluble)和不溶性盐(insoluble salts)的区别
根据其水溶性,我们可以把盐化合物分为两类。它们是可溶和不溶的盐。可溶盐和不溶盐的关键区别在于,可溶盐在室温下能溶于水,而不溶盐在室温下不能溶于水。此外,可溶盐是极性的,这就是为什么它们能溶于水,水是一种极性溶剂。相反,不溶性盐是非极性的。所以,这是可溶盐和不溶盐的另一个显著区别。
除此之外,水分子可与可溶盐离子形成分子间吸引,但不溶性盐与水之间不存在分子间相互作用。此外,可溶盐在水中的溶解使水溶液具有很高的导电性,因为溶解在水中的离子可以通过水进行导电。与可溶盐不同,将不溶盐与水混合不会使水导电。氯化钠是可溶盐的一个例子,而氯化银是不溶盐的一个例子。

总结 - 可溶的(soluble) vs. 不溶性盐(insoluble salts)
根据其水溶性,我们可以把盐化合物分为两类。它们是可溶和不溶的盐。可溶盐和不溶盐的关键区别在于,可溶盐在室温下能溶于水,而不溶盐在室温下不能溶于水。此外,可溶盐是极性的,这就是为什么它们能溶于水,水是一种极性溶剂。相反,不溶性盐是非极性的。
引用
1“不溶性盐。”化学剧本,歌词,2019年6月5日,可在这里查阅。“不溶性盐(沉淀物)的定义。”Cehmicool字典,可在这里查阅。“不溶盐。”盐三脚架,这里有。
2“不溶性盐(沉淀物)的定义。”Cehmicool字典,
三。“不溶盐”盐三脚架,