自电离和自质子分解的关键区别在于,自电离是一种化学物质的中性状态转化为电离状态,而自电离是两种相同化学物质之间质子的转移,形成电离形式。
自电离和自质子分解两个术语描述了形成电离物质的两种方法,即阳离子和阴离子。这些都是自发反应,电离发生时没有外界因素的影响。
目录
1. 概述和主要区别
2. 什么是自电离
3. 什么是自溶
4. 并列比较-自电离与自分解的表格形式
5. 摘要
什么是自电离(autoionization)?
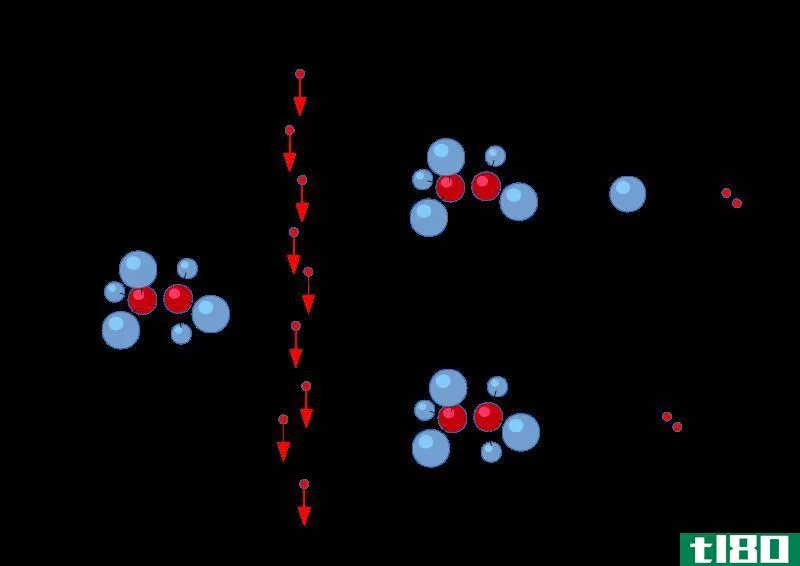
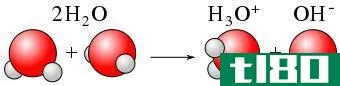
自电离是将化学物质的中性态转变为电离态的过程。这个术语通常描述水分子的电离。因此,我们可以称之为水的自电离或水的自解离。在这里,一个水分子去质子化形成一个氢离子,OH-和一个氢离子,H+(一个质子)。在这里,脱质子化立即质子化另一个水分子,并导致形成一个氢离子(H3O+)。所以,这个过程是水的两性性质的一个很好的例子。

图01:水分子的自电离
此外,这个过程描述了水的两性性质。两性性是指水既能作酸又能作碱,因为自电离既能形成质子又能形成氢氧化物离子,使水具有一定程度上中和酸碱的能力;例如,氢离子或H3O+离子能中和弱碱,氢氧化物离子能中和弱酸。
什么是自溶(autoprotolysis)?
自质子分解是质子在同一化学物质之间转移以形成离子化物质的过程。在这里,两个相同的分子中的一个充当了布朗斯特德酸,它释放出一个质子。另一个分子可以接受这个质子。因此,另一个分子充当了布朗斯特德碱。水的自电离就是自分解的一个例子。此外,这个术语不同于自旋分解,因为自旋分解描述的是酸对化学键的裂解。
其他一些经过自分解的化合物的例子包括氨和乙酸;
氨的自动分解:
2NH3⇌NH2–+NH4+
醋酸的自分解作用:
2CH3COOH⇌CH3COOH–+CH3COOH2+
自电离(autoionization)和自溶(autoprotolysis)的区别
自电离和自分解都是自发反应。自电离和自质子分解的关键区别在于,自电离是一种化学物质的中性状态转化为电离状态,而自电离是两种相同化学物质之间质子的转移,形成电离形式。自电离的一个例子是水,而水、氨、乙酸是一些自分解的例子。
此外,在自电离过程中(也称为水的自电离或自解离),水分子脱质子形成氢氧化物离子OH-和氢离子H+(质子),而在自转解过程中,两个完全相同的分子中的一个作为Brønsted酸,它释放出一个质子,这个质子被作为Brønsted碱的另一个分子接受。此外,水的自电离过程描述了水的两性性质(它可以中和弱酸和弱碱)。另一方面,自交解作用描述了水、乙酸和氨等化合物的两性性质。
下面的信息图总结了自电离和自分解之间的区别。
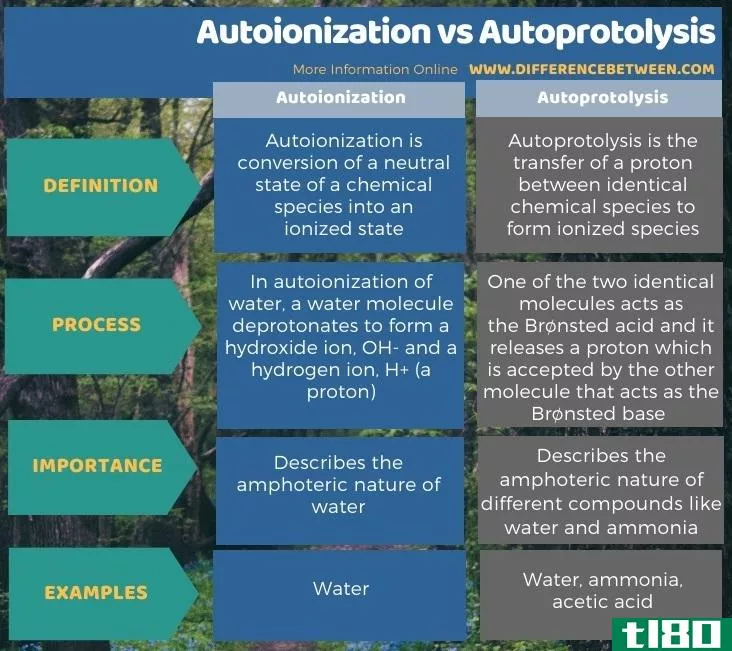
总结 - 自电离(autoionization) vs. 自溶(autoprotolysis)
自电离和自分解都是自发反应。自电离和自质子分解的关键区别在于,自电离是一种化学物质的中性状态转化为电离状态,而自电离是两种相同化学物质之间质子的转移,形成电离形式。
引用
1“水的自电离”,维基百科,维基媒体基金会,2019年6月3日,可在这里查阅。“自动分解”,维基百科,维基媒体基金会,2019年9月24日,可在这里查阅。“水自电离”,化学剧本,歌词,2019年6月5日,可在这里查阅。
2“自动分解”,维基百科,维基媒体基金会,2019年9月24日,
三。“水自电离”,化学剧本,歌词,2019年6月5日,