原电池和浓差电池的关键区别在于,原电池可能有或可能没有具有相同成分的两个半电池,而浓度电池有两个具有相同成分的半电池。
原电池和浓电池都是电化学电池。电化学电池是一种利用化学反应产生电能或利用电使化学反应发生的装置。
目录
1. 概述和主要区别
2. 什么是原电池
3. 什么是浓缩池
4. 并列比较-原电池与浓度电池的表格形式
5. 摘要
什么是原电池(a galvanic cell)?
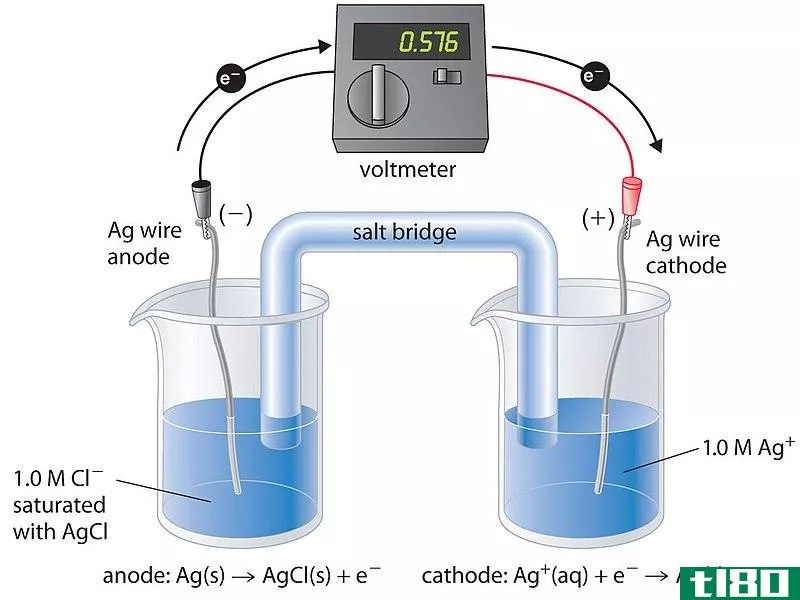
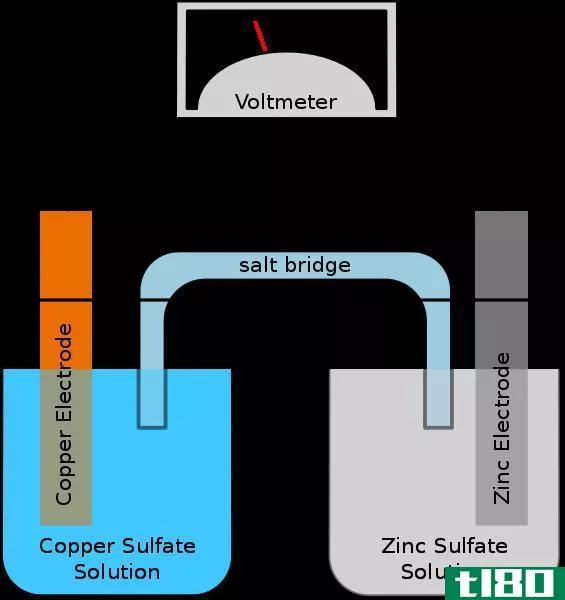
原电池是一种利用自发氧化还原反应产生电能的电化学电池。这种电池的同义词是伏打电池。细胞包含两个半细胞,可以是相同成分,也可以是不同成分。每个半电池包含一个电极和一个电解液。电极应浸入电解溶液中。有时这些电解液是完全分离的,但有时它们只被多孔屏障隔开。当电解质完全分离时,我们需要使用盐桥来维持两种电解质之间的离子运动。
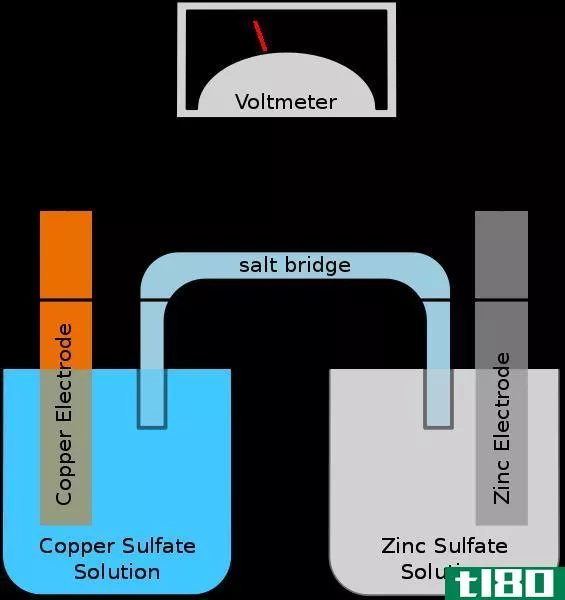
图01:简单原电池
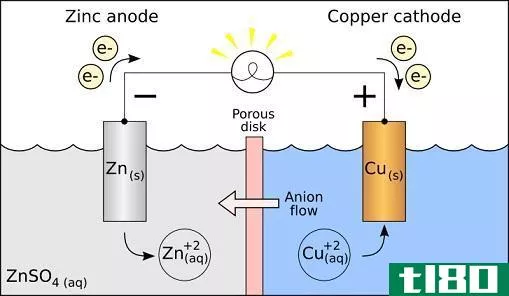
在制备这种电池时,我们需要考虑电极和电解质是否自发。通过计算每个半电池的电极电位,我们可以从理论上找到它。然而,一半的电池应该表现出氧化,而另一半电池应该表现出还原反应。氧化发生在阳极,而还原发生在阴极。由于原电池利用自发氧化还原反应中释放的能量来发电,因此原电池作为电能的来源非常重要。它们产生直流电。
什么是浓缩池(a concentration cell)?
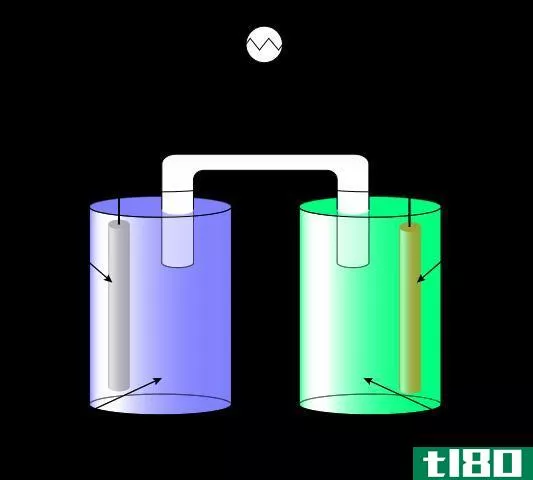
浓差电池是一种原电池,其中两个半电池的成分相似。因此,我们说这两个半单元是等价的。它们只是浓度不同。这个电池产生的电压很小,因为这个电池趋于平衡状态。当两个半细胞的浓度相等时,平衡就来了。
浓缩池通过还原系统的热力学自由能产生电能。由于半细胞的组成相似,所以发生相同的反应,但方向相反。这个过程增加了低浓度细胞的浓度,降低了高浓度细胞的浓度。当电流流动时,热能就产生了。细胞吸收这种能量作为热量。浓缩池有两种类型,如下所示:
- 电解液浓度电池-电极由相同的物质组成,半电池含有相同的电解质,浓度不同
- 电极浓度电池-将两个不同浓度的电极(相同物质)浸入同一电解液中
原电池(galvanic cell)和浓缩池(concentration cell)的区别
原电池是一种利用自发氧化还原反应产生电能的电化学电池。另一方面,浓缩池是一种原电池,其中两个半电池的成分相似。因此,原电池和浓差电池的关键区别在于,原电池可能有或可能没有具有相同成分的两个半电池,而浓度电池有两个具有相同成分的半电池。
此外,原电池的电极可以由相同的物质制成,也可以由不同的物质制成,而浓度电池的电极则可以由相同浓度或不同浓度的物质制成。除此之外,原电池在两个半电池中具有相同或不同的电解质,而浓度电池具有相同浓度或不同浓度的相同电解质。
下面的信息图总结了原电池和浓缩电池之间的区别。

总结 - 原电池(galvanic cell) vs. 浓缩池(concentration cell)
原电池是一种利用自发氧化还原反应产生电能的电化学电池。浓差电池是一种原电池,其中两个半电池的成分相似。因此,原电池和浓差电池的关键区别在于,原电池可能有或可能没有具有相同成分的两个半电池,而浓度电池有两个具有相同成分的半电池。
引用
1赫尔曼斯汀,安妮·玛丽。“电化学电池”,ThoughtCo,2019年1月26日,可在这里查阅。