氧化数和电荷之间的关键区别在于,我们可以根据原子除去或获得的电子数来确定原子的氧化数,而电荷是根据原子中电子和质子的总数来确定的。
元素周期表中的不同元素表现出不同的化学和物理特性。当它们结合形成分子时,不同的元素以不同的比例与其他元素结合。在元素之间的大量变化中,最简单和重要的参数是它们的电荷和氧化数。一个元素的电荷和氧化数有助于确定元素周期表中该元素属于哪一组。最重要的是,它有助于描述元素形成其他分子和配位化合物的能力,从而有助于确定它们的经验公式。
目录
1. 概述和主要区别
2. 氧化数是多少
3. 什么是电荷
4. 并列比较-氧化数与电荷的表格形式
5. 摘要
什么是氧化值(oxidation number)?
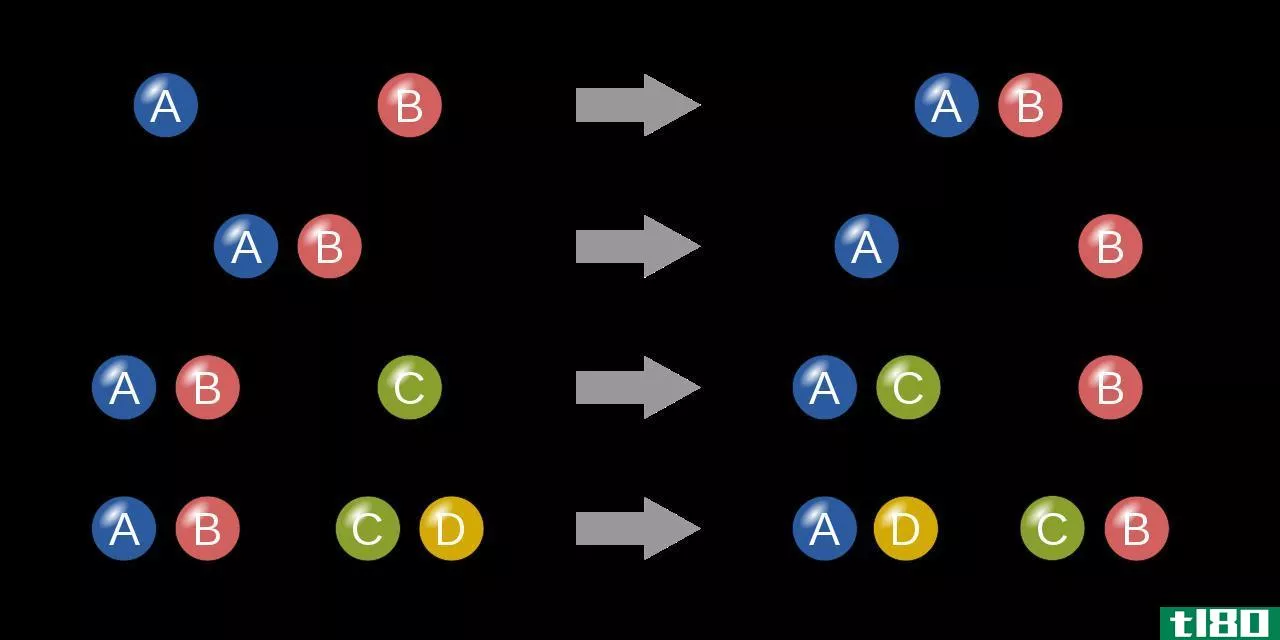
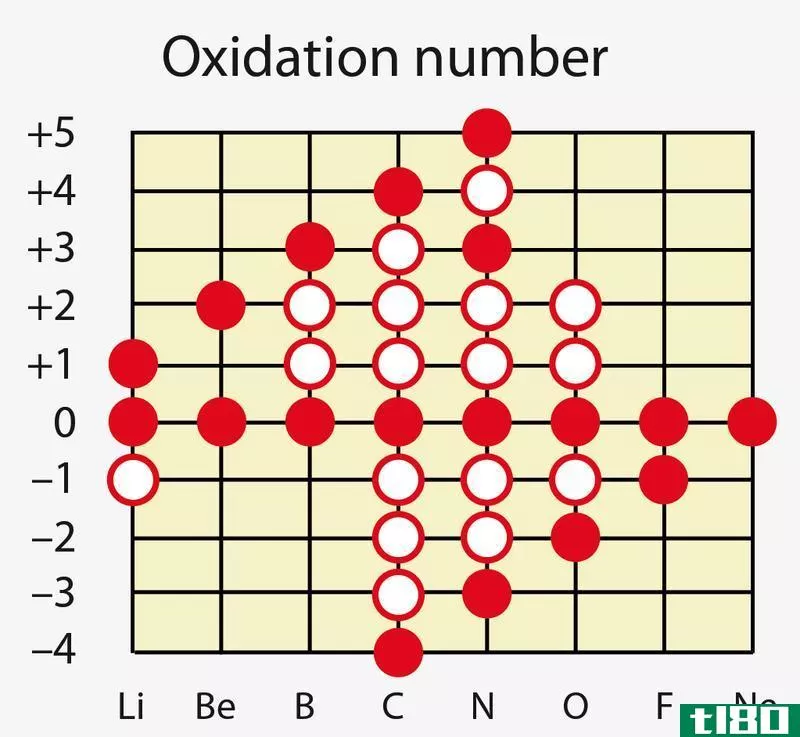
氧化数是配位化合物中心原子的特征。它是一种配位化合物的中心原子的电荷,当这个原子周围的所有键都是离子键时。因此,电荷和氧化数有时相似,有时不同。例如,简单的s块和p块元素的氧化数与其电荷相同。此外,多原子离子的氧化数与电荷相同。然而,同一种化学元素可能有不同的氧化数,这取决于它周围的其他原子。在自由元素中,氧化数总是零。此外,过渡金属离子(d块)和元素具有不同的氧化数。
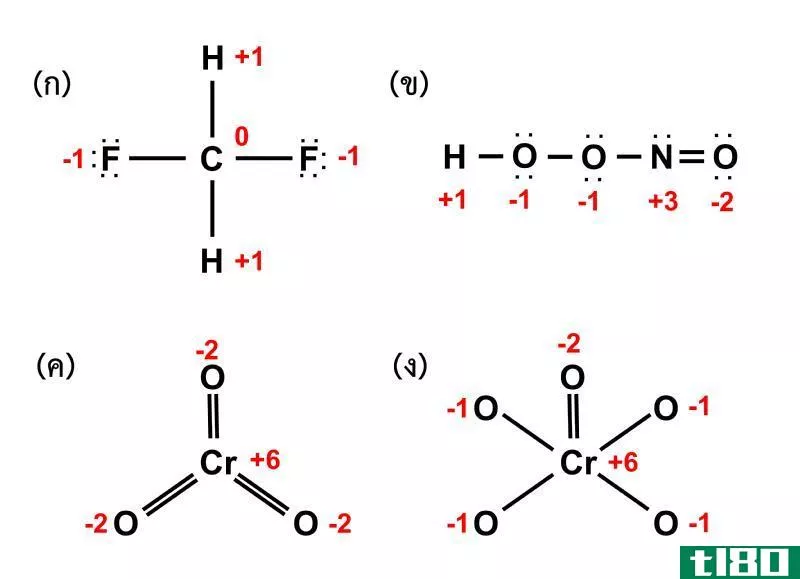
图01:测定化合物中不同元素的氧化数
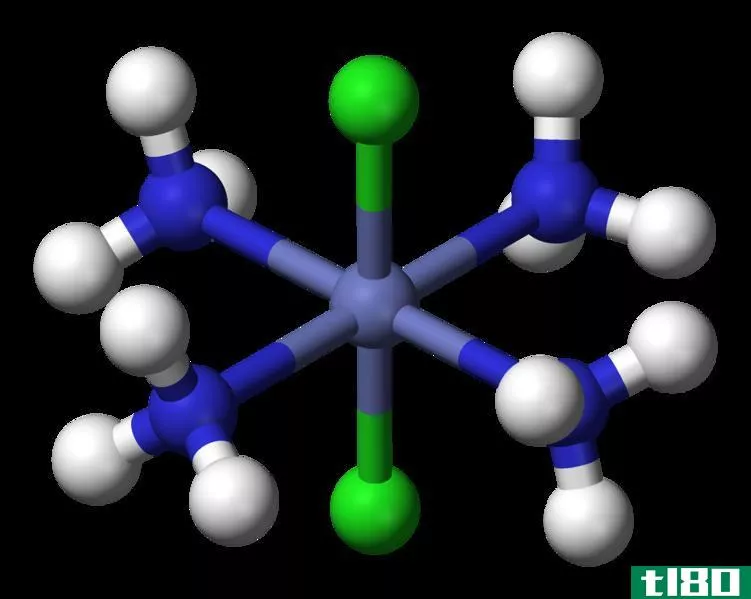
当考虑配位化合物时,中心金属原子应该总是有空位轨道,配位体向其捐赠孤电子对并形成离子键。此外,我们可以用括号内的罗马数来表示中心金属原子的氧化数。例如,如果金属“M”的氧化数是3,那么我们把它写成M(III)。
什么是指控(charge)?
任何原子的电荷为零。当原子除去或获得电子时,它们获得电荷。这是因为,电子是带负电的亚原子粒子,而质子是带正电荷的。原子根据八位元规则除去或获得电子以填充其价壳层。
在一个原子中,质子和电子的数目相等。由于质子带正电荷,电子带负电荷,所以当电子从价壳层中移除时,原子就形成了带正电荷的离子,因为正质子的数量比离子中的电子数要高。
费用的确定
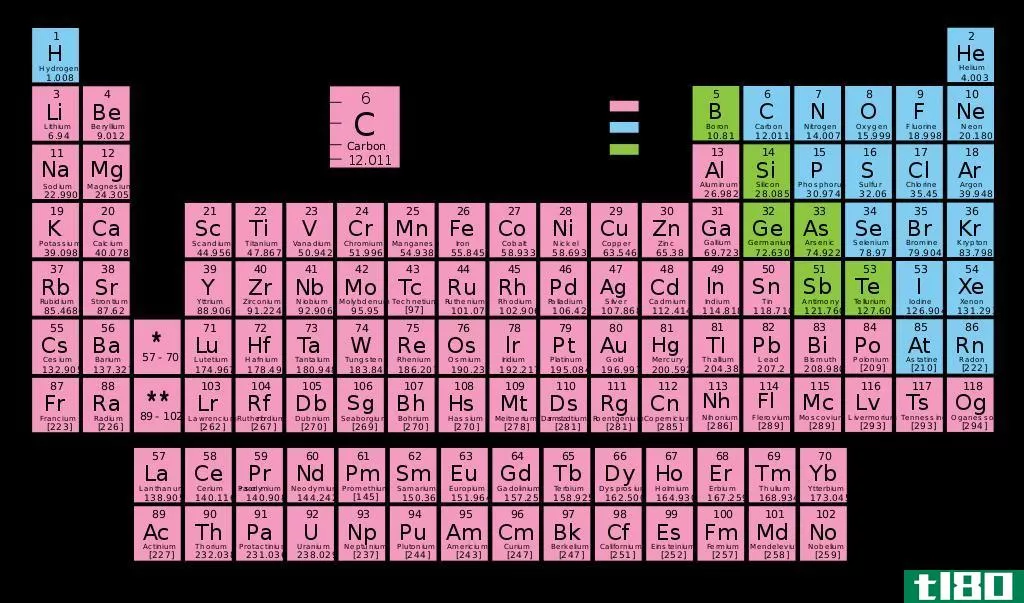
此外,当一个原子的电负性更强时,它可以把其他原子的电子吸引到自己身上。在那里,它们获得的电子比原子核中的质子数量还要多。因此,原子变成负离子。此外,捐赠或抽象的电子数因原子而异。我们可以从元素在周期表中的位置来预测。通常,相同的原子群会形成相同的带电离子,因为它们的价电子数目相同。
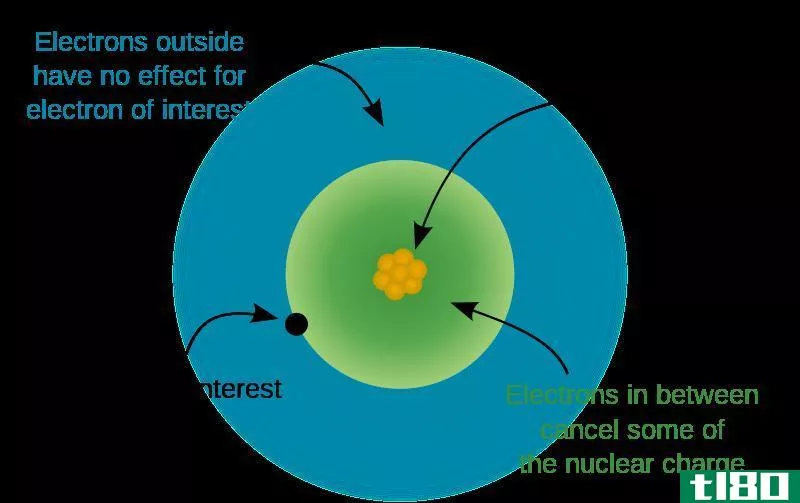
图02:决定电荷的原子结构
基团数也表示价电子的数目;因此,我们可以确定由该基团中的原子形成的离子的电荷。例如,第一族元素形成带有+1电荷的单价离子。第二族元素形成二价正电荷离子。第三组和第四组原子相应地形成+3和+4带电离子。从第五组到第七组,原子生成带负电荷的离子,因为只需获得2或3个电子就可以填充其价电子,而不是发射5、6或7个电子。因此,第五族元素生成-3个带电离子,而第6组元素生成-2个离子,第7组元素生成-1个离子。除了这些简单带电的离子外,还有一些带有NH4+和CO32-等电荷的复杂离子。
氧化值(oxidation number)和指控(charge)的区别
氧化数和电荷是化学中两个相关的术语。然而,氧化数和电荷之间存在一些差异。氧化数和电荷之间的关键区别在于,我们可以根据原子除去或获得的电子数来确定原子的氧化数,而电荷是根据原子中电子和质子的总数来确定的。
此外,同一化学元素的氧化数取决于它周围的原子,而原子的电荷只取决于原子中电子和质子的数量。因此,这是氧化数和电荷之间的另一个重要区别。

总结 - 氧化值(oxidation number) vs. 指控(charge)
电荷和氧化数是两个相关的术语。氧化数和电荷之间的关键区别在于,我们可以根据原子除去或获得的电子数来确定原子的氧化数,而电荷是根据原子中电子和质子的总数来确定的。
引用
1“氧化数。”过渡金属。这里有2个。歌词。“原子”,化学剧本,国家科学基金会,2018年11月26日。此处提供
2歌词。“原子”,化学剧本,国家科学基金会,2018年11月26日。