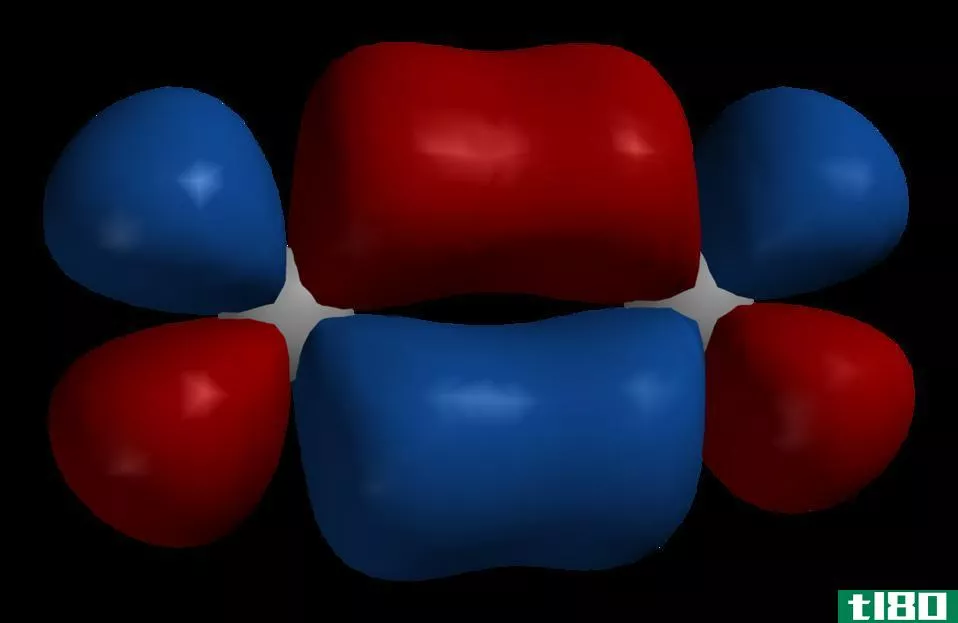
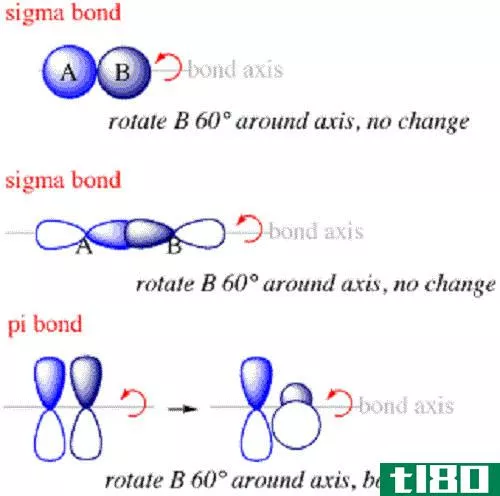
反键和非键的关键区别在于反键轨道增加了分子的能量,而非键轨道不会改变分子的能量。
反键和非键这两个术语都属于分子轨道理论。根据这个理论,这些轨道是由于其他轨道重叠而形成的混合轨道。
目录
1. 概述和主要区别
2. 什么是反键
3. 什么是非键合
4. 并列比较-表格形式的反键与非键合
5. 摘要
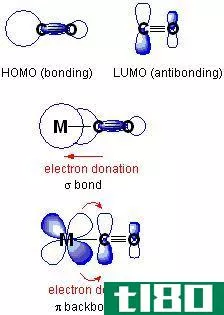
什么是反键合(antibonding)?
反键分子轨道是两个原子核之间区域外含有电子的轨道。反键轨道上的电子会降低分子的稳定性,因为这些电子大部分时间都在原子核之外。因此,与成键分子轨道相比,反键分子轨道的电子密度要小,而反键分子轨道表示键外的电子密度。
反键分子轨道比原子轨道和成键分子轨道具有更高的能量。这是因为这些轨道上的电子对减少两个原子核之间的斥力没有贡献。因此,在反键分子轨道上有电子的化合物的稳定性较低。然而,在稳定的化合物中,反键分子轨道上的电子不存在或更少。此外,反键分子轨道的空间排列并不决定分子的形状或几何形状。
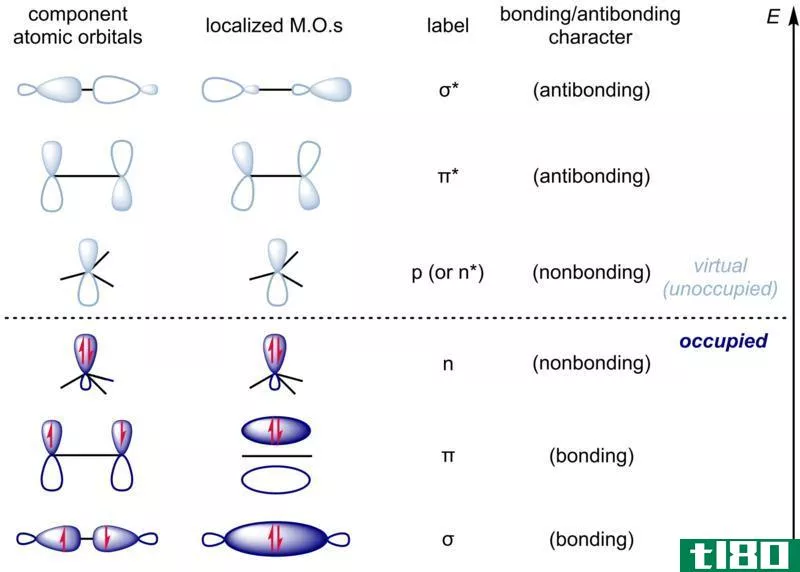
根据上面的分子轨道键合图,分子的轨道密度是相等的。因此,它是一种非常不稳定的分子。因此,He2分子不存在。反键分子轨道表示为σ*。
什么是非键合(nonbonding)?
Nonbonding orbital is the molecular orbital in which addition or removal of electr*** neither increases or decreases the bond order between atoms. We often designate this orbital by “n”. These orbitals resemble the lone electron pairs in Lewis structures.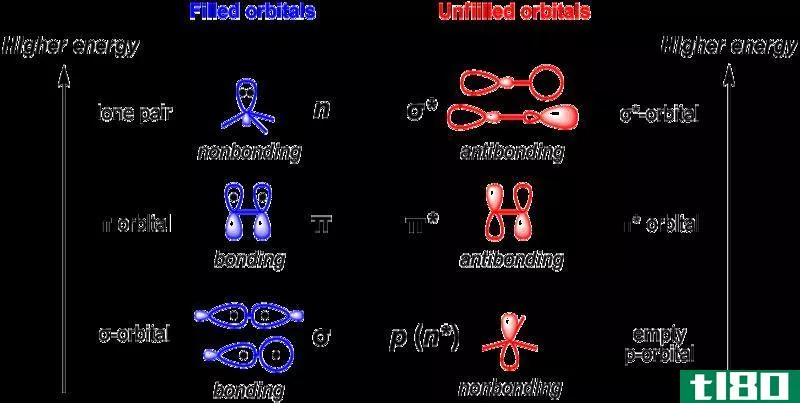
此外,非键轨道的能量介于反键轨道能量和成键轨道之间。
反键合(antibonding)和非键合(nonbonding)的区别
反键轨道和非键轨道是分子轨道。反键和非键的关键区别在于反键轨道增加了分子的能量,而非键轨道不会改变分子的能量。此外,反键轨道的存在会使分子不稳定,而非键轨道对分子的稳定性没有影响。

总结 - 反键合(antibonding) vs. 非键合(nonbonding)
反键轨道和非键轨道是分子轨道。反键和非键的关键区别在于反键轨道增加了分子的能量,而非键轨道不会改变分子的能量。
引用
1赫尔曼斯汀,安妮·玛丽。“反键轨道定义”,ThoughtCo,2019年7月3日,可在这里查阅。