配位数和氧化数的关键区别在于,配位数是附着在配位化合物金属中心的配位体的数目,而氧化数则是中心原子的电荷,如果我们去掉它周围的所有配体和电子对。
在配位化学中,我们遇到了配位数和氧化数这两个术语。在配位化学中,我们研究的是含有金属中心的复杂化合物,这些金属中心被称为配体的化学物质所包围。
目录
1. 概述和主要区别
2. 什么是协调数
3. 氧化数是多少
4. 并列比较-以表格形式列出配位数与氧化数
5. 摘要
什么是协调数(coordination number)?
配位数是配位络合物中连接到金属中心的配位体的数目。因此,我们有时称之为连接性。这些配体可以是原子、离子或分子。通常在配位化合物中可以观察到2到9的配位数,但高配位数的情况非常少见。
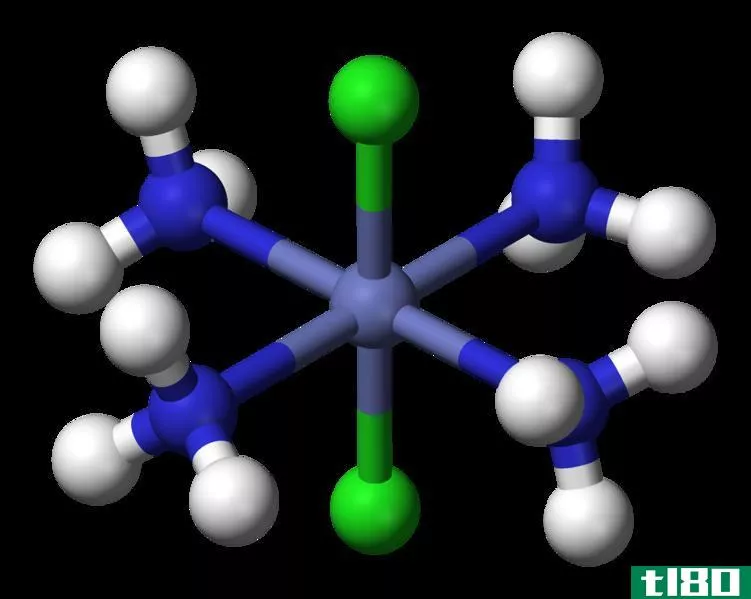
图01:配位数为6的配位化合物
然而,这个数字并不包括围绕金属中心的电子对的数量。例如,[Mo(CN)8]4-是一种以钼为金属中心的配位络合物,配位数为8,因为金属中心上有八个配体。
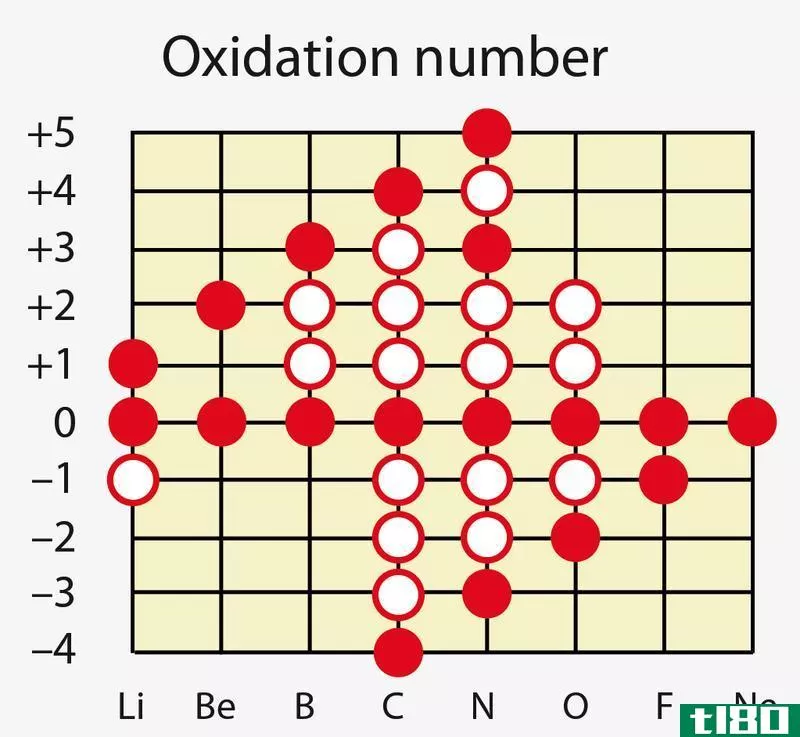
什么是氧化值(oxidation number)?
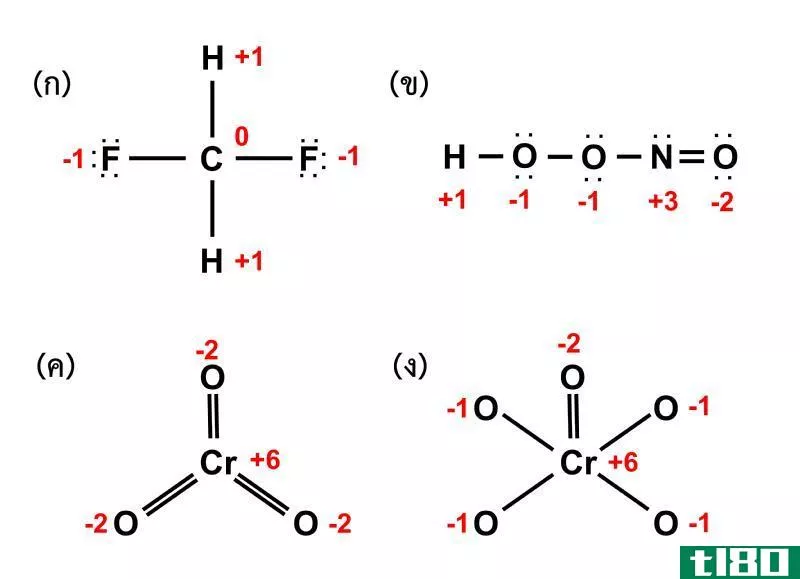
氧化数是中心原子的电荷,如果与原子共享的所有配体和电子对被移除。此外,这一数字适用于过渡金属,因为配合物是通过与过渡金属结合的配体形成的。过渡金属是元素周期表d区第3~12族的化学元素。通常,由于未成对电子的低反应性,它们可以形成几种氧化态。例如,配位络合物[Fe(CN)6]3-中铁(Fe)的氧化数为+3。我们可以通过去除所有带电荷的配体(CN配体)来获得这个值。
总费用为-3
去掉-1×6(因为有六个配体,一个Cn配体有-1电荷)
则Fe的氧化数=-3–(-6)=+3
协调数(coordination number)和氧化值(oxidation number)的区别
配位数和氧化数的关键区别在于,配位数是附着在配位化合物金属中心的配位体的数目,而氧化数则是中心原子的电荷,如果我们去掉它周围的所有配体和电子对。此外,我们给出了整个配位化合物的配位数,但氧化数是针对金属中心的。例如,[Mo(CN)8]4-配合物的配位数为8,而配位配合物[Fe(CN)6]3-中的铁(Fe)的氧化数为+3。
下面的信息图总结了配位数和氧化数之间的区别。

总结 - 协调数(coordination number) vs. 氧化值(oxidation number)
配位数和氧化数是配位化学中两个不同的术语。配位数是配位化合物的金属中心所含配体的数目。相反,氧化数是中心原子的电荷,如果我们去掉它周围的所有配体和电子对。所以,这就是配位数和氧化数的关键区别。
引用
1赫尔曼斯汀,托德。“氧化状态和氧化数之间的差异。”ThoughtCo,2019年7月3日,可在这里查阅。