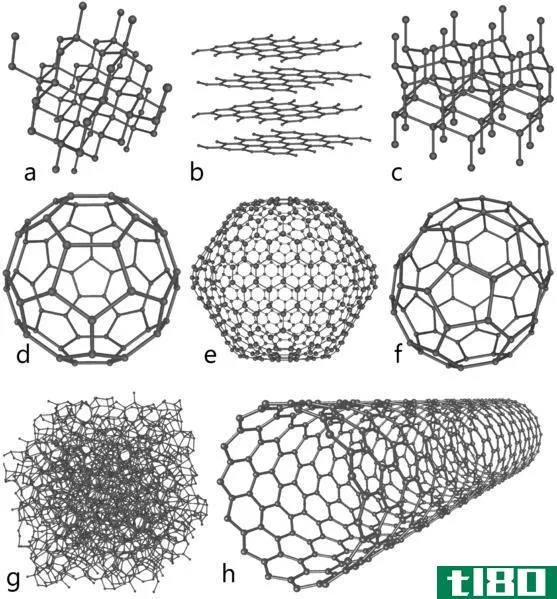
金刚石石墨和富勒烯的关键区别在于金刚石具有金刚石立方晶体结构和石墨具有六角形晶体结构,而富勒烯则以大的球状分子形式存在。
金刚石、石墨和富勒烯是化学元素碳的不同同素异形体。所有这些化合物的组成中只有碳原子,但碳原子的排列方式各不相同。
目录
1. 概述和主要区别
2. 什么是钻石
3. 什么是石墨
4. 什么是富勒烯
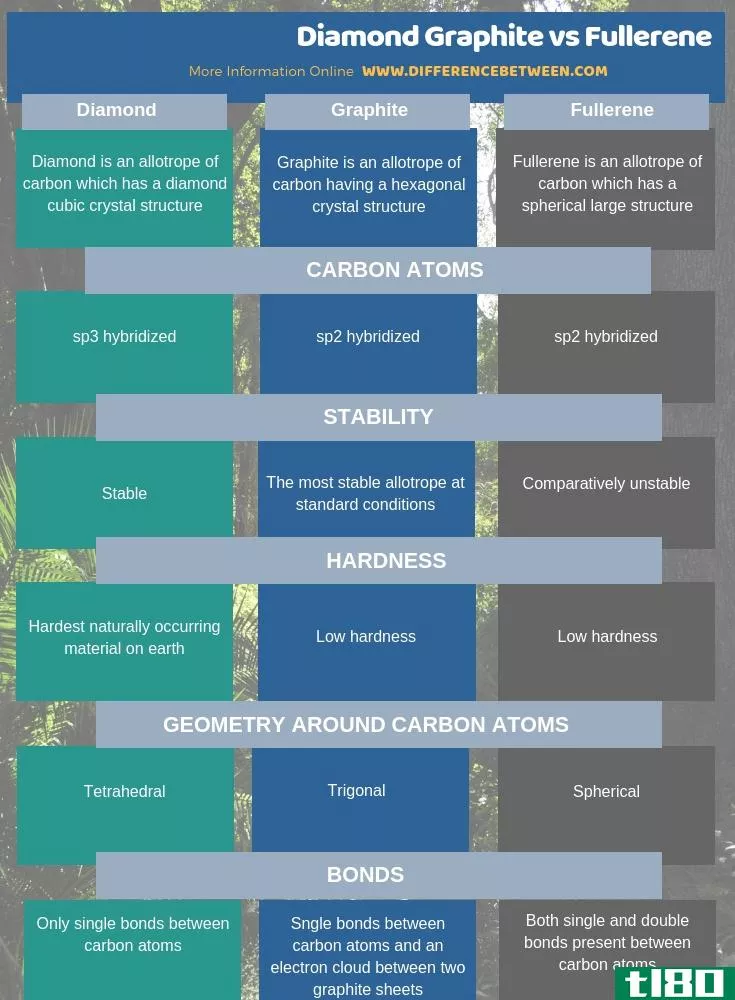
5. 并列比较-金刚石、石墨和富勒烯的表格形式
6. 摘要
什么是钻石(diamond)?
金刚石是碳的同素异形体,具有金刚石立方晶体结构。它在标准温度和压力下处于固态。此外,它具有所有材料中最高的硬度和最高的导热系数。钻石属于天然矿物的范畴,通常它的颜色是黄色、棕色或灰色到无色。此外,这种材料在四个方向的解理是完美的,断裂是不规则的。钻石的矿物条纹是无色的。在考虑光学性质时,金刚石是各向同性的。

图01:钻石
在这种材料中,碳原子是sp3杂化的。每个原子与另一个原子形成四面体。四面体结构是刚性的,原子间的键很强。而且,在一个单位的钻石中,原子的数量最多。
什么是石墨(graphite)?
石墨是碳的同素异形体,具有六方晶体结构。这种化合物自然以石墨矿的形式存在,因此,我们可以通过采矿获得这种材料。它是标准温度和压力下碳最稳定的同素异形体。此外,在很高的温度和压力条件下,石墨可以转化为金刚石。它具有很高的导电性。

图02:石墨
石墨也属于天然矿物的范畴。颜色可能从铁黑到铁灰色。此外,这种材料的解理是基底的,断裂是片状的。它的硬度很低,有一种金属的,泥土般的光泽。石墨的矿物条纹是黑色的。当考虑光学性质时,石墨是单轴的。
什么是富勒烯(fullerene)?
富勒烯是碳的同素异形体,具有大的球形结构。同素异形体中的碳原子通过单键和双键相互连接。此外,球形结构是一个封闭或部分封闭的网状结构,具有包含5到7个碳原子的熔合环。它们是sp2杂化原子。然而,这种结构在原子之间有一个角度应变。
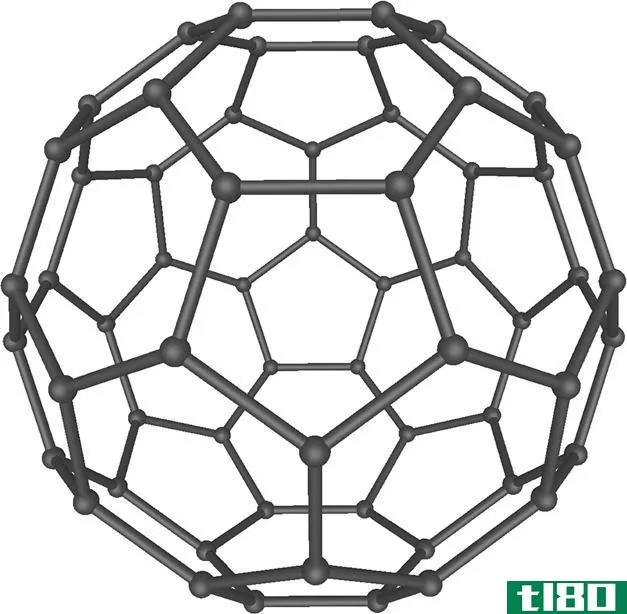
图03:富勒烯球体的结构
此外,富勒烯可溶于有机溶剂,包括甲苯、氯苯等。一般来说,这种材料是一种电绝缘体。
金刚石石墨(diamond graphite)和富勒烯(fullerene)的区别
金刚石、石墨和富勒烯是碳的同素异形体。金刚石石墨和富勒烯的关键区别在于金刚石具有金刚石立方晶体结构和石墨具有六角形晶体结构,而富勒烯则以大的球状分子形式存在。此外,金刚石是地球上最坚硬的天然物质,但石墨和富勒烯的硬度相对较低。
此外,金刚石石墨和富勒烯之间的另一个区别是,金刚石的碳原子是sp3杂化的,但在石墨和富勒烯中,它们是sp2杂化的。当考虑碳原子周围的几何结构时,金刚石是四面体的,石墨是三角形的平面,而富勒烯是球形的。
总结 - 钻石(diamond) vs. 石墨(graphite)
金刚石、石墨和富勒烯是碳的同素异形体。综上所述,金刚石石墨和富勒烯的关键区别在于金刚石具有金刚石立方晶体结构和石墨具有六角晶体结构,而富勒烯则以大的球状分子形式存在。
引用
1“石墨”。地质学,这里有。“钻石”,维基百科,维基媒体基金会,2019年7月13日,可在这里查阅。
2“钻石”,维基百科,维基媒体基金会,2019年7月13日,