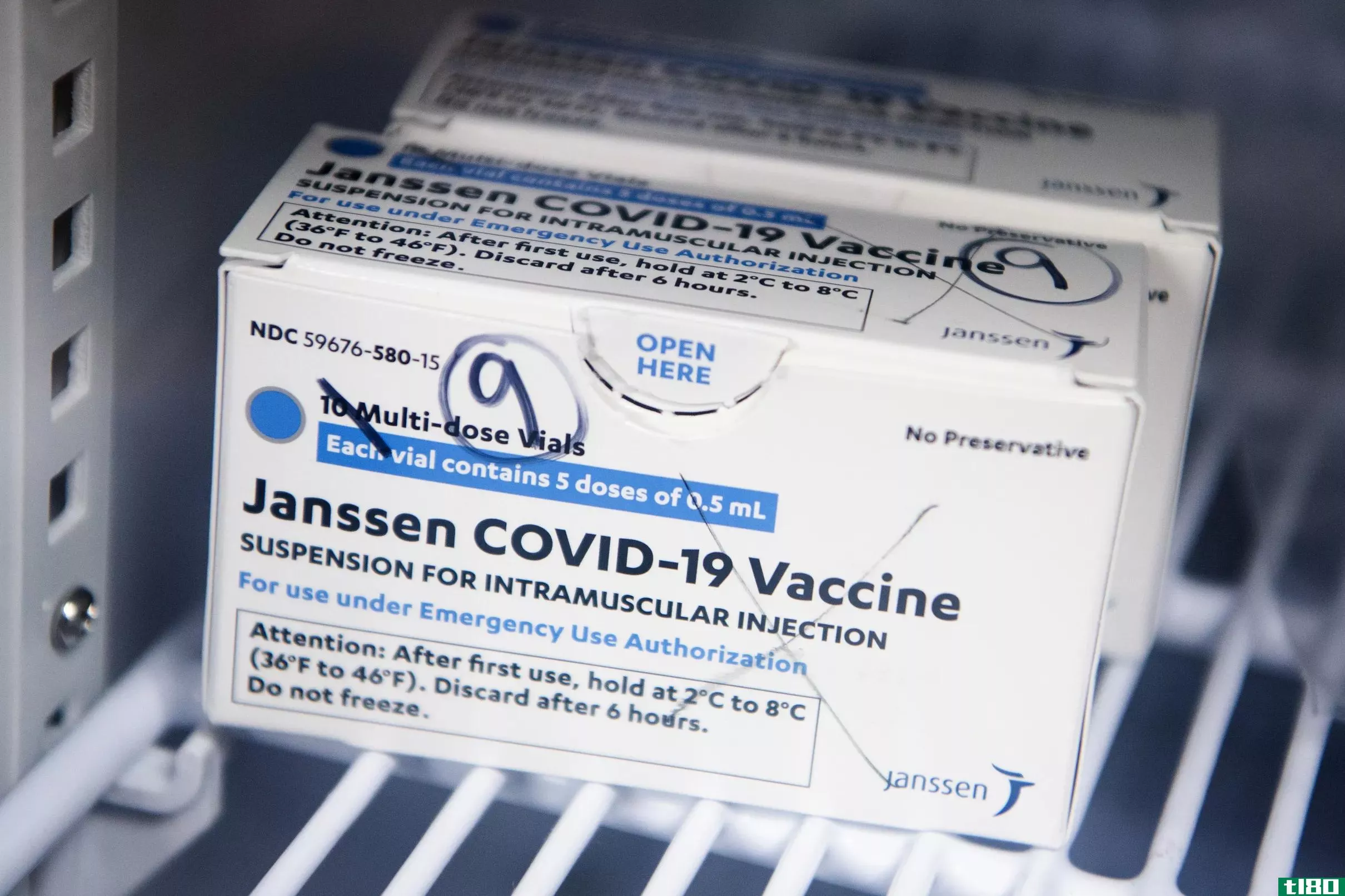
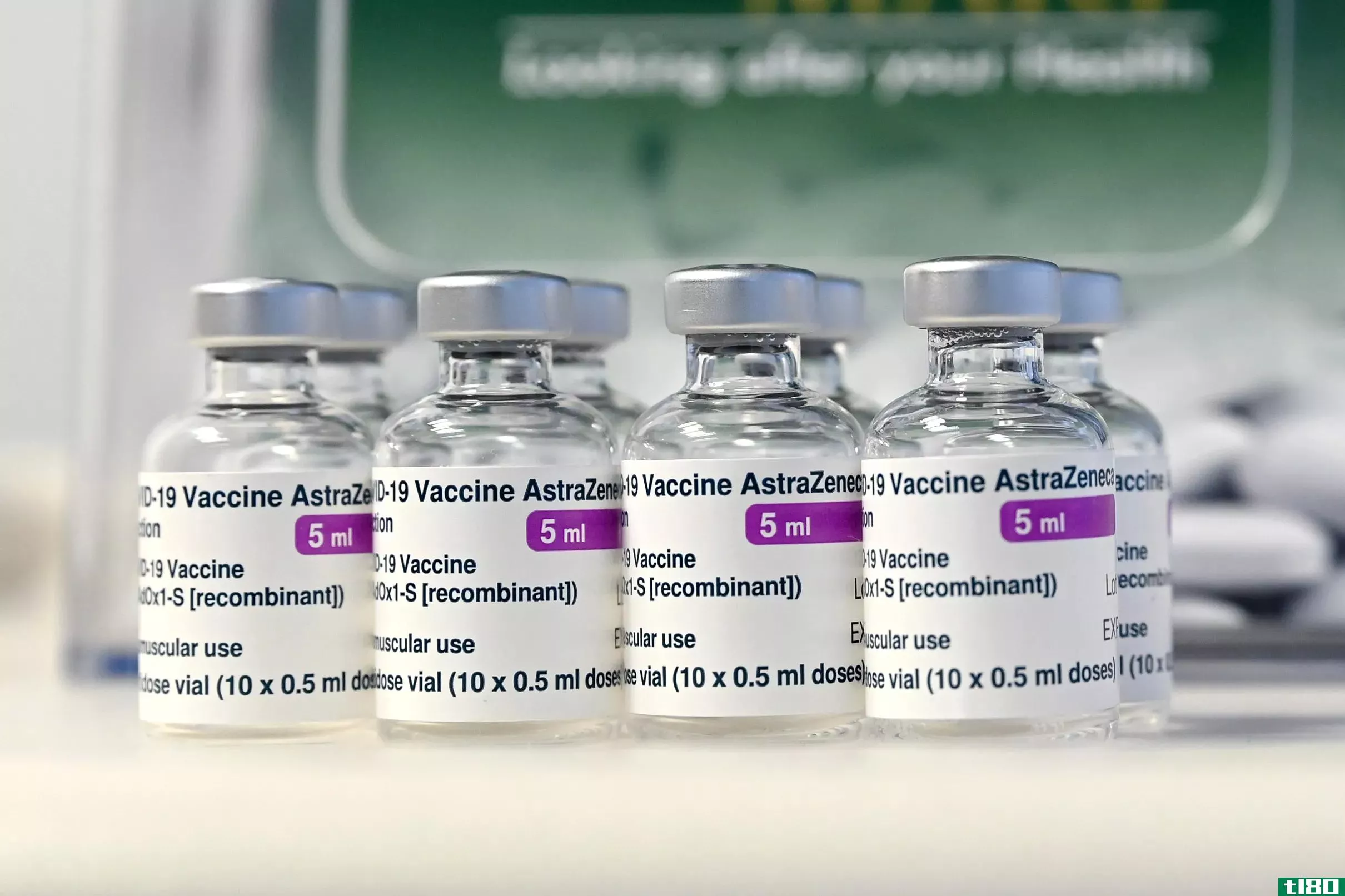
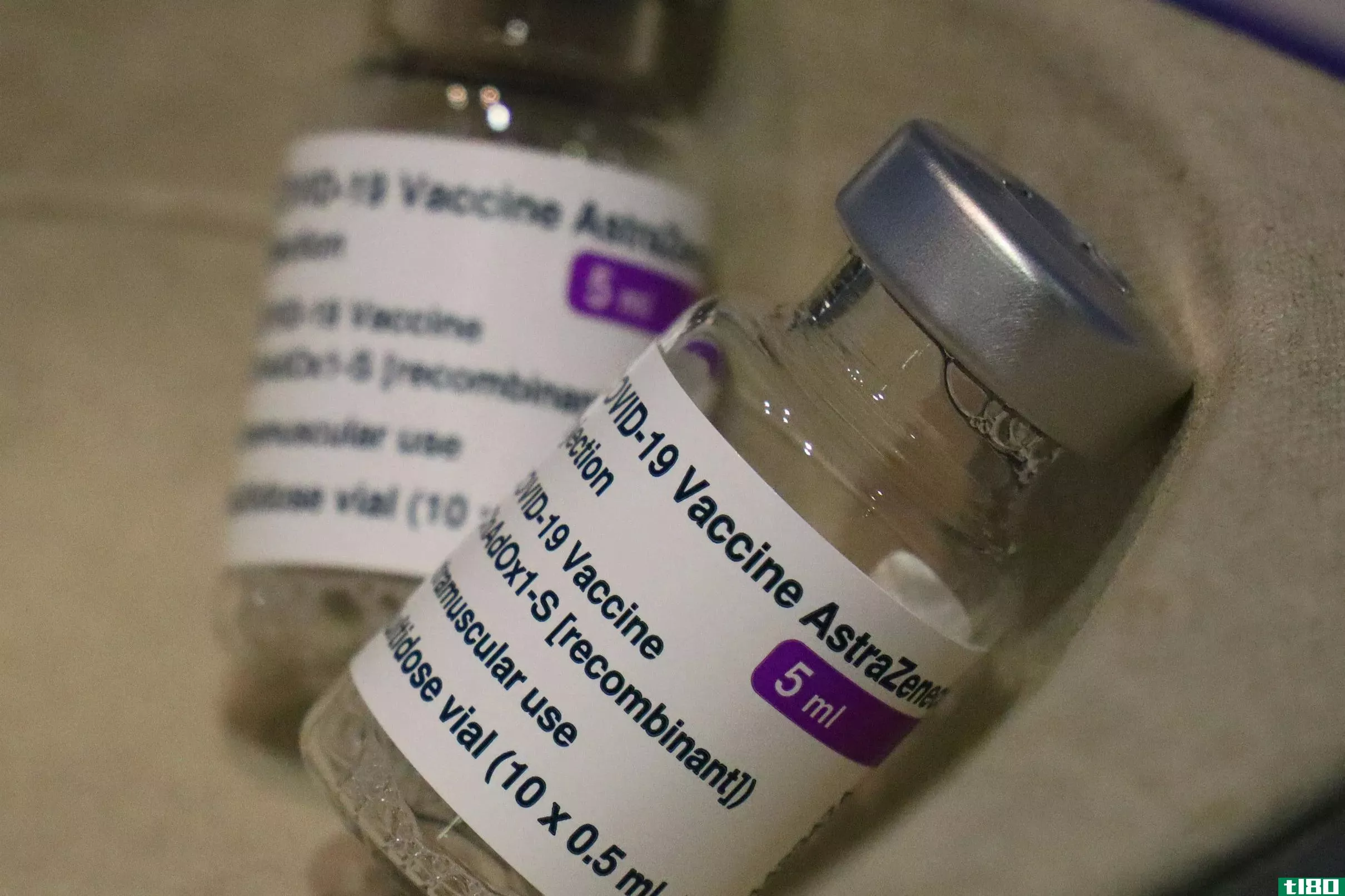美国官员公开质疑阿斯利康的covid-19疫苗数据
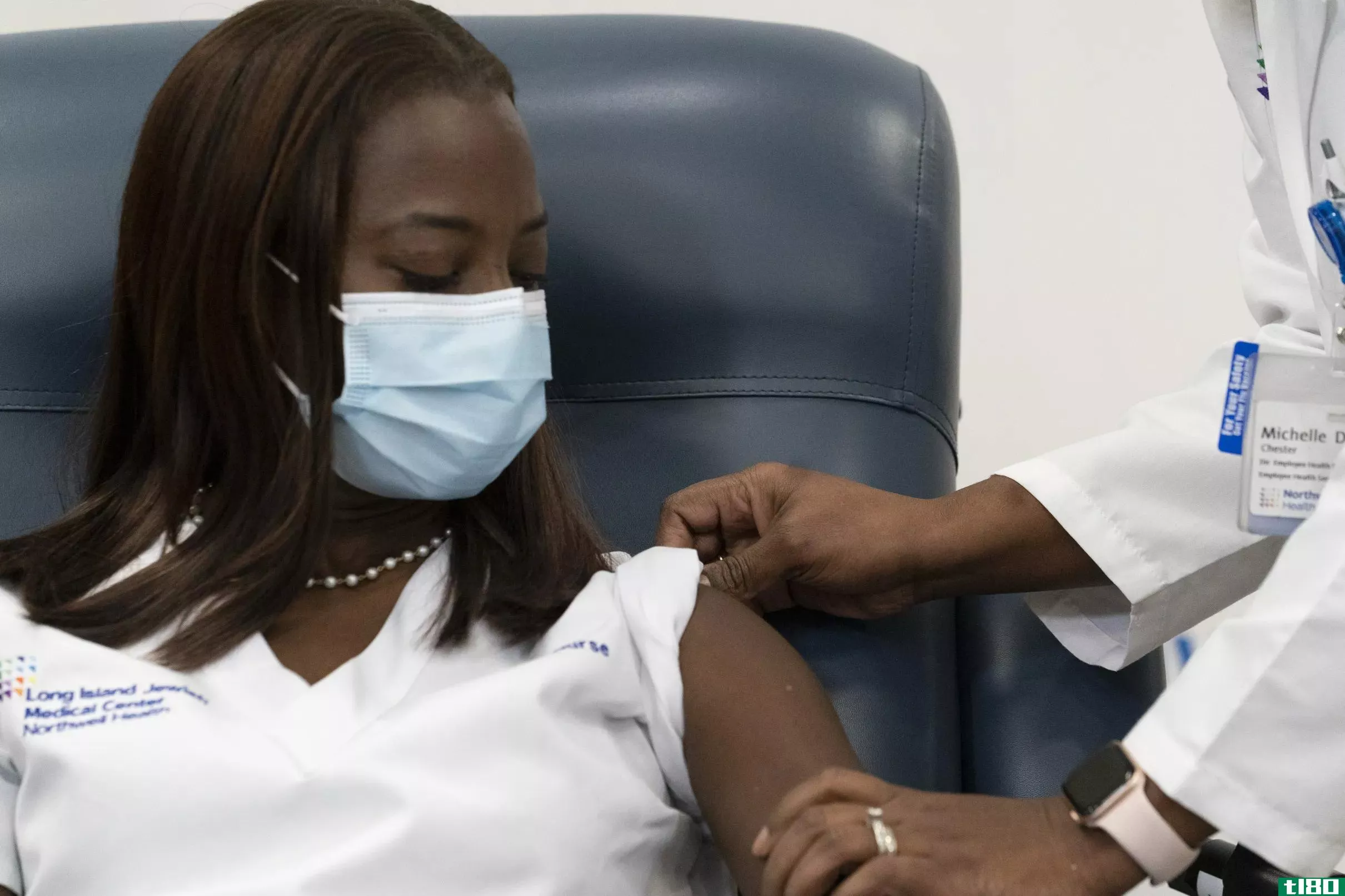
美国卫生官员在今早发表的一份极不寻常的声明中说,阿斯利康发布的COVID-19疫苗数据可能包含“过时信息”,此前不到一天,这家制药公司表示,其疫苗在美国试验中非常有效。
NIAID说,独立专家委员会审查了试验数据,对公开发布的数据表示担忧。该机构在声明中说,它“可能提供了一个不完整的疗效数据视图”。
NIAID负责人安东尼·福西(Anthony Fauci)今天上午在《早安美国》节目中说,这一宣布可能会导致人们对阿斯利康疫苗产生一些不必要的犹豫。
他说:“这真的是你所说的非受迫性错误,因为事实是,这很可能是一种非常好的疫苗。”。“如果你看看这些数据,他们确实相当不错,但当他们把数据放进新闻稿时,并不完全准确。”
阿斯利康在一份声明中说,它发布的信息是基于2月17日之前收集的数据。该公司表示,目前正在分析最新数据,并将在48小时内分享。
临床试验专家埃里克·托波尔对《****》说,通常情况下,公司和监督其试验的独立董事会之间的分歧不会公开发生。“我从来没见过这样的事,”托波尔说,他同时也是加州斯克里普斯研究转化研究所的负责人。
今天上午的声明是阿斯利康疫苗一长串问题中的最新一个。该公司对监管机构的透明度不够,给了英国一些临床试验参与者错误的疫苗剂量。一些人在接种疫苗后出现异常凝血障碍,欧洲医生对此提出了安全问题。专家们希望,昨天的声明,包括来自美国大规模和严格控制的临床试验的数据,将有助于澄清有关疫苗的悬而未决的问题,并恢复对疫苗注射的一些信心。
如果阿斯利康在美国申请授权,它必须将美国临床试验的所有数据发送给食品和药物管理局。该机构的科学家们将公开发表他们的独立分析报告,这也将给专家们提供审查的机会。
阿斯利康COVID-19疫苗已经在世界多个国家使用。
- 发表于 2021-04-16 04:48
- 阅读 ( 136 )
- 分类:互联网
你可能感兴趣的文章
美国建议暂停使用强生疫苗,理由是“非常谨慎”
联邦机构建议美国暂停使用强生COVID-19疫苗,直到当局能够收集到更多关于6名注射者出现罕见凝血障碍的报告。 食品和药物管理局(FDA)在与疾病控制和预防中心(CDC)的联合声明中说:“出于谨慎,我们建议暂停...
- 发布于 2021-04-15 22:05
- 阅读 ( 192 )
强生公司的停摆将如何影响疫苗市场的恐慌
...安全问题的重要性,以便让人们不那么犹豫不决。”。 美国食品药品监督管理局(FDA)和美国疾病控制与预防中心(CDC)在调查六份关于强生疫苗接种者出现罕见血栓的报告时,建议暂停接种。这些特殊的疾病是不寻常的:患...
- 发布于 2021-04-15 22:14
- 阅读 ( 156 )
强生covid-19疫苗暂停继续,官方要求提供更多数据
在美国,强生COVID-19疫苗的使用仍处于暂停状态,因为官员们收集了更多关于6名注射者体内罕见血栓的信息。疾病控制和预防中心的一个独立咨询委员会说,他们还没有足够的信息来说明哪些人群可能有血栓的风险,也没有建议...
- 发布于 2021-04-15 22:42
- 阅读 ( 196 )
欢迎来到疫苗外交时代
白宫称,目前存放在美国仓库中的数百万剂COVID-19疫苗现在运往墨西哥和加拿大的疫苗接种点。这一捐赠标志着美国迈出了第一步,进入了大流行后期疫苗外交的曙光——也是充满争议的世界。 据报道,这一睦邻姿态...
- 发布于 2021-04-16 04:19
- 阅读 ( 188 )
阿斯利康covid-19疫苗在美国的研究中有79%的有效率
在美国进行的一项大型试验中,第四种COVID-19疫苗显示,它可以保护人们免受该疾病最严重的影响。阿斯利康公司今天发布的一份新闻稿称,两剂阿斯利康疫苗对预防人们出现症状性COVID-19的有效率为79%。该公司说,在美国试验...
- 发布于 2021-04-16 04:29
- 阅读 ( 163 )
调整后的阿斯利康数据显示covid-19疫苗的有效率为76%
...比该公司本周早些时候在一份公告中吹嘘的79%略有下降。美国卫生官员在一份非同寻常的公开声明中指责该公司说,这个数字是基于过时的数据。 最初的疗效是基于使用2月17日之前收集的数据进行的中期分析。但是...
- 发布于 2021-04-16 04:55
- 阅读 ( 142 )
vergecast:oneplus 9审查和今年第一次大型科技国会听证会
...中的完整讨论。 进一步阅读: 阿斯利康COVID-19疫苗在美国的研究中有79%的有效率 美国官员公开质疑阿斯利康的COVID-19疫苗数据 拜登的COVID-19疫苗网站建立在猪流感工具的基础上 OnePlus 9和9 Pro推出哈塞尔布拉德品牌相机 OnePlus 9...
- 发布于 2021-04-16 05:43
- 阅读 ( 233 )
疫苗正在改变我们对covid-19数字的理解
我们永远无法确定在美国有多少人在某个特定的时间感染了COVID-19。相反,我们将所有的指标结合起来——检测结果呈阳性的百分比、每天报告的新病例数、有COVID-19症状的急诊病人——得到一个估计值。这就像盲人和大象的故...
- 发布于 2021-04-16 05:50
- 阅读 ( 154 )
为什么fda要花22天来检查强生的数据
...的数据进行审查。这需要研究所有研究地点的病例——在美国、拉丁美洲和南非,一种新的冠状病毒变种占主导地位。疫苗的典型审查过程可能需要几个月。相反,它将在几周内发生。 如果这个过程和FDA为早期候选疫苗计划的...
- 发布于 2021-04-16 08:30
- 阅读 ( 152 )
阿斯利康的covid-19疫苗从一开始就令人困惑
...类服务部对这些预测大加赞赏,称疫苗将于2020年10月抵达美国。 这些预测将证明是不现实的。该疫苗的临床试验在9月份因安全问题而暂停,减缓了进展,最初的数据直到11月下旬才公布。当时,该公司宣布疫苗的有效率高达90%...
- 发布于 2021-04-16 08:57
- 阅读 ( 164 )