活化能与阈能的关键区别在于,活化能描述了反应物与活化络合物之间的势能差,而阈能则描述了反应物成功碰撞形成活化络合物所需的能量。
精力是工作的能力。如果有足够的能量,我们可以用它来做一些我们想要的工作;在化学中,这个功可以是化学反应,也可以是核反应。我们用两种不同的能量形式来定义化学反应能。
目录
1. 概述和主要区别
2. 什么是活化能
3. 什么是临界能量
4. 并列比较-激活能与阈值能量的表格形式
5. 摘要
什么是活化能(activation energy)?
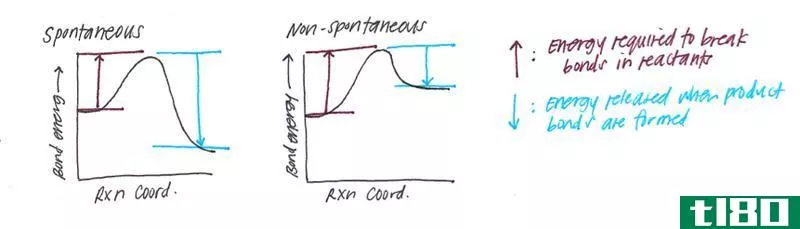
活化能是我们激活化学反应或核反应或任何其他反应所需的一种能量。大多数情况下,我们用单位千焦每摩尔(kJ/mol)来测量这种能量形式。这种形式的能量是阻止化学反应进行的势能屏障。这意味着它阻止反应物转化为产物。此外,为了在热力学系统中进行化学反应,系统必须达到一个足够高的温度,该温度足以为反应物提供等于或大于活化能垒的能量。
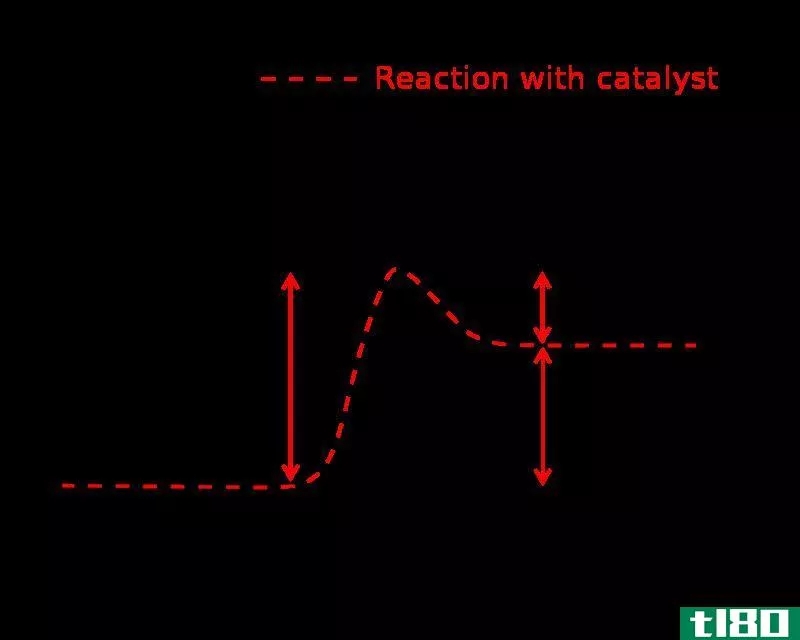
图01:无催化剂和有催化剂时的反应速率
如果系统得到足够的能量,那么反应速率就会增加。然而,在某些情况下,反应速率随着温度的升高而降低。这是由于负的活化能。我们可以用Arrhenius方程计算反应速率和活化能。具体如下:
K=Ae-Ea/(RT)
式中,k为反应速率系数,A为反应频率因子,R为通用气体常数,T为绝对温度。那么Ea是活化能。
除此之外,催化剂是能够降低反应活化能垒的物质。它是通过改变反应的过渡态来实现的。此外,在进行反应时,反应不消耗催化剂。
什么是阈值能量(threshold energy)?
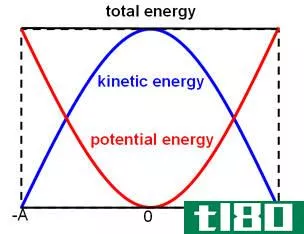
临界能量是一对粒子为了成功碰撞所必须具备的最小能量。这个术语在粒子物理中非常有用,而不是在化学中。在这里,我们讨论粒子的动能。粒子的这种碰撞形成了反应的活化复合物(中间物)。因此,阈值能量等于动能和活化能之和。因此,这种形式的能量总是等于或大于活化能。
活化能(activation energy)和阈值能量(threshold energy)的区别
活化能是我们激活化学反应或核反应或任何其他反应所需的一种能量。它描述了反应物和活化络合物之间的势能差。此外,它的值总是等于或低于同一热力学系统的临界能量。另一方面,临界能量是一对粒子为了成功碰撞所必须具备的最小能量。它描述了反应物成功碰撞形成活化络合物所需的能量。除此之外,这个能量的值总是等于或大于同一热力学系统的活化能。下面的信息图以表格形式展示了活化能和阈值能量之间的差异。

总结 - 活化能(activation energy) vs. 阈值能量(threshold energy)
我们可以定义热力学系统的临界能和活化能。活化能与阈能的关键区别在于,活化能描述了反应物与活化络合物之间的势能差,而阈能则描述了反应物成功碰撞形成活化络合物所需的能量。
引用
1“激活能”,维基百科,维基媒体基金会,2018年7月27日。在这里可以买到2。“临界能量”,维基百科,维基媒体基金会,2018年8月9日。此处提供
2“临界能量”,维基百科,维基媒体基金会,2018年8月9日。