定域化学键和离域化学键的关键区别在于,定域化学键是特定原子上的特定键或孤电子对,而离域化学键是与单个原子或共价键无关的特定键。
化学键是两个原子之间的连接。这种联系是由于分子轨道的重叠造成的。化学键有两种主要形式,即局域化和非局域化化学键。定域化学键是正常的分子轨道重叠,如sigma键和pi键。然而,离域化学键则不同。这些债券形成时,几个地方债券混合在一起。更多细节如下。
目录
1.概述和主要区别
2. 什么是局部化学键
3. 什么是离域化学键
4. 并列比较——以表格形式表示的局部化学键和非局域化学键
5. 摘要
什么是局部化学键(localised chemical bonds)?
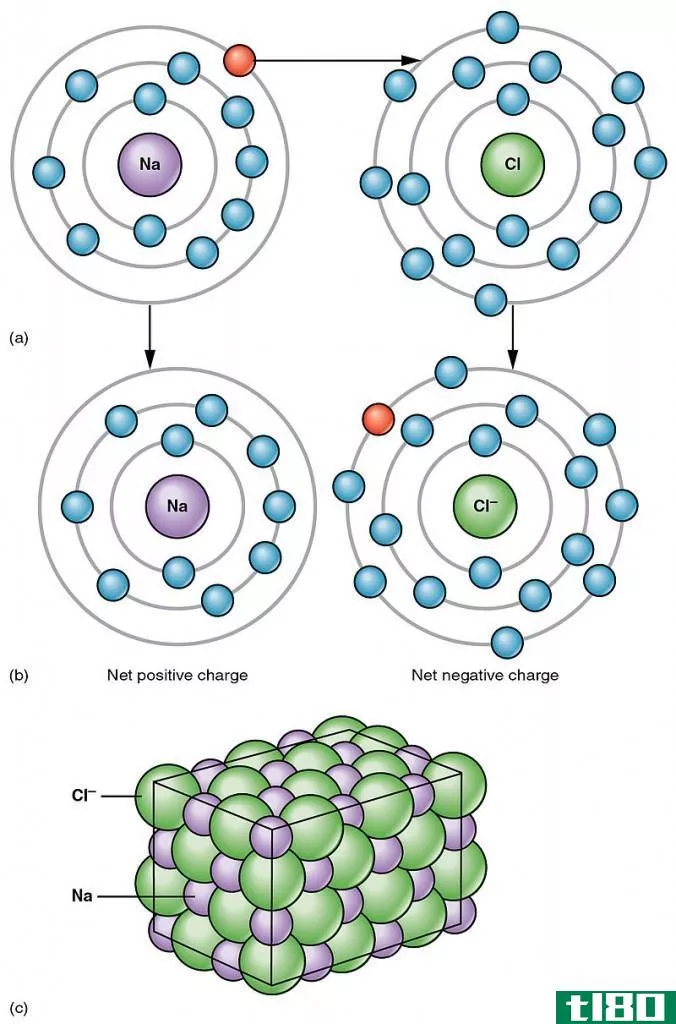
局域化化学键是存在于单个原子上的标准sigma和pi键或孤电子对。这些键集中在分子的有限区域。这些区域有集中的电子分布。换句话说,这个区域的电子密度非常高。
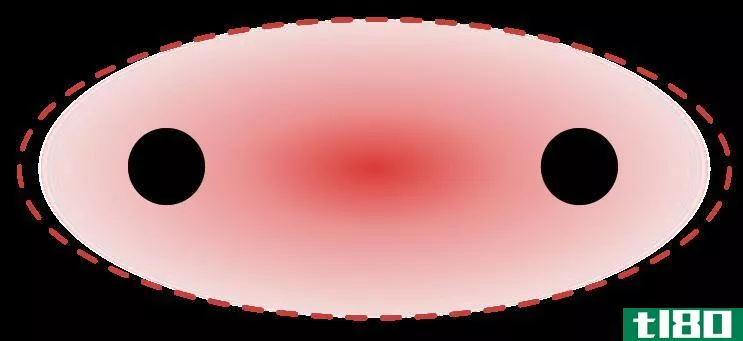
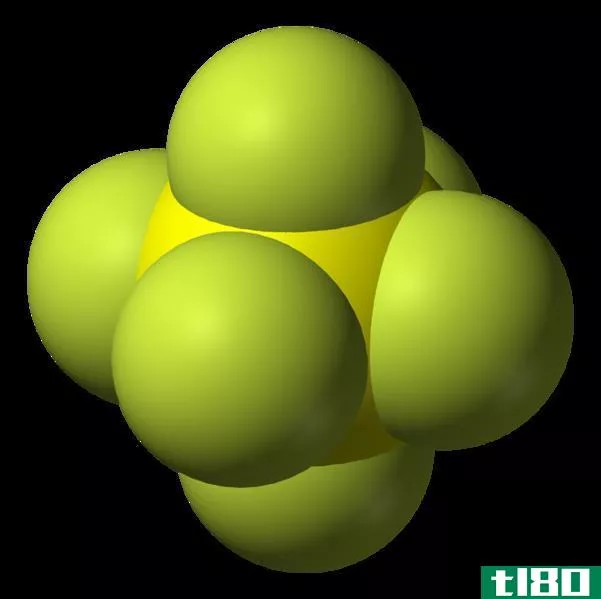
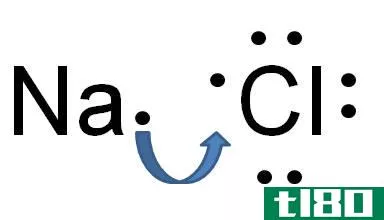
图01:Sigma键-局部化学键
当两个独立原子的两个分子轨道相互重叠时,就形成了局域键。由于两个s轨道、两个p轨道或s-p轨道重叠,可能形成Sigma键。
什么是离域化学键(delocalised chemical bonds)?
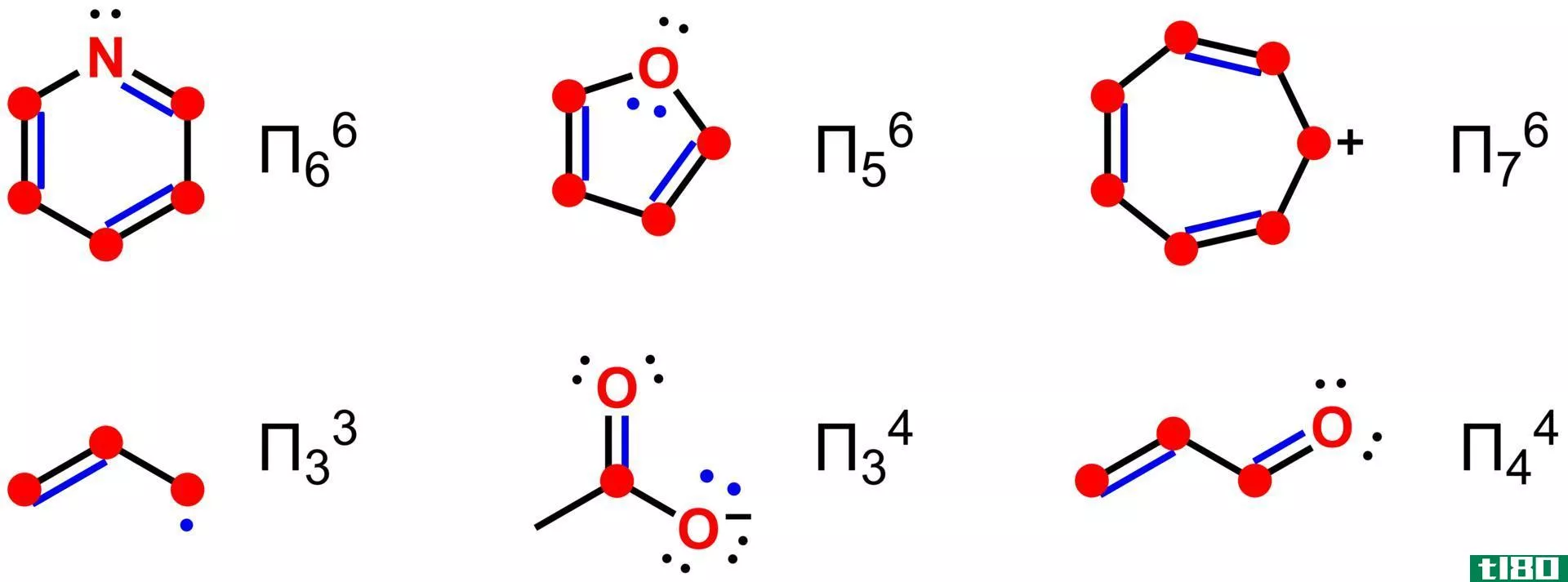
离域化学键是指不与单个原子结合,而是与几个原子或其他化学键结合的化学键。我们把这些键中的电子称为“离域电子”。在共轭pi系统中发生了离域现象。共轭π体系具有双键和单键交替模式。

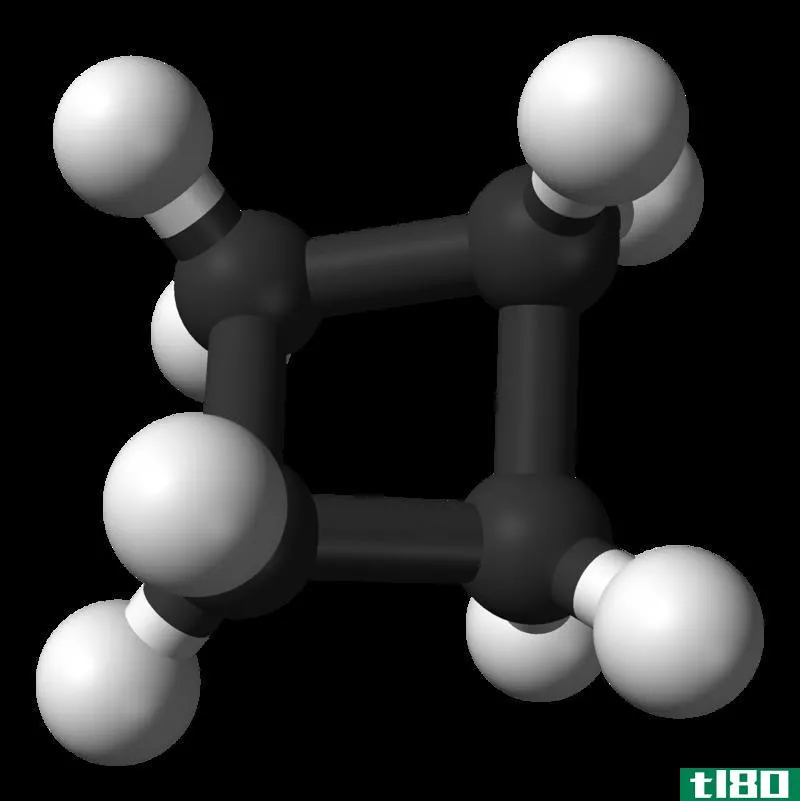
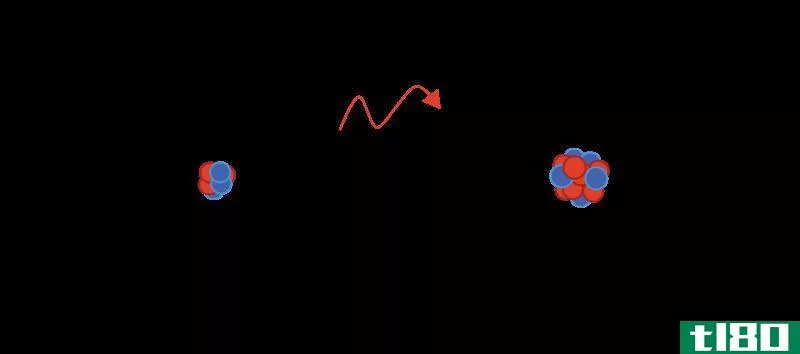
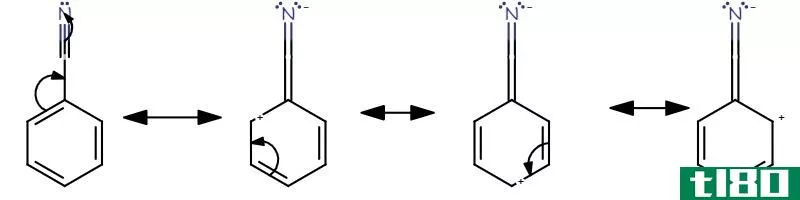
图02:电子离域
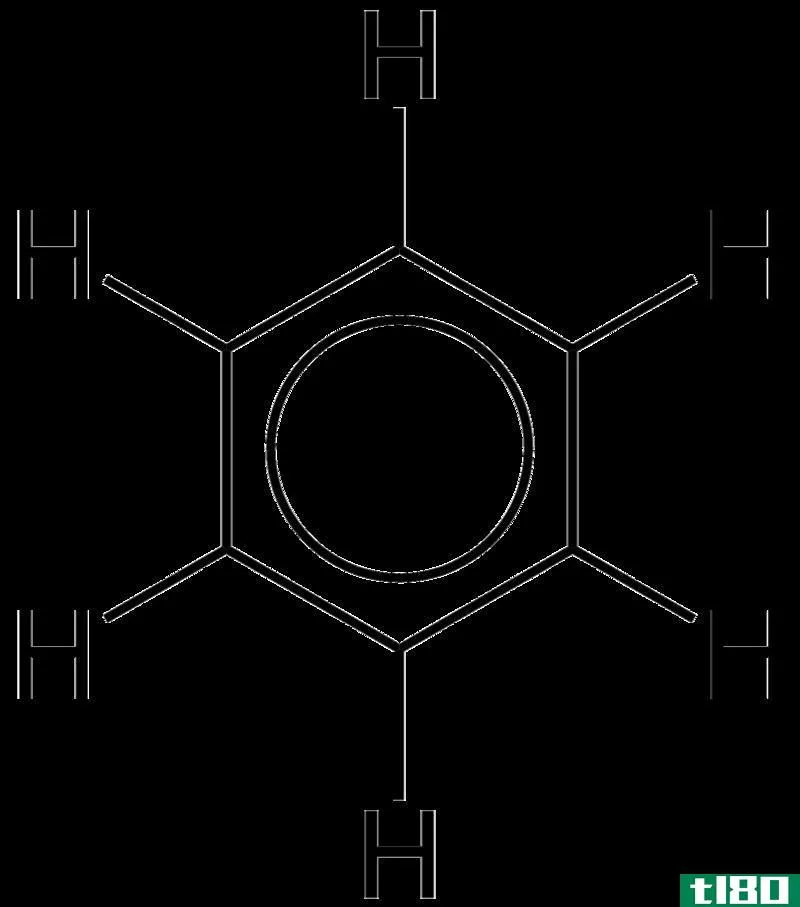
例如,苯环有三个单键和三个双键交替排列。这个环中的每个碳原子都有一个p轨道,它不发生正面重叠。因此这些p轨道可以有边重叠。这种重叠就是离域。我们可以表示为苯环顶部和底部的两个圆圈。这些电子可以在分子中自由移动,因为它们没有与单个原子或共价键的永久结合。
本地化的(localised)和离域化学键(delocalised chemical bonds)的区别
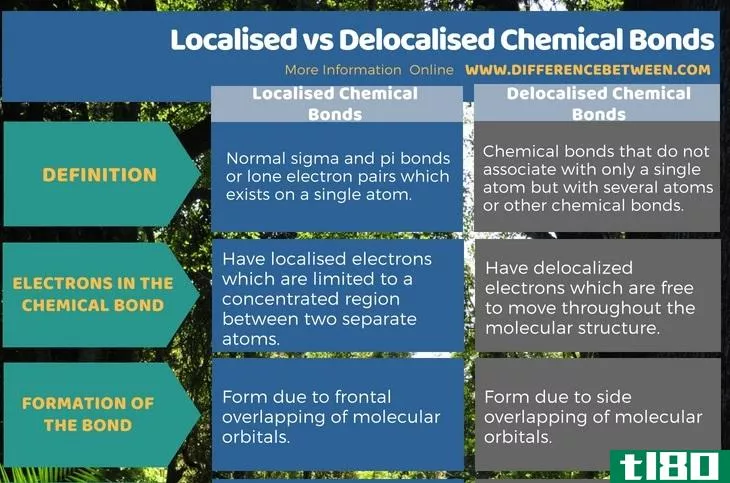
局域化化学键是存在于单个原子上的标准sigma和pi键或孤电子对。这些键的形成是由于s轨道,p轨道或s和p轨道之间的前沿重叠。此外,这些电子仅限于两个独立原子之间的特定区域。离域化学键是指不与单个原子结合,而是与几个原子或其他化学键结合的化学键。这些键的电子分布在整个分子中,可以自由移动。这些键是由于p轨道的侧面重叠而形成的。这是局域化和非局域化化学键之间的主要区别。
总结 - 本地化的(localised) vs. 离域化学键(delocalised chemical bonds)
化学键是两个原子之间的连接。化学键有两种形式:局部化学键和非局域化学键。定域化学键和离域化学键的区别在于,定域化学键是特定原子上的特定键或孤电子对,而离域化学键是与单个原子或共价键无关的特定键。
引用
1歌词。“电子的离域化”,《化学文摘》,歌词,2016年12月20日。这里有2个。“局部分子轨道”,维基百科,维基媒体基金会,2018年6月19日。此处提供
2“局部分子轨道”,维基百科,维基媒体基金会,2018年6月19日。