立体中心和手性中心的关键区别在于,当两个基团在这个点上交换时,立体中心是分子中任何一个能产生立体异构体的点,而手性中心是分子中的一个原子,当这个中心的两个基团互换时,它能产生一个对映体。
立体中心和手性中心这两个术语经常互换使用,因为所有的手性中心都是立体中心;然而,所有的立体中心都不是手性中心。

目录
1. 概述和主要区别
2. 什么是立体中心
3. 什么是手性中心
4. 立体中心与手性中心的相似性
5. 并列比较-立体中心和手性中心的表格形式
6. 摘要
什么是立体中心(a stereocenter)?
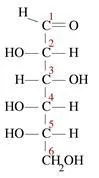
立体中心是分子中能产生立体异构体的点。然而,它不一定是一个原子。如果键合在这一点上的两组原子互换,就会得到立体异构体。立体异构体是指分子式和原子结构相同,但空间排列不同的分子。
立体中心也称为立体生成中心。如果立体中心是一个碳原子,它可以是sp2杂化或sp3杂化。这意味着立体中心可以是双键,也可以是单键。一些非手性分子也有立体中心。例如,顺反异构体有立体中心,但大多数没有手性中心。
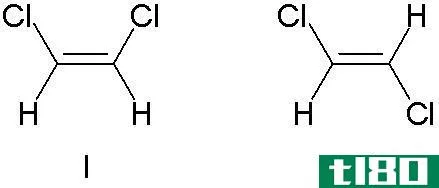
图1:二氯乙烯的顺反异构体(I-顺式异构体,II-反式异构体)
上述分子没有手性中心。但它们有立体中心。两个乙烯基碳原子都是立体中心(双键碳原子)。这是因为当附着在这些碳原子上的基团发生交换时,它们会产生异构体。
什么是手性中心(chiral center)?
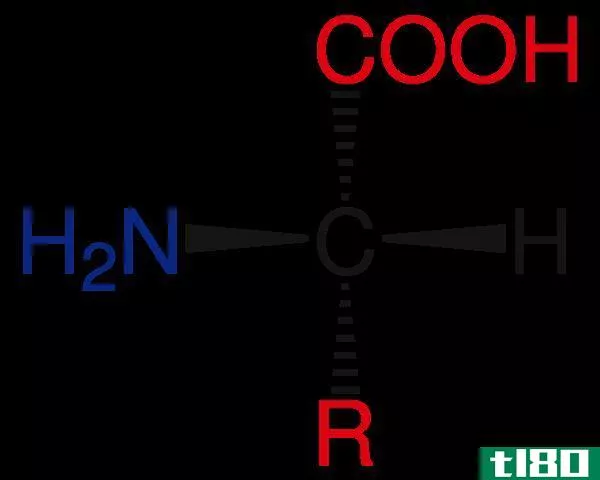
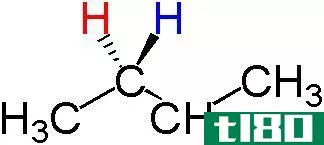
手性中心是四个不同的原子或原子群与之结合的碳原子。手性化合物是指含有手性碳原子的化合物。值得注意的是,具有手性中心的性质被称为手性。手性中心本质上是sp3杂化的,因为它必须承载四个不同的原子团,形成四个单一的共价键。
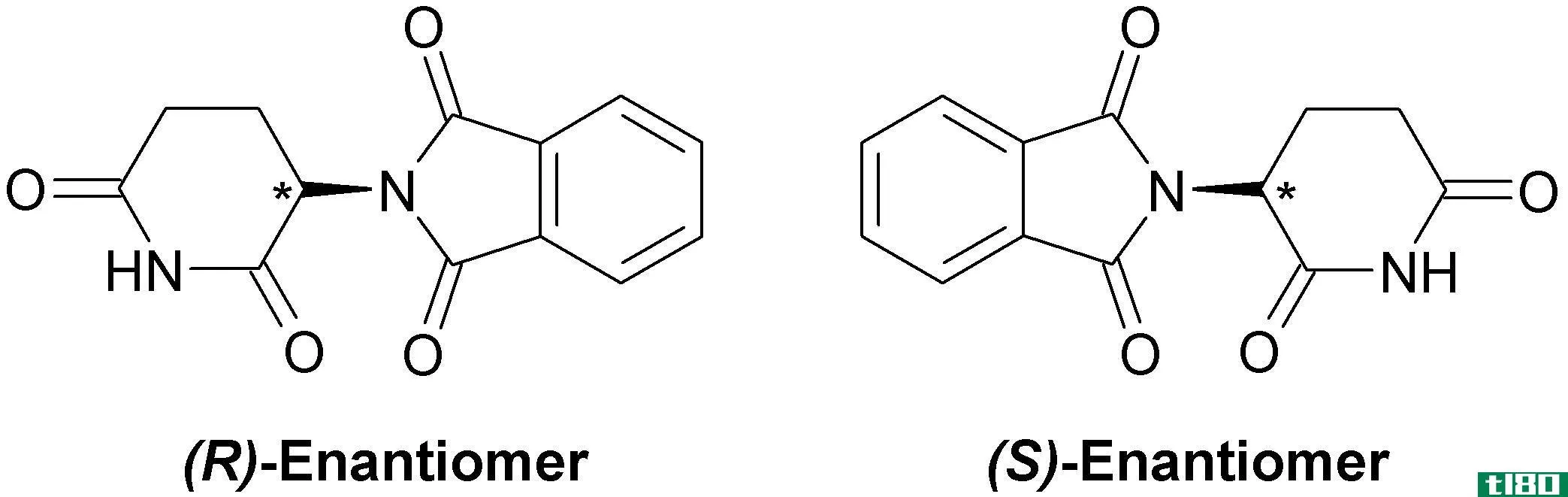
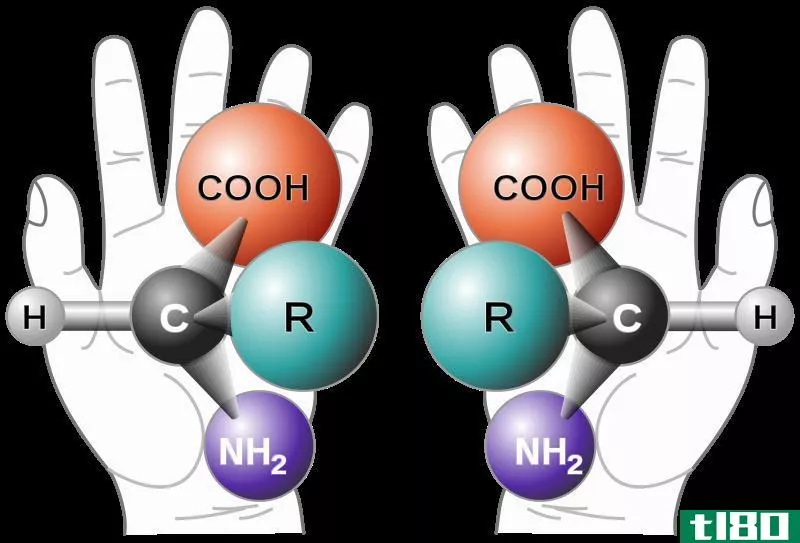
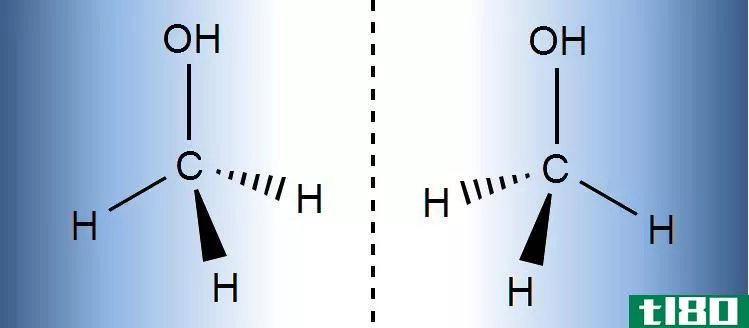
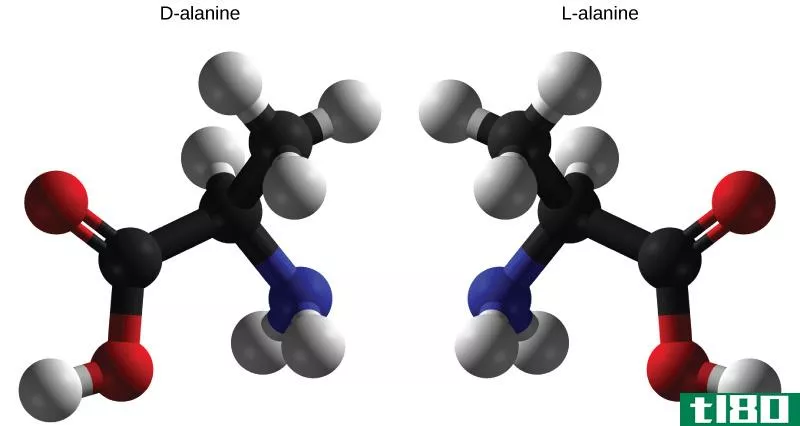
图2:由于手性中心的存在,对映体上升。
手性中心导致化合物的光学异构。换句话说,具有手性中心的化合物不会与其镜像叠加。因此,具有手性中心的化合物和与其镜像相似的分子是两种不同的化合物。这两个分子一起被称为对映体。
立体中心(stereocenter)和手性中心(chiral center)的共同点
- 立体中心和手性中心都会产生立体异构体。
- 所有的手性中心都是立体中心,但不是所有的手性中心。
立体中心(stereocenter)和手性中心(chiral center)的区别
| 立体中心与手性中心 | |
| 立体中心是分子中一个能产生立体异构体的点。 | 手性中心是一个碳原子,它与四个不同的原子或原子群结合在一起。 |
| 自然 | |
| 立体中心是分子中的一个点,不一定是原子。 | 手性中心是碳原子。 |
| 碳的杂交 | |
| 如果立体中心是碳原子,它可以是sp2杂交或sp3杂交。 | 手性中心本质上是sp3杂化的。 |
| 原子群 | |
| 立体中心可以有三个或四个组连接到它。 | 手性中心基本上有四个基团附着在它上。 |
| 化学键 | |
| 立体中心可以有单键或双键围绕它。 | 手性中心周围只有单一的键。 |
| 交换组结果 | |
| 立体中心的基团交换形成立体异构体。 | 手性中心基团的交换形成对映体。 |
总结 - 立体中心(stereocenter) vs. 手性中心(chiral center)
所有的手性中心都是立体中心,但不是所有的手性中心。立体中心是一个分子的任何一个点,当两个基团在这一点上交换时,它能产生立体异构体,而手性中心是分子中的一个原子,当这个中心的两个基团互换时,它能产生一个对映体。这就是立体中心和手性中心的关键区别。