主要区别-质子溶剂与非质子溶剂
质子溶剂和非质子溶剂的关键区别在于,质子溶剂中含有可离解的氢原子,而非质子溶剂则没有离解氢原子。
溶剂是一种能溶解其他物质的液体化合物。有不同形式的溶剂,基本上可分为极性溶剂和非极性溶剂两大类。极性溶剂可分为质子溶剂和非质子溶剂两大类。质子溶剂可以形成氢键,因为它们具有氢键所需的化学键,即O-H键和N-H键。相反,非质子溶剂缺乏氢键所需的化学键。
目录
1.概述和主要区别
2. 什么是质子溶剂
3. 什么是非质子溶剂
4. 质子和非质子溶剂的相似性
5. 并列比较-表格式的质子与非质子溶剂
6. 摘要
什么是质子溶剂(protic solvents)?
质子溶剂是极性液体化合物,具有不可分离的氢原子。这些溶剂有许多O-H键和N-H键。非相离氢原子是指在这些O-H和N-H键中与氧原子和氮原子结合的氢原子。因此,羟基(-OH)和胺基(-NH2)是蛋白质溶剂中的重要组成部分。
质子溶剂与非质子溶剂具有相同的离子溶解能力,并且是酸性的(因为它们可以释放质子)。这些质子溶剂的介电常数非常高(介电常数是电绝缘材料的一种性质,是测量物质在电场中储存电能的能力的一个量)。
质子溶剂的实例包括水、醇(如甲醇和乙醇)、氟化氢(HF)和氨(NH3)。这些溶剂通常用来溶解盐。极性质子溶剂倾向于发生SN1反应。
什么是非质子溶剂(aprotic solvents)?
非质子溶剂是极性液体化合物,没有离解氢原子。这些溶剂缺乏化学bod,如O-H键和N-H键。因此,非质子溶剂缺乏羟基(-OH)和胺基(-NH2),不能形成氢键。
非质子溶剂与质子溶剂具有相同的离子溶解能力。这些非质子溶剂缺乏酸性氢,因此不会释放大量氢离子。极性非质子溶剂具有低或中等介电常数。这些溶剂的极性适中。
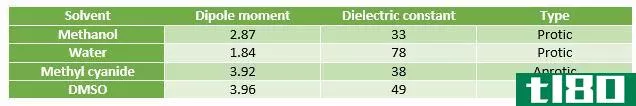
图01:质子和非质子溶剂的比较
非质子溶剂的实例包括二氯甲烷(DCM)、四氢呋喃(THF)、乙酸乙酯和丙酮。非质子盐可用于溶解。这些溶剂喜欢进行SN2反应。
原生的(protic)和非质子溶剂(aprotic solvents)的共同点
- 质子和非质子溶剂都是极性溶剂。
- 质子和非质子溶剂都能溶解盐。
原生的(protic)和非质子溶剂(aprotic solvents)的区别
| 质子与非质子溶剂 | |
| 质子溶剂是极性液体化合物,具有离解氢原子。 | 非质子溶剂是极性液体化合物,没有离解氢原子。 |
| 氢键形成 | |
| 质子溶剂能形成氢键。 | 非质子溶剂不能形成氢键。 |
| 酸度 | |
| 质子溶剂是酸性的。 | 非质子溶剂不是酸性的。 |
| 存在化学键 | |
| 质子溶剂富含O-H键和N-H键。 | 非质子溶剂缺少O-H键和N-H键。 |
| 介电常数 | |
| 质子溶剂具有很高的介电常数。 | 非质子溶剂的介电常数很低。 |
| 首选反应类型 | |
| 质子溶剂倾向于发生SN1反应。 | 非质子溶剂更容易发生SN2反应。 |
总结 - 原生的(protic) vs. 非质子溶剂(aprotic solvents)
溶剂是能够溶解物质的液体。溶剂有两种主要形式,即极性溶剂和非极性溶剂。极性溶剂又可分为质子溶剂和非质子溶剂两大类。质子溶剂和非质子溶剂的区别在于,质子溶剂有可离解的氢原子,而非质子溶剂没有离解氢原子。