关键区别——代表性要素与过渡要素
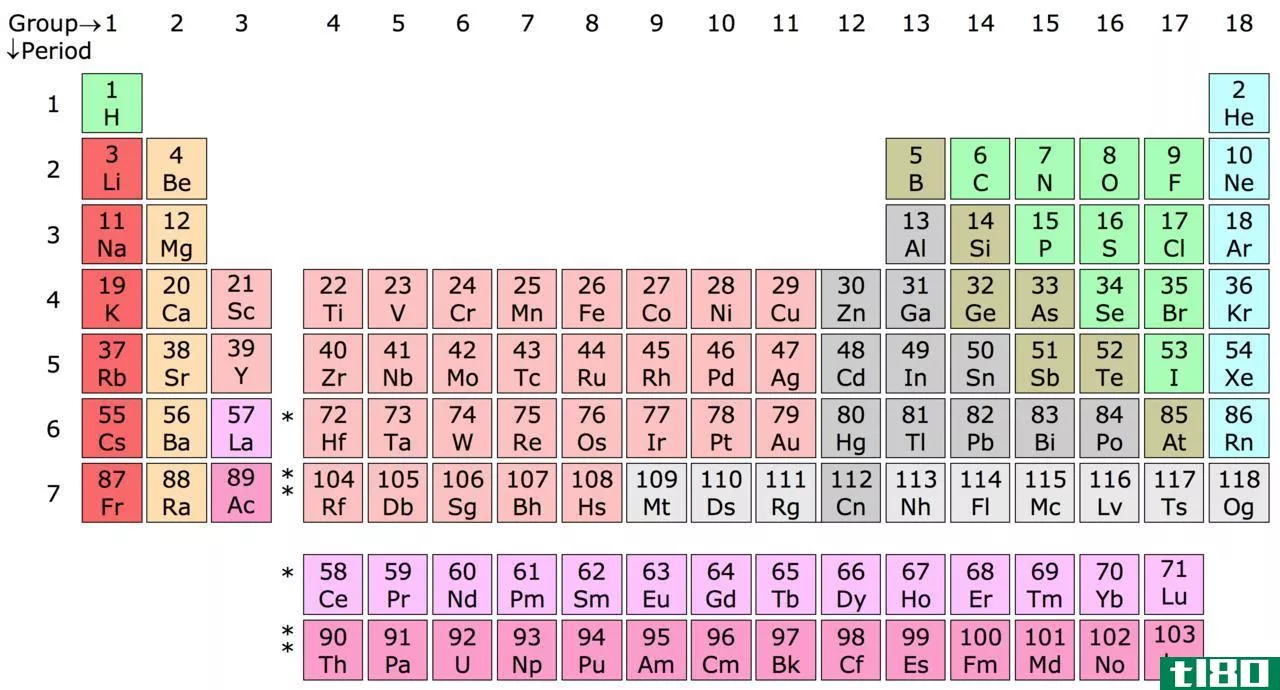
元素周期表是以原子序数为基础的所有已知化学元素的列表排列。周期表中有行或句点、列或组。元素周期表中有周期性的趋势。周期表中的元素可分为代表元素和过渡元素两类。代表元素与过渡元素的主要区别在于,代表元素是第1、第2组和第13-18组中的化学元素,而过渡元素是第3-12组中的化学元素,包括镧系元素和锕系元素。
目录
1. 概述和主要区别
2.什么是代表性要素
3. 什么是过渡元素
4. 并列比较-代表性元素与表格形式的过渡元素
5. 摘要
什么是代表性要素(representative elements)?
代表性元素是第1组、第2组和第13-18组中的化学元素。代表元素又称为“A族元素”或“s族元素和p族元素”或“主族元素”,即代表性元素包括以下几组化学元素;
- S块状元素(碱金属和碱土金属)
S块体元素的价电子位于S轨道的最外层,分为碱金属和碱土金属以及氢和氦两种类型。碱金属是第1组元素(不包括氢),而碱土金属是第2组元素。这些金属之所以这样命名,是因为它们形成碱性或碱性化合物。碱金属包括锂、钠、钾、铷、铯和弗朗。碱土金属包括铍、镁、钙、锶、钡和镭。
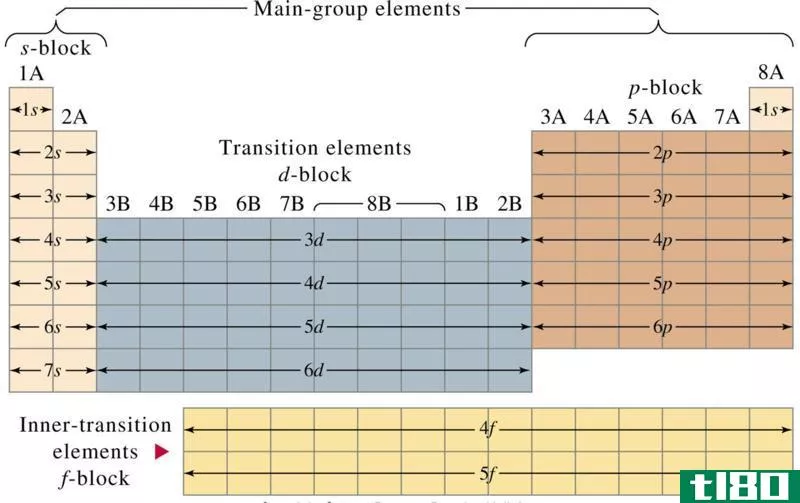
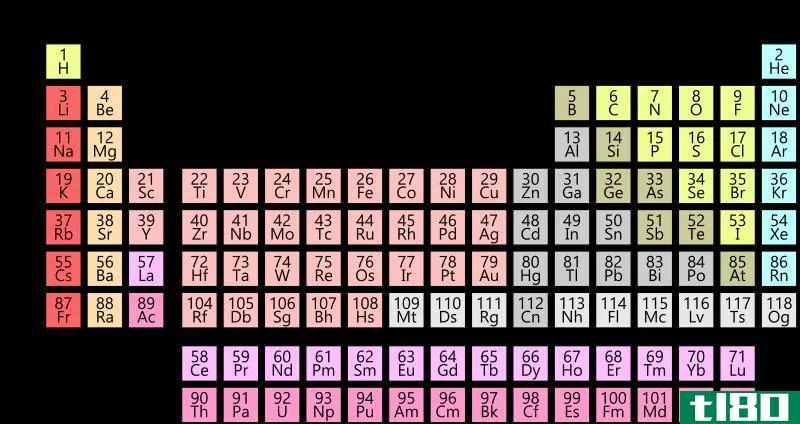
图01:周期表中代表元素和过渡元素的排列
- 惰性气体、非金属元素
P块元素的价电子在最外层的P轨道上。几乎所有的p块体元素都是非金属元素,包括一些类金属元素(不包括氦,因为它是s块体元素)。在p块体中,沿周期和群向下有周期性趋势。类金属包括硼、硅、锗、砷、锑和碲。惰性气体是18族元素(完成了电子组态)。其他的都是非金属的。
什么是过渡元素(transition elements)?
过渡元素是一种化学元素,它至少在能形成的稳定阳离子中有未成对的d电子。所有的过渡元素都是金属。它们的价电子在最外层的d轨道上。因此,从第3组到第12组的所有化学元素都是除锌以外的过渡金属(因为锌没有未成对电子,而Zn+2也没有未成对电子)。Zn+2是锌唯一稳定的阳离子)。
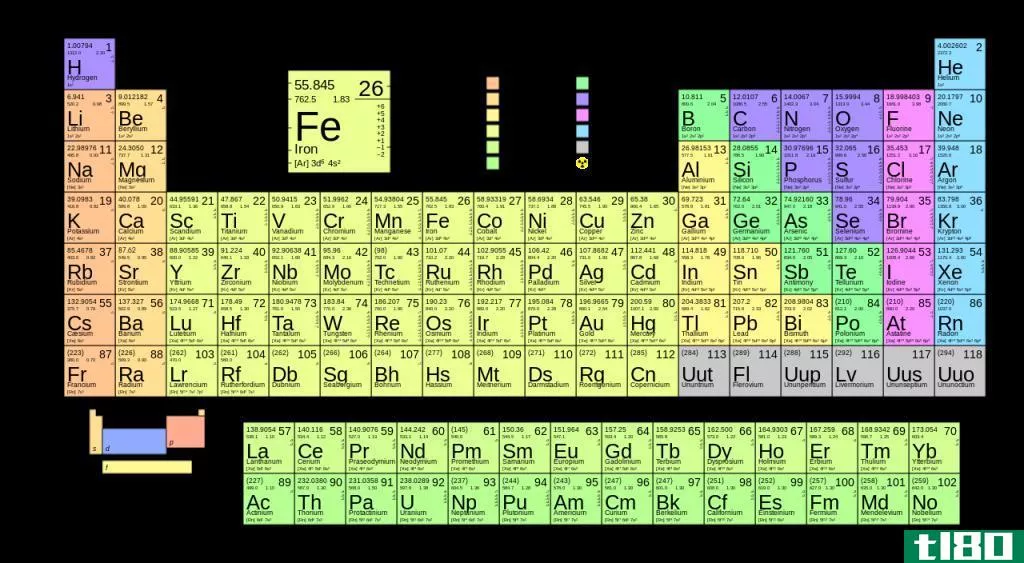
几乎所有的过渡金属在不同的化合物中都有多种稳定的氧化态。所有这些化合物都非常丰富多彩。同时,含有相同过渡元素、不同氧化状态的字幕,根据氧化状态(阳离子的颜色随同一化学元素的氧化状态而变化)而不同。这种颜色的原因是存在未配对的d电子(它允许电子通过吸收能量从一个轨道跳到另一个轨道)。当这些电子回到上一个轨道时,它以可见光的形式发出吸收的能量)。
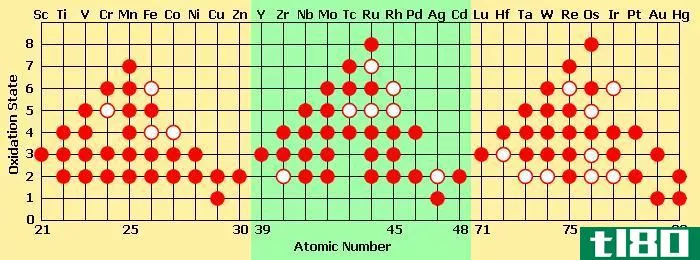
图02:过渡金属形成的不同氧化状态
镧系元素和锕系元素也被称为“内过渡金属”,因为它们的价电子位于倒数第二电子壳层的f轨道上。这些元素可以在周期表的f块中看到。
代表(representative)和过渡元素(transition elements)的区别
| 代表与过渡元素 | |
| 代表性元素是第1组、第2组和第13-18组中的化学元素。 | 过渡元素是一种化学元素,它至少在能形成的稳定阳离子中有未成对的d电子。 |
| 成员 | |
| 代表性元素包括s块和p块元素。 | 过渡元素包括d块和f块元素。 |
| 组 | |
| 代表性元素在第1组、第2组和第13至第18组中。 | 过渡元素在组3到12中。 |
| 颜色 | |
| 大多数由代表性元素形成的化合物是无色的。 | 所有由过渡元素形成的化合物都是彩色的。 |
总结 - 代表(representative) vs. 过渡元素(transition elements)
代表元素是主要的族元素,包括碱金属、碱土金属、非金属和稀有气体。过渡金属在周期表的d区和f区。代表元素与过渡元素的区别在于,代表元素是第1、第2组和第13-18组中的化学元素,而过渡元素是第3-12组中的化学元素,包括镧系元素和锕系元素。
引用
1.“代表元素的定义。”科学,可在此处查阅2.“过渡金属”,维基百科,维基媒体基金会,2018年2月25日。这里提供3.“代表性和过渡元素;)——Jade Bailey的俳句牌组。”俳句牌组:演示软件和在线演示工具。此处提供
2.“过渡金属”,维基百科,维基媒体基金会,2018年2月25日。
3.“代表性和过渡元素;)——Jade Bailey的俳句牌。”俳句牌:演示软件和在线演示工具。