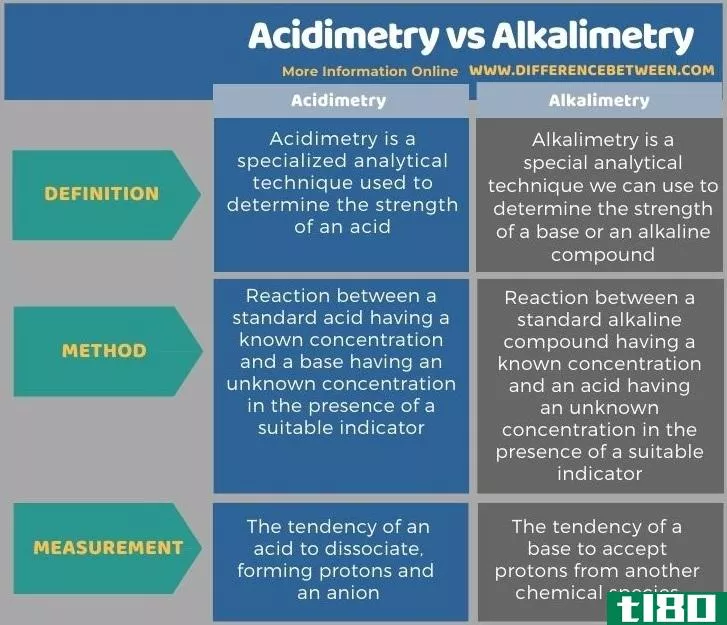
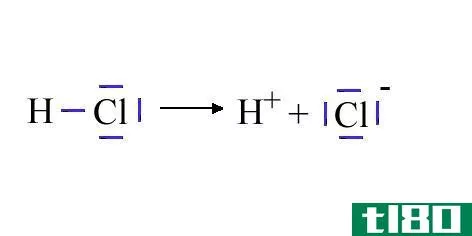主要区别——酸度与碱度
化合物的酸碱度是pH值的指示。介质的酸性是由酸性化合物引起的,酸性化合物会释放氢离子(H+),从而导致介质中的pH值较低。介质的碱性是由碱性化合物引起的,碱性化合物可以释放氢氧化物离子(OH-),从而导致介质中的高pH值。酸性和碱性之间的主要区别在于酸性导致低pH值,而碱性导致水介质中的高pH值。
目录
1. 概述和主要区别
2.什么是酸度
3.什么是碱度
4. 并列比较-以表格形式显示酸度与碱度
5. 摘要
什么是酸度(acidity)?
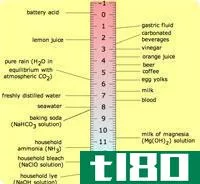
酸度是物质中酸的含量。氢离子(H+)的浓度是鉴定酸度的主要参数。氢离子浓度用pH值表示。pH是氢离子浓度的负对数。因此,氢离子浓度越高,pH值越低。pH值越低,酸度越高。
根据物质的酸性,有强酸和弱酸两种类型。在水介质中,强酸会导致较高的酸度,而弱酸则会导致低酸度。强酸可以完全分解成离子,释放出所有可能的氢离子(H+)。相反,弱酸部分分解,只释放一些氢离子。酸也可以分为一元酸和多元酸;一元酸每分子释放一个氢离子,而多元酸每分子释放更多的氢离子。
酸的酸度由酸的pKa决定。pKa是Ka的负对数。Ka是溶液的酸离解常数。它是对酸在溶液(或酸度)中强度的定量测量。降低pKa,酸就越强。pKa越高,酸性越弱。

图01:柠檬汁的酸度很高
化学元素酸度的周期性变化基本上取决于它们的电负性价值观化学元素的电负性从一个周期的左到右递增。如果一个原子的电负性更高,它很容易使负原子稳定在它上面,因为它对电子有更高的亲和力。因此,与高负性原子相关的氢离子比低负性原子更容易释放,从而产生更高的酸度。在元素周期表中,当一个基团向下移动时,酸度会增加。这是因为原子的尺寸随着原子群的增加而增加。大原子可以稳定负电荷(通过电荷分布);因此与大原子相关的氢离子可以很容易地释放出来。
什么是碱度(basicity)?
一种物质的碱度是指在一种特定的酸中,一种碱可取代的氢原子的数量。换言之,化合物的碱度是能与碱释放的氢离子完全反应的氢离子数。

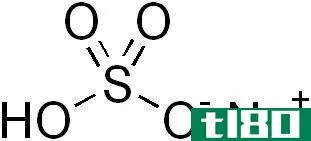
图02:氢氧化物离子的化学结构
影响化合物碱度的因素如下。
- Electronegativity
- Atomic radius
- Formal charges
原子的电负性是指它对电子的亲和力。与低电负性原子相比,具有高电负性的原子可以吸引电子。电负性越高,碱度越低。为了释放氢氧化离子,氧原子和分子其余部分之间的键电子应完全被氧原子吸引(氢氧化基团中的氧原子应比它所连接的另一个原子更具电负性)。例:如果ROH的碱度高,R的电负性小于氧原子的电负性。

图03:肥皂是脂肪酸与氢氧化钠或氢氧化钾反应形成的弱碱。
原子半径是影响化合物碱度的另一个因素。如果原子半径很小,原子的电子密度就高。因此,氢氧化物离子很容易被释放。那么化合物的碱度就比较高。
形式电荷通常是正电荷或负电荷。正的形式电荷表明电子密度较小。因此,键电子不能被氢氧化离子完全吸引。那么它就不容易释放(氢氧化物离子),表明碱度较低。相反,负的形式电荷会导致更高的碱度。
酸度(acidity)和碱度(basicity)的区别
| 酸碱度 | |
| 酸度是物质中酸的含量。 | 碱度是指作为碱的状态,可以释放出氢氧化物离子(OH-)。 |
| pH值 | |
| 酸性导致水介质中的低pH值。 | 碱性导致水介质中的高pH值。 |
| 离子 | |
| 酸性表示介质中氢离子浓度很高。 | 碱度表示介质中氢氧化物离子浓度较高。 |
| 周期性趋势 | |
| 酸度从左到右增加了一个周期,然后下降到一组。 | 碱度从左到右依次为一个周期和一组。 |
| 电负性效应 | |
| 如果(和氢原子结合的原子的)电负性高,酸度就高。 | 如果(氢氧根离子的氧原子与之结合的原子的)电负性低,碱度就高。 |
总结 - 酸度(acidity) vs. 碱度(basicity)
酸碱度是化学中使用的两个基本术语。酸性是由酸性化合物引起的。碱性是由碱性化合物引起的。酸性和碱性之间的主要区别在于酸性导致低pH值,而碱性导致水介质中的高pH值。
引用
1“7.3:结构对酸碱性的影响。”化学图书馆,图书馆,2016年9月7日,可在这里查阅。“元素周期表趋势”,学生医生网络,这里有。
2“周期表趋势”,学生医生网络,