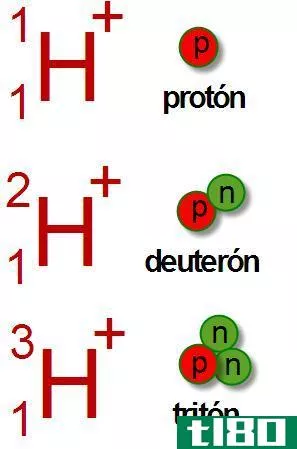
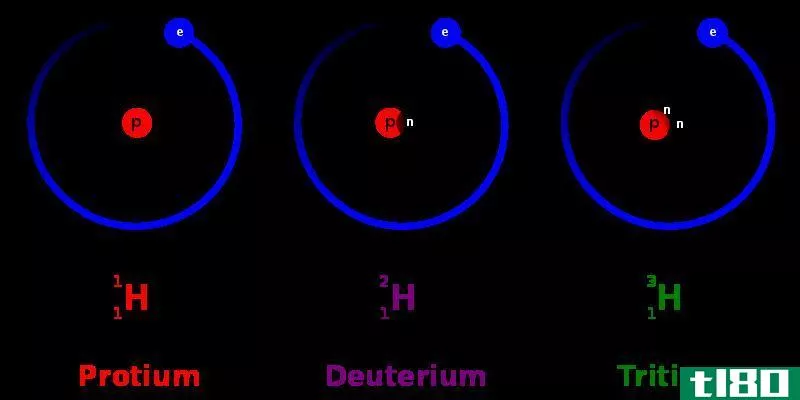
氘和氚的关键区别在于氘核有一个中子,而氚核有两个中子。
氢是周期表中的第一个和最小的元素,我们称之为H,它有一个电子和一个质子。我们可以在周期表中的第一组和周期1下对其进行分类,因为它的电子构型为1s1。氢可以吸收电子形成负电荷离子,也可以很容易地捐献电子产生一个带正电荷的质子。如果没有,它可以共享电子,形成共价键。由于这种能力,氢存在于大量的分子中,是地球上一种非常丰富的元素。氢有三种同位素,如质子-1H(无中子)、氘-2H(一个中子)和氚-3H(两个中子)。其中,蛋白质含量最高,相对丰度约为99%。
目录
1. 概述和主要区别
2. 什么是氘
3. 什么是氚
4. 并列比较-表格形式的氘与氚
5. 摘要
什么是氘(deuterium)?
氘是氢的同位素之一。它是一种稳定同位素,天然丰度为0.015%。氘核中有一个质子和一个中子。因此,它的质量数是2,原子序数是1。我们称这种同位素为重氢,显示为2H,但最常见的是用D来表示。
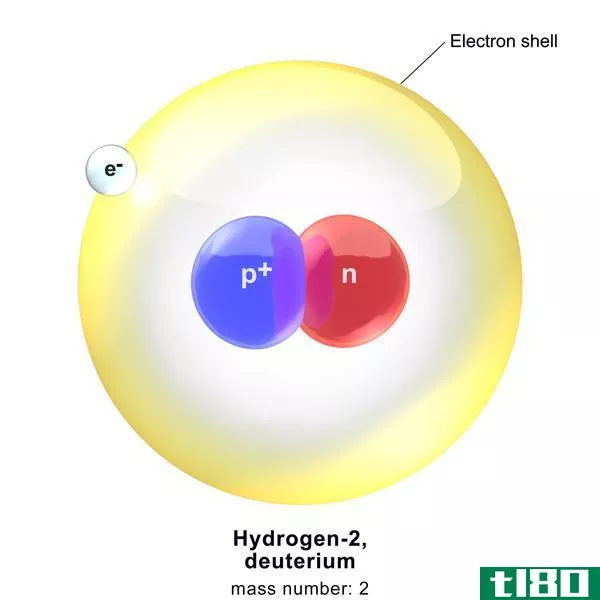
图1:氘
氘可以作为双原子气态分子存在,化学式为D2。然而,自然界中两个D原子结合的可能性很低,因为它的丰度较低。因此,氢原子主要与氢原子结合。另外,两个氘原子可以与氧结合形成水的类似物D2O,我们称之为重水。
此外,含氘的分子表现出与氢类似物不同的化学和物理性质。例如,它可以表现出动力学同位素效应。此外,氘化物在核磁共振、红外光谱和质谱上表现出特征性差异,因此,我们可以用这些方法对其进行鉴定。而且,氘的自旋是1。因此,在核磁共振中,这种同位素的耦合产生了三重态。此外,在红外光谱中,它吸收的红外频率与氢不同。由于质量差异大,在质谱中,氘和氢可以区别开来。
什么是氚(tritium)?
氚是氢的同位素,质量数为3。因此,氚原子核有一个质子和两个中子。由于它的放射性,它在自然界中只存在微量。由于这个原因,它必须人工生产,以供实际使用。
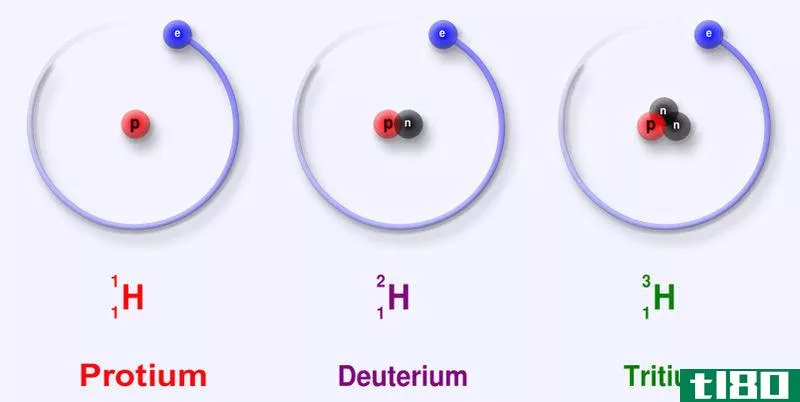
图02:氢的三种主要同位素
氚是一种放射性同位素(这是氢的唯一放射性同位素)。它的半衰期为12年,通过发射β粒子产生氦-3而衰变。这个同位素的原子质量是3.0160492。除此之外,它还存在于标准温度下。此外,它还可以形成氧化物(HTO),我们称之为“氚水”。氚可用于**核武器,并在生物和环境研究中用作示踪剂。
氘(deuterium)和氚(tritium)的区别
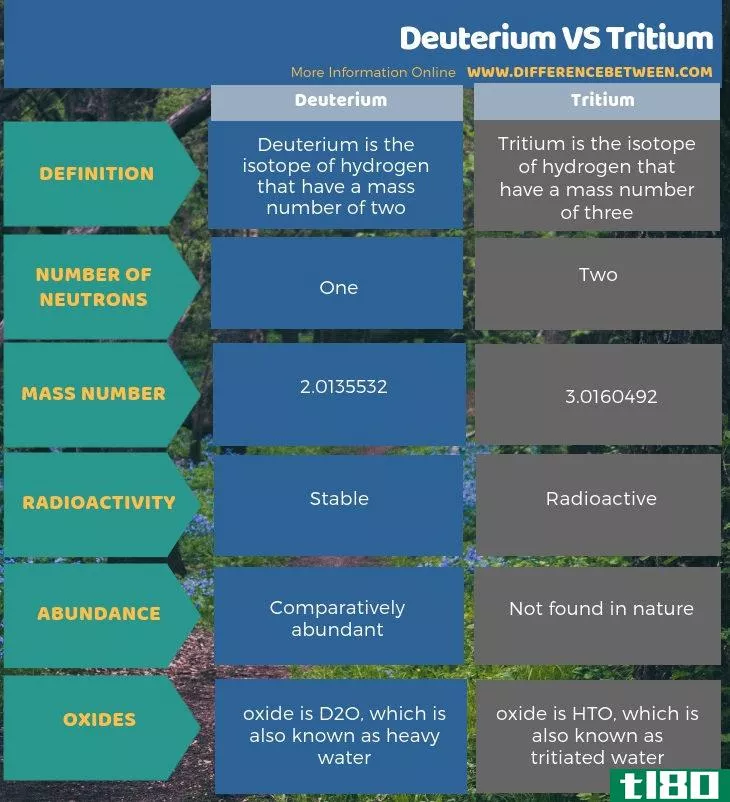
氘和氚是氢的两种同位素。氘和氚的关键区别在于氘核有一个中子,而氚核有两个中子。此外,氘的质量数为2.0135532,氚的质量数为3.0160492。所以,这是氘和氚的另一个重要区别。
此外,氘和氚之间的另一个区别是,氘是一种稳定的同位素,我们可以在自然界中找到它,而氚是一种放射性同位素,我们在自然界中找不到它。然而,我们可以人为地生产它以供实际使用。
总结 - 氘(deuterium) vs. 氚(tritium)
氘和氚是化学元素氢的同位素。氘和氚的关键区别在于氘核有一个中子,而氚核有两个中子。此外,氚是放射性的,而氘是稳定的同位素。
引用
1Helmenstine,Anne Marie,博士,“氘事实”,ThoughtCo,2019年4月2日,可在这里查阅。