化学元素周期表中周期和组的关键区别在于周期是水平行,而组是垂直列。元素周期表中有7个主要周期和18个组。
元素周期表是一个大表,其中每一个已知的化学元素都放在一个考虑到原子结构的特定位置。因此,与任何网格一样,这个周期表也有行和列。此外,每一行和每列都有特定的特征,我们将周期表中的行命名为周期,将列命名为组。
目录
1. 概述和主要区别
2. 周期表中的周期是什么
3. 周期表中的群是什么
4. 并列比较-以表格形式显示周期与组
5. 摘要
什么是周期表中的周期(periods in periodic table)?
周期是周期表中的水平行。这一行的所有化学元素都有相同数量的电子壳层。当我们经过一行时,原子核中的质子数,每增加一个元素,在这个周期内。此外,当我们向前移动一排时,元素的金属元素会减少。
然而,这些时期的成员数目不同,有些时期的化学元素比其他时期的化学元素多。这是因为,元素的数量是由每个电子壳层中允许的电子数决定的。周期表中主要有7个周期。因此,我们将它们命名为周期1,周期2,…周期7。
什么是周期表中的群(groups in periodic table)?
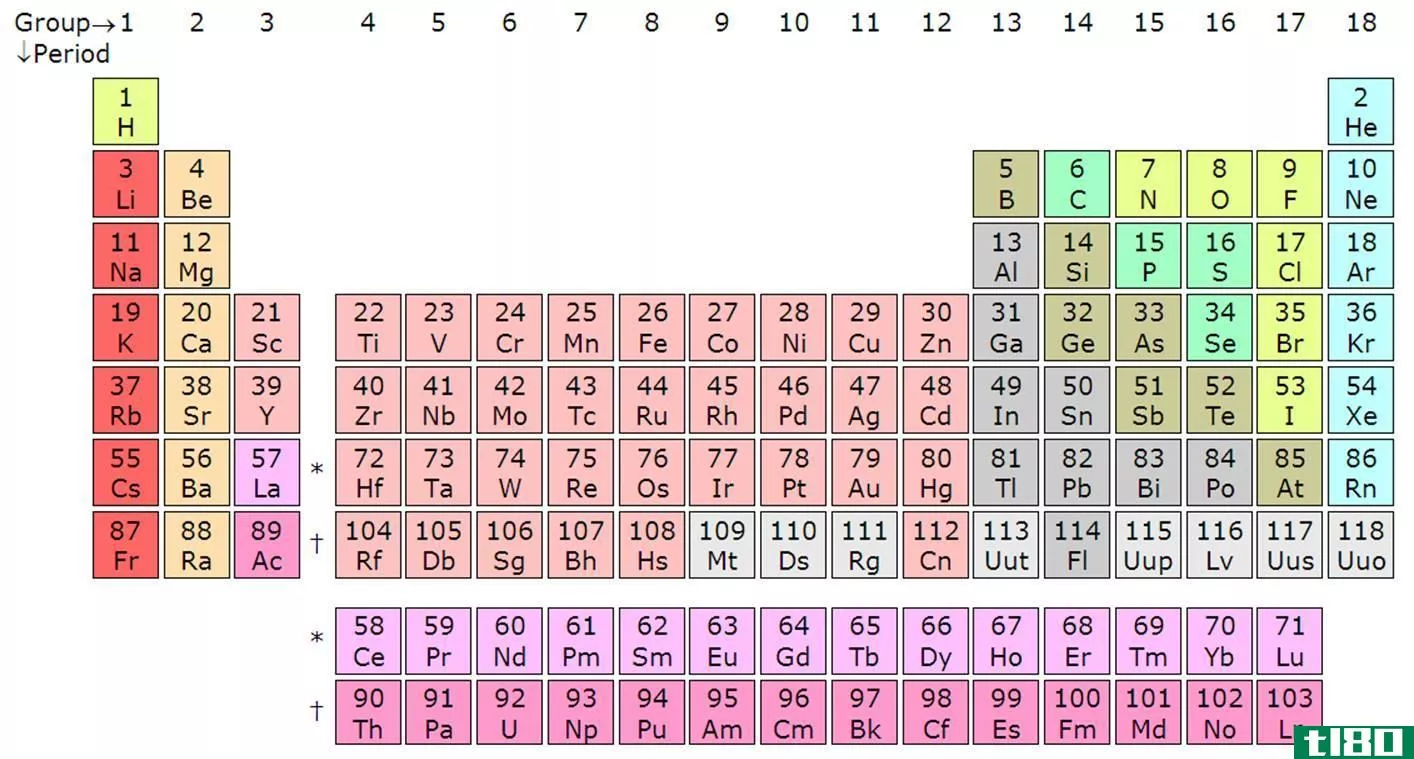
组是元素周期表中的垂直列。同一组中的所有化学元素含有相等数量的价电子。例如,第1组中的价电子数是1。大多数情况下,同一组元素的化学和物理性质有些相似。周期表中主要有18个类群。然而,有些群体也有共同的名字。例如,我们称第一族元素为碱金属,第二族元素称为碱土金属。
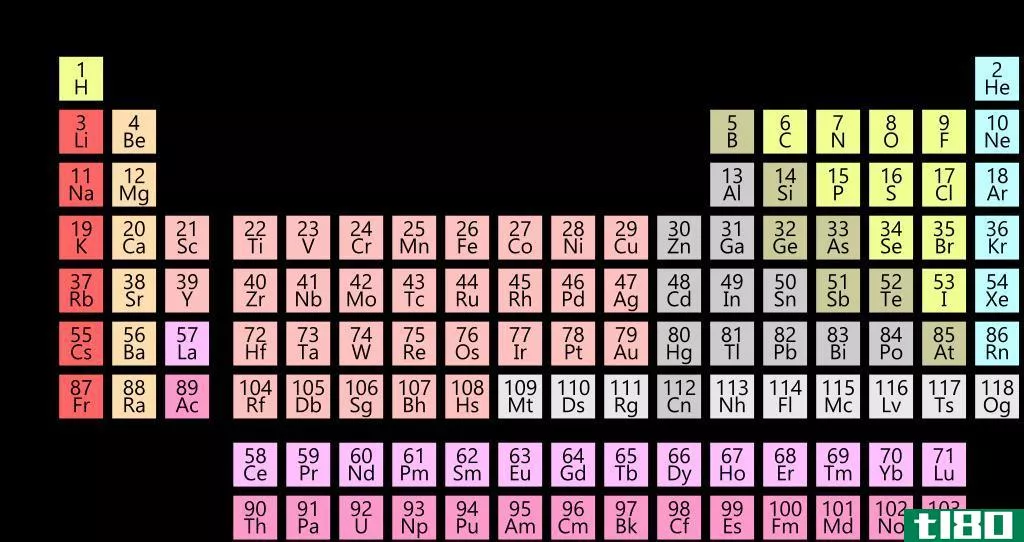
图01:周期表中的周期和组
其中一些常用名称如下:
- Group 1 = alkali metals
- Group 2 = alkaline earth metals
- Group 11 = coinage metals
- Group 12 = volatile metals
- Group 17 = halogens
时期(periods)和周期表中的群(groups in periodic table)的区别
周期是周期表中的水平行,而组是周期表中的垂直列。因此,这就是周期表中周期和组之间的关键区别。元素周期表中有7个主要周期和18个组。此外,我们还可以发现电子回旋排列中周期和群之间的另一个区别。相同电子周期的元素的电子数是相同的,而电子在同一个周期内有相同的电子数。

总结 - 时期(periods) vs. 组(groups)
综上所述,周期和群是我们对元素周期表中的化学元素进行分类的两种方式。化学元素周期表中周期和群的关键区别在于周期是水平行,而群是垂直列。
引用
1Helmenstine,Anne-Marie博士,“元素组和周期之间的差异”,ThoughtCo,2017年8月3日。可在此处查阅2。中级,CK12。“非专业化学”,Lumen,Lumen Learning。此处提供
2中级,CK12。“非专业化学”,Lumen,Lumen Learning。