主要区别
强电解质在水中完全电离,是电的良导体,而弱电解质在水中部分离子化,是电的不良导体。
比较图
什么是强电解质(strong electrolytes)?
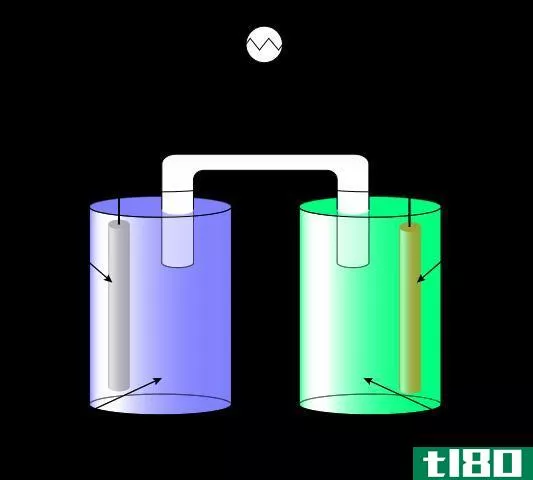
电解液是水溶液中的一种物质,它允许电流通过它并在导电时分解成离子。强电解液是一种当电流通过时完全电离并在水溶液中离解的物质。强电解质是电的优良导体。以前,强电解质被认为是一种存在于水溶液中并导电的化学物质。随着对溶液中离子性质的进一步了解,其定义被目前的定义所取代。在相同温度下,强电解质浓溶液的蒸气压比纯水低。强电解质在原电池中产生更高的电压。强电解质是强酸、强碱和可溶性离子盐,不是弱酸或弱碱。第1组(碱金属)和第2组(碱土金属)的氢氧化物是强碱,因此是强电解质。大多数盐是强电解质。强酸的实例包括高氯酸、氢碘酸、氢溴酸、盐酸、硫酸、硝酸、氯酸、过溴酸、溴酸、周期酸、三氟酸和魔幻酸。强音的例子有氢氧化锂、氢氧化钠、氢氧化钾、氢氧化铷、氢氧化钙、酰胺钠、氢化钠和氢氧化钡。强盐的例子是氯化钠、硝酸钾、乙酸钠和氯化镁。
什么是弱电解质(weak electrolytes)?
弱电解质是在水溶液中不电离的电解质。溶液中含有电解质的离子和分子。除少数酸外,大多数酸都是弱电解质。醋酸和醋酸都是弱酸和电解质。物质在水中的溶解并不是决定其作为电解液强度的因素。这意味着溶解和离解是不同的现象。例如,醋酸是醋中的一种酸,它很容易溶于水。然而,绝大多数的醋酸残留物都是原样的,而不是游离态的乙酸酯。平衡反应在这方面起着重要作用。醋酸溶于水时,会电离成氢离子和乙醇酸盐,但平衡位置在左边。这意味着当乙醇酸和氢离子形成时,它们会迅速返回醋酸和水:
CH3COOH+H2O⇆CH3COO–+H3O+
少量的乙酸酯使醋酸成为弱电解质而不是强电解质。
主要区别
- 弱电解质在水中部分电离约1%-10%。
- 强电解质在水中完全100%电离。
- 强电解质在中等浓度下完全离解。
- 弱电解质在中等浓度下不能完全离解。
- 强电解质的电导随稀释度的增加而增大,但在一定程度上有所增加。
- 弱电解质的电导在稀释时迅速增加,特别是在无限稀释时。
- 强电解质在中等浓度下有很强的离子间相互作用。
- 弱电解质即使在较高的含量下也没有很强的离子间相互作用。